Clear Sky Science · fr
Détection polyvalente et portable, médiée par Cas12a, des marqueurs de résistance aux antibiotiques
Pourquoi il est important de suivre des agents invisibles
La résistance aux antibiotiques paraît abstraite jusqu’à ce qu’une infection courante ne réponde plus aux médicaments. Des bactéries capables d’échapper à nos traitements apparaissent non seulement dans les hôpitaux, mais aussi dans les élevages, les rivières et les sols. Pour rester en avance sur cette menace, les chercheurs ont besoin de méthodes rapides et abordables pour repérer, partout où elles apparaissent, les signatures génétiques annonciatrices de la résistance. Cet article décrit une nouvelle boîte à outils de laboratoire, appelée C12a, qui utilise la technologie CRISPR d’édition de gènes pour détecter des gènes clés de résistance chez des bactéries provenant de personnes, d’animaux et de l’environnement.
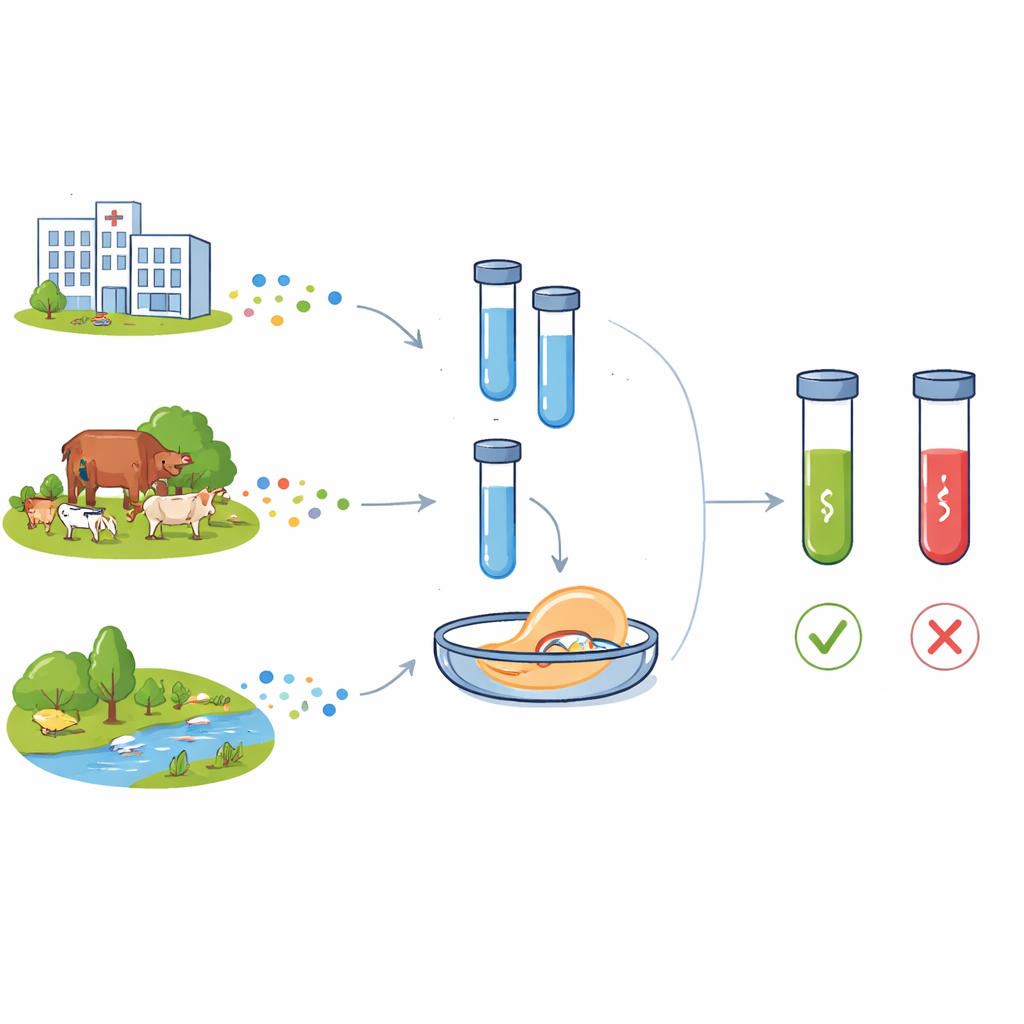
Un problème croissant qui dépasse les murs des hôpitaux
Les antibiotiques modernes ont transformé la médecine, faisant de maladies autrefois mortelles des affections traitables et permettant des chirurgies complexes et des soins intensifs. Mais l’usage intensif en médecine humaine, en production animale et la mauvaise épuration des déchets ont accéléré l’évolution et la propagation de la résistance aux antimicrobiens. Deux gènes de résistance sont particulièrement préoccupants : blaCTX-M-15, qui protège les bactéries contre une vaste classe d’antibiotiques bêta‑lactamines utilisés chez l’humain, et floR, qui confère une protection contre les amphenicols largement employés en médecine vétérinaire. Les deux gènes se retrouvent désormais chez des bactéries issues d’hôpitaux, de la communauté, d’exploitations agricoles et d’eaux, circulant souvent entre espèces via des éléments génétiques mobiles. Un autre élément génétique, l’intégron de classe 1 (suivi par le gène intI1), porte fréquemment des grappes de gènes de résistance et est considéré comme un marqueur d’un fort impact humain sur les écosystèmes microbiens.
Transformer CRISPR en détecteur de résistance
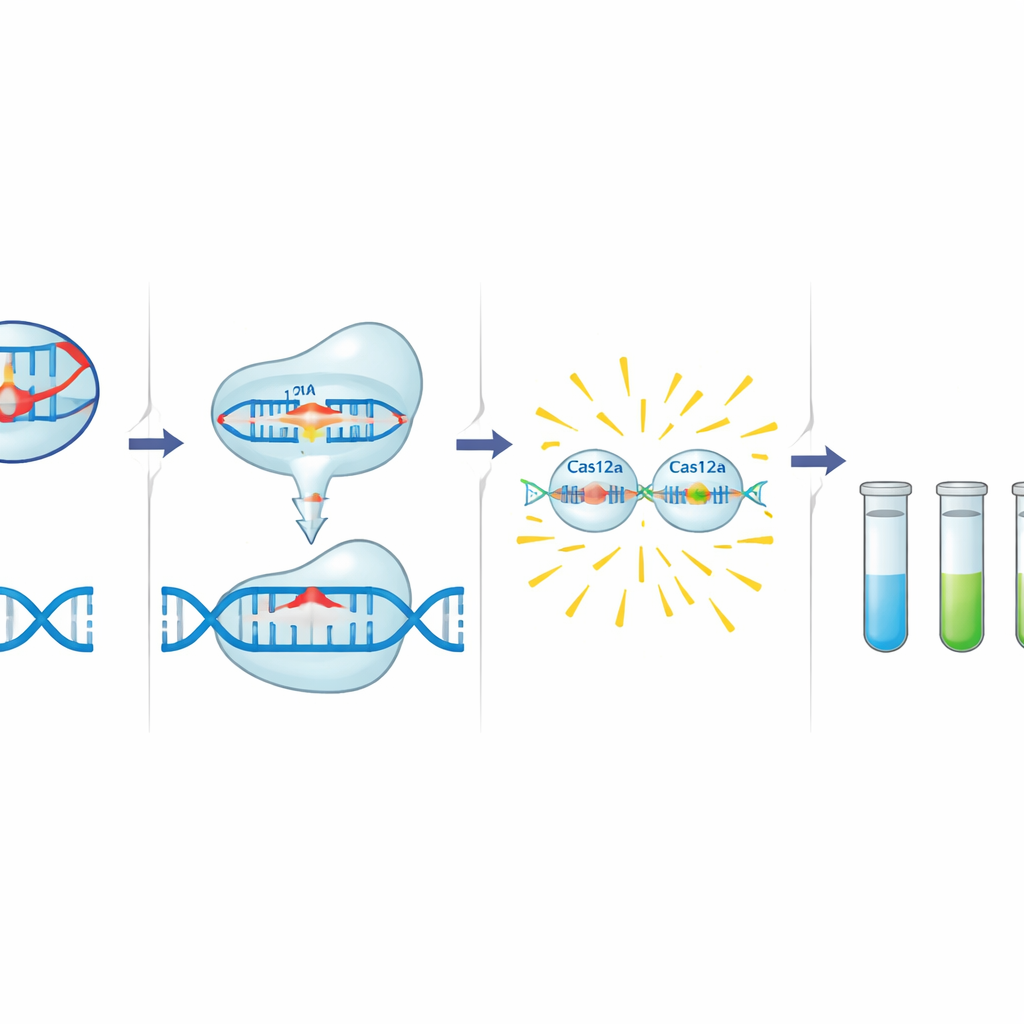
La boîte à outils C12a s’appuie sur Cas12a, une enzyme associée à CRISPR qui peut être programmée par un court ARN guide pour reconnaître une séquence d’ADN spécifique. Lorsque Cas12a trouve sa cible à côté d’un court motif déclencheur, elle coupe d’abord cet ADN puis commence rapidement à cliver l’ADN simple brin à proximité. Les auteurs exploitent ce comportement en ajoutant une petite sonde d’ADN marquée par un colorant fluorescent et un éteigneur. En présence d’un gène de résistance, Cas12a activée tranche la sonde, libérant un signal lumineux. Avant cette étape de détection, une réaction PCR standard amplifie une petite région du gène cible incluant à la fois le motif déclencheur de Cas12a et le site de liaison du guide, ajoutant une seconde couche de spécificité. L’équipe a conçu et optimisé des guides et des amorces pour trois cibles : blaCTX-M-15 (C12abCTX), floR (C12aFLO) et le gène de l’intégrase de l’intégron de classe 1 intI1 (C12aINT).
Quelle est la sensibilité et la fiabilité de la boîte à outils ?
Pour évaluer les performances, les chercheurs ont mesuré la plus faible quantité d’ADN que le système pouvait détecter de manière fiable. En utilisant des fragments purifiés des gènes cibles, C12abCTX et C12aFLO ont détecté des concentrations aussi basses que 70 et 50 attomolaires, respectivement — bien en dessous de ce qu’on observe en simple migration des produits PCR sur gel. Lors des tests sur cultures bactériennes réelles, les essais ont pu détecter environ 77 cellules par millilitre pour blaCTX-M-15 et 173 cellules par millilitre pour floR. Dans des collections d’Escherichia coli provenant d’échantillons de selles d’enfants, les résultats de la boîte à outils C12a concordaient avec les tests standards de sensibilité aux antibiotiques et, lorsque disponibles, avec le séquençage complet du génome : les échantillons positifs génétiquement pour les gènes de résistance donnaient de forts signaux fluorescents, tandis que les échantillons négatifs restaient au niveau du bruit de fond.
Lier les gènes de résistance à un risque plus large
Les auteurs ont aussi exploré si leurs outils pouvaient signaler des bactéries portant de nombreux traits de résistance simultanément. En utilisant C12aINT, ils ont recherché dans les mêmes isolats le gène de l’intégrase de l’intégron de classe 1. Ils ont trouvé intI1 dans presque tous les échantillons portant soit blaCTX-M-15 soit floR. Les analyses génomiques ont montré que ces intégrons hébergeaient souvent des groupes de gènes conférant une résistance à plusieurs familles d’antibiotiques et même à des désinfectants, bien que les gènes cibles principaux de cette étude se trouvent habituellement ailleurs dans le génome. Cela soutient l’idée que le suivi de intI1 peut servir de proxy pratique pour la pression antibiotique d’origine humaine et la multirésistance, tout en soulignant la nécessité de tester directement des gènes spécifiques à haut risque.
Du laboratoire hautement équipé au kit sur le terrain
Un atout majeur de la boîte à outils C12a est son adaptabilité à différentes réalités de laboratoire. Dans un environnement entièrement équipé, les réactions étaient mesurées avec un lecteur de microplaques, produisant des courbes quantitatives au fil du temps. Dans des laboratoires plus simples, les mêmes réactions pouvaient être visualisées avec un transilluminateur à lumière bleue basique, où seules les tubes contenant des gènes de résistance brillaient. Pour les tests portables sur site, l’équipe a remplacé la lecture par fluorescence par des bandes à flux latéral, similaires à un test de grossesse, qui montraient des bandes uniquement lorsque la réaction CRISPR avait été activée. À travers ces configurations et types d’échantillons — y compris l’ADN total directement extrait des fèces — la présence ou l’absence des gènes cibles a été identifiée de façon cohérente, avec seulement de modestes pertes de sensibilité dans les modes à ressources limitées.
Ce que cela signifie pour la lutte contre les infections résistantes
Globalement, les résultats présentent C12a comme une plateforme polyvalente de preuve de concept pour surveiller la circulation des gènes de résistance aux antibiotiques chez les personnes, les animaux et dans l’environnement. L’approche n’est pas encore un diagnostic clinique, et elle détecte le potentiel génétique de résistance plutôt que la réponse d’une infection particulière à un traitement. Néanmoins, sa rapidité, ses faibles limites de détection et sa compatibilité avec des instruments sophistiqués comme avec des outils de terrain simples en font un élément prometteur pour de futurs systèmes de surveillance. En facilitant la détection des points chauds de résistance dans les hôpitaux, les exploitations agricoles et les cours d’eau, des boîtes à outils CRISPR comme C12a pourraient aider les responsables de santé publique et les chercheurs à réagir plus rapidement et à concevoir des stratégies plus intelligentes pour préserver l’efficacité des antibiotiques restants.
Citation: Vargas-Reyes, M., Alcántara, R., Alfonsi, S. et al. Versatile and portable Cas12a-mediated detection of antibiotic resistance markers. Sci Rep 16, 11509 (2026). https://doi.org/10.1038/s41598-026-42073-2
Mots-clés: résistance aux antimicrobiens, diagnostics CRISPR, Cas12a, gènes de résistance aux antibiotiques, surveillance One Health