Clear Sky Science · pt
Detecção versátil e portátil mediada por Cas12a de marcadores de resistência a antibióticos
Por que rastrear germes invisíveis importa
Resistência a antibióticos soa abstrata até que uma infecção rotineira deixa de responder ao medicamento. Bactérias que conseguem escapar dos nossos fármacos estão surgindo não apenas em hospitais, mas também em fazendas, rios e solos. Para se manter à frente dessa ameaça, os cientistas precisam de maneiras rápidas e econômicas de identificar os sinais genéticos de resistência onde quer que apareçam. Este artigo descreve uma nova caixa de ferramentas laboratorial, chamada C12a, que usa a tecnologia CRISPR de corte gênico para detectar genes-chave de resistência em bactérias de pessoas, animais e do meio ambiente.
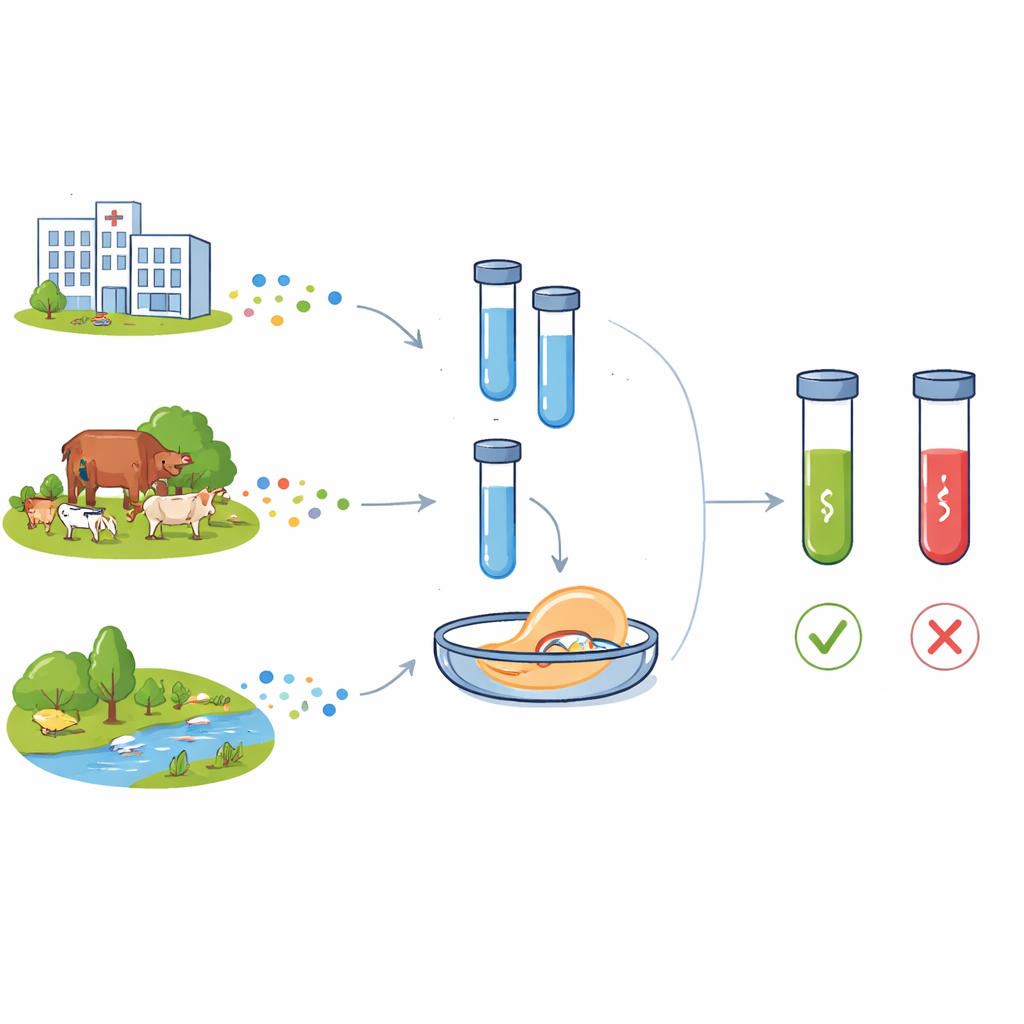
Um problema crescente que atravessa os muros do hospital
Os antibióticos modernos transformaram a medicina, convertendo infecções antes fatais em doenças tratáveis e possibilitando cirurgias complexas e cuidados intensivos. Mas o uso intensivo na medicina humana, na produção animal e o tratamento inadequado de resíduos aceleraram a evolução e a disseminação da resistência antimicrobiana. Dois genes de resistência são especialmente preocupantes: blaCTX-M-15, que protege bactérias de uma ampla classe de antibióticos beta-lactâmicos usados em humanos, e floR, que confere proteção contra amfenicóis amplamente usados em animais. Ambos os genes agora aparecem em bactérias de hospitais, comunidades, fazendas e corpos d’água, frequentemente movimentando-se entre espécies em elementos genéticos móveis. Outro elemento genético, o integron classe 1 (rastreado pelo gene intI1), frequentemente carrega grupos de genes de resistência e é considerado um marcador de forte impacto humano sobre ecossistemas microbianos.
Transformando CRISPR em um detector de resistência
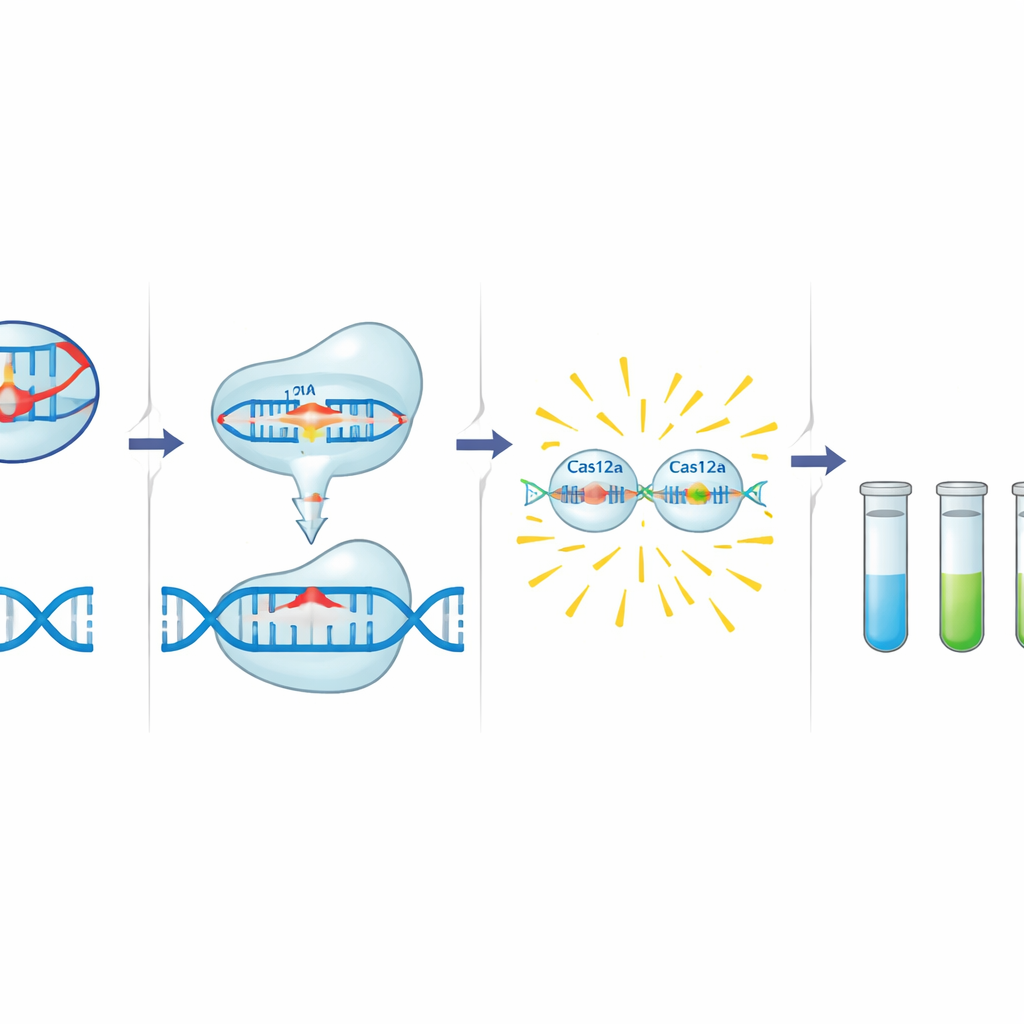
A caixa de ferramentas C12a baseia-se na Cas12a, uma enzima associada ao CRISPR que pode ser programada com um pequeno RNA guia para reconhecer uma sequência específica de DNA. Quando a Cas12a encontra seu alvo ao lado de um curto motivo ativador, ela primeiro corta esse DNA e então começa a degradar rapidamente o DNA de fita simples nas proximidades. Os autores aproveitam esse comportamento adicionando uma minúscula sonda de DNA marcada com um corante fluorescente e um quencher. Na presença de um gene de resistência, a Cas12a ativada corta a sonda, liberando um sinal brilhante. Antes dessa etapa de detecção, uma reação padrão de PCR amplifica uma pequena região do gene alvo que inclui tanto o motivo ativador da Cas12a quanto o sítio de ligação do guia, adicionando uma segunda camada de especificidade. A equipe projetou e otimizou guias e primers para três alvos: blaCTX-M-15 (C12abCTX), floR (C12aFLO) e o gene da integrase do integron classe 1 intI1 (C12aINT).
Quão sensível e confiável é a caixa de ferramentas?
Para avaliar o desempenho, os pesquisadores mediram quanta pouca quantidade de DNA o sistema poderia detectar de forma confiável. Usando fragmentos purificados dos genes alvo, C12abCTX e C12aFLO detectaram concentrações tão baixas quanto 70 e 50 attomolar, respectivamente—muito abaixo do que pode ser observado simplesmente rodando produtos de PCR em um gel. Quando testaram culturas bacterianas reais, os ensaios puderam detectar cerca de 77 células por mililitro para blaCTX-M-15 e 173 células por mililitro para floR. Em coleções de Escherichia coli provenientes de amostras de fezes de crianças, os resultados da caixa C12a corresponderam aos testes padrão de sensibilidade a antibióticos e, quando disponíveis, ao sequenciamento do genoma completo: amostras geneticamente positivas para os genes de resistência apresentaram sinais fluorescentes fortes, enquanto amostras negativas permaneceram em níveis de fundo.
Ligando genes de resistência a um risco mais amplo
Os autores também exploraram se suas ferramentas poderiam identificar bactérias que carregam múltiplas características de resistência ao mesmo tempo. Usando C12aINT, eles procuraram nos mesmos isolados pelo gene da integrase do integron classe 1. Encontraram intI1 em quase todas as amostras que carregavam blaCTX-M-15 ou floR. Análises genômicas mostraram que esses integrons frequentemente hospedavam agrupamentos de genes que conferem resistência a múltiplas famílias de antibióticos e até a desinfetantes, embora os genes-alvo principais deste estudo geralmente estivessem localizados em outras regiões do genoma. Isso apoia a ideia de que rastrear intI1 pode servir como um proxy conveniente para a pressão humana por antibióticos e resistência a múltiplos fármacos, ao mesmo tempo em que ressalta a necessidade de testar diretamente genes de alto risco específicos.
Do laboratório de alta tecnologia ao kit de campo
Uma força chave da caixa de ferramentas C12a é sua adaptabilidade a diferentes realidades laboratoriais. Em um ambiente totalmente equipado, as reações foram medidas com um leitor de microplacas, produzindo curvas quantitativas ao longo do tempo. Em laboratórios mais simples, as mesmas reações podiam ser visualizadas com um transiluminador de luz azul básico, em que apenas tubos contendo genes de resistência brilhavam. Para testes portáteis no local, a equipe substituiu a leitura por fluorescência por tiras de fluxo lateral, semelhantes no formato a um teste de gravidez, que mostraram bandas apenas quando a reação CRISPR havia sido ativada. Nesses formatos e tipos de amostra—incluindo DNA total direto de fezes—a presença ou ausência dos genes alvo foi identificada de forma consistente, com apenas perdas modestas de sensibilidade nos modos de recursos limitados.
O que isso significa para combater infecções resistentes
Em conjunto, os resultados apresentam a C12a como uma plataforma versátil proof-of-concept para monitorar a circulação de genes de resistência a antibióticos entre pessoas, animais e o ambiente. A abordagem ainda não é um diagnóstico clínico e detecta o potencial genético de resistência, em vez de como uma infecção específica responderá ao tratamento. Ainda assim, sua rapidez, baixos limites de detecção e compatibilidade com instrumentos sofisticados e ferramentas simples de campo a tornam um componente promissor para futuros sistemas de vigilância. Ao facilitar a identificação de pontos críticos de resistência em hospitais, fazendas e cursos d’água, caixas de ferramentas baseadas em CRISPR como a C12a podem ajudar autoridades de saúde pública e pesquisadores a reagir mais rápido e a desenhar estratégias mais inteligentes para preservar a eficácia dos antibióticos remanescentes.
Citação: Vargas-Reyes, M., Alcántara, R., Alfonsi, S. et al. Versatile and portable Cas12a-mediated detection of antibiotic resistance markers. Sci Rep 16, 11509 (2026). https://doi.org/10.1038/s41598-026-42073-2
Palavras-chave: resistência antimicrobiana, diagnósticos CRISPR, Cas12a, genes de resistência a antibióticos, vigilância One Health