Clear Sky Science · pl
Wszechstronne i przenośne wykrywanie markerów oporności na antybiotyki za pomocą Cas12a
Dlaczego ważne jest śledzenie niewidocznych zarazków
Oporność na antybiotyki brzmi abstrakcyjnie, dopóki rutynowa infekcja przestaje odpowiadać na leki. Bakterie potrafiące zignorować nasze środki nie pojawiają się już tylko w szpitalach, lecz także na fermach oraz w rzekach i glebach. Aby wyprzedzić to zagrożenie, naukowcy potrzebują szybkich, niedrogich metod wykrywania genetycznych znaków ostrzegawczych oporności w miejscach, gdzie się pojawiają. W artykule opisano nowe narzędzie laboratoryjne nazwane C12a, które wykorzystuje technologię CRISPR do wykrywania kluczowych genów oporności w bakteriach pochodzących od ludzi, zwierząt i ze środowiska.
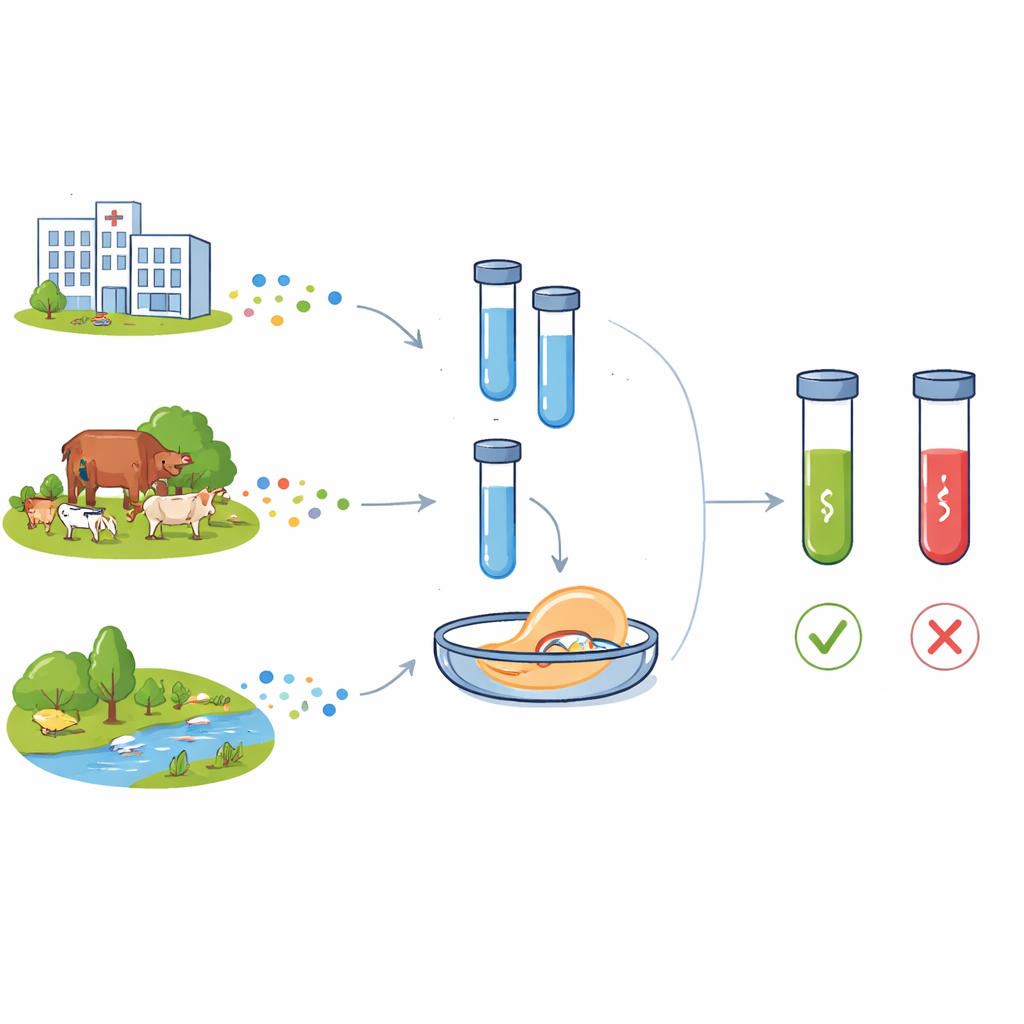
Rosnący problem, który wychodzi poza mury szpitali
Współczesne antybiotyki zrewolucjonizowały medycynę, przekształcając niegdyś śmiertelne infekcje w choroby dające się leczyć oraz umożliwiając skomplikowane operacje i opiekę intensywną. Jednak intensywne stosowanie w medycynie ludzkiej, produkcji zwierzęcej i słabo oczyszczanych ściekach przyspieszyło ewolucję i rozprzestrzenianie się oporności na środki przeciwdrobnoustrojowe. Dwa geny oporności budzą szczególne obawy: blaCTX-M-15, który chroni bakterie przed szeroką klasą beta-laktamów stosowanych u ludzi, oraz floR, zapewniający odporność na amfenikole szeroko stosowane u zwierząt. Oba geny pojawiają się teraz w bakteriach ze szpitali, środowisk społecznych, gospodarstw i wód, często przemieszczając się między gatunkami na ruchomych elementach genetycznych. Inny element genetyczny, integron klasy 1 (śledzony za pomocą genu intI1), często przenosi skupiska genów oporności i jest uważany za marker silnego wpływu działalności człowieka na ekosystemy mikrobiologiczne.
Przekształcanie CRISPR w detektor oporności
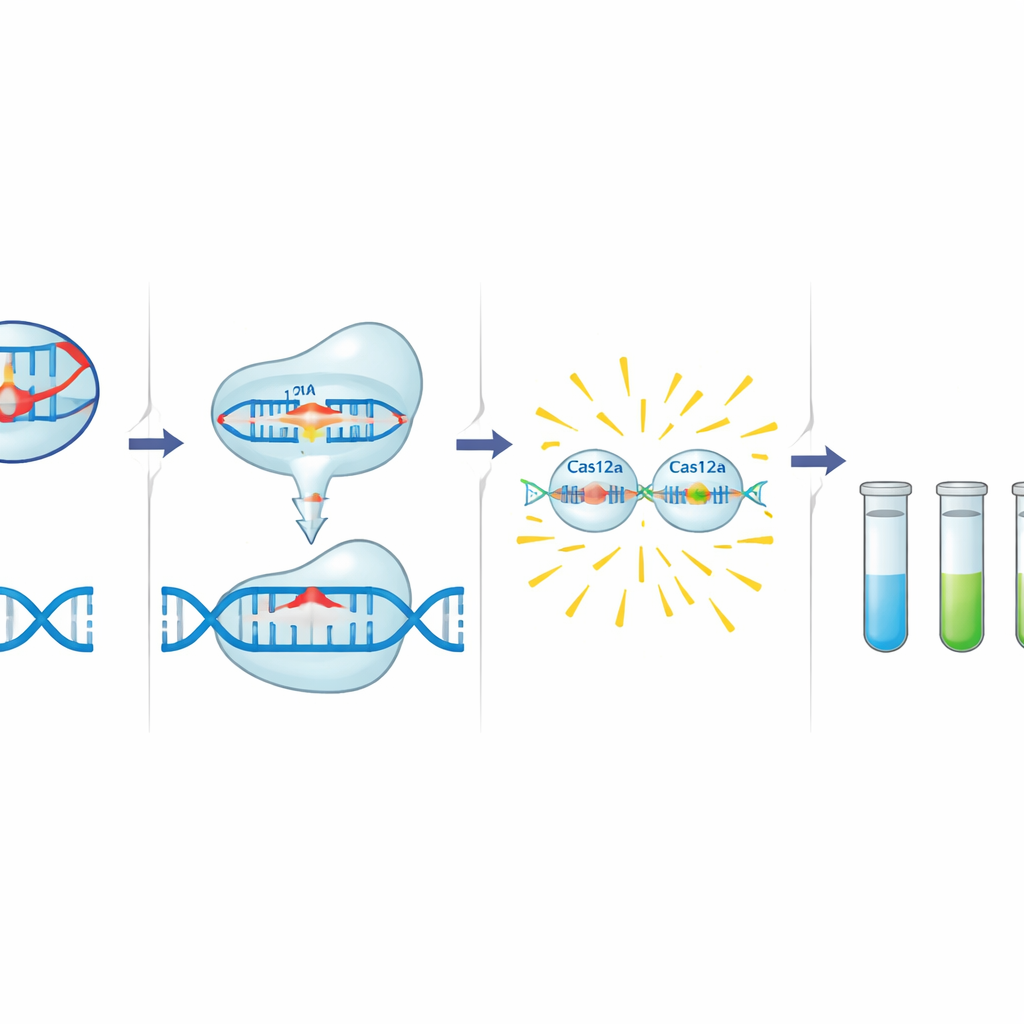
Zestaw narzędzi C12a opiera się na Cas12a, enzymie związanym z CRISPR, który można zaprogramować krótkim RNA przewodnikiem, aby rozpoznać konkretną sekwencję DNA. Gdy Cas12a znajdzie cel obok krótkiego motywu uruchamiającego, najpierw tnie to DNA, a następnie zaczyna szybko rozcinać pobliskie jednoniciowe DNA. Autorzy wykorzystali to zachowanie, dodając maleńką sondę DNA oznakowaną barwnikiem fluorescencyjnym i tłumikiem. W obecności genu oporności aktywowany Cas12a tnie sondę, uwalniając jasny sygnał. Przed tym etapem detekcji standardowa reakcja PCR namnaża mały fragment genu docelowego, który obejmuje zarówno motyw uruchamiający Cas12a, jak i miejsce wiązania przewodnika, co dodaje drugą warstwę specyficzności. Zespół zaprojektował i zoptymalizował przewodniki i startery dla trzech celów: blaCTX-M-15 (C12abCTX), floR (C12aFLO) oraz genu integrazy integronu klasy 1 intI1 (C12aINT).
Jak czuły i niezawodny jest zestaw?
Aby ocenić wydajność, badacze zmierzyli, jak mało DNA system potrafi wykryć w sposób wiarygodny. Używając oczyszczonych fragmentów genów docelowych, C12abCTX i C12aFLO wykrywały stężenia odpowiednio aż do 70 i 50 attomoli—znacznie poniżej progu widocznego po prostym uruchomieniu produktów PCR na żelu. Testując rzeczywiste kultury bakteryjne, assaye były w stanie wykryć około 77 komórek na mililitr dla blaCTX-M-15 i 173 komórek na mililitr dla floR. W kolekcjach Escherichia coli z próbek kału dzieci wyniki z zestawu C12a zgadzały się z standardowymi testami wrażliwości na antybiotyki i, tam gdzie dostępne, z sekwencjonowaniem całogenomowym: próbki genetycznie pozytywne dla genów oporności dawały silne sygnały fluorescencyjne, podczas gdy próbki negatywne pozostawały na poziomie tła.
Łączenie genów oporności z szerszym ryzykiem
Autorzy sprawdzili również, czy ich narzędzia potrafią wykryć bakterie niosące wiele cech oporności jednocześnie. Używając C12aINT, przeszukali te same izolatów w poszukiwaniu genu integrazy integronu klasy 1. Znaleźli intI1 w niemal wszystkich próbkach, które nosiły blaCTX-M-15 lub floR. Analizy genomowe pokazały, że te integrony często zawierały skupiska genów nadających oporność na wiele rodzin antybiotyków, a nawet na środki dezynfekujące, chociaż główne geny celu tego badania zwykle lokalizowały się w innych miejscach genomu. To wspiera pogląd, że śledzenie intI1 może służyć jako wygodny proxy ludzkiego nacisku antybiotykowego i oporności wielolekowej, jednocześnie podkreślając potrzebę bezpośredniego testowania konkretnych genów wysokiego ryzyka.
Z laboratorium zaawansowanego technologicznie do zestawu polowego
Kluczową zaletą zestawu C12a jest jego adaptowalność do różnych warunków laboratoryjnych. W w pełni wyposażonym laboratorium reakcje mierzone były czytnikiem mikropłytek, dając ilościowe krzywe w czasie. W prostszych pracowniach te same reakcje można było obserwować za pomocą podstawowego transiluminatora emitującego niebieskie światło, gdzie świeciły tylko probówki zawierające geny oporności. Dla przenośnych testów w terenie zespół zastąpił odczyt fluorescencyjny paskami typu lateral flow, podobnymi do testu ciążowego, które pokazywały pasma tylko wtedy, gdy reakcja CRISPR została aktywowana. We wszystkich tych konfiguracjach i typach próbek—including całkowite DNA bezpośrednio z kału—obecność lub brak genów docelowych identyfikowano konsekwentnie, z jedynie umiarkowaną utratą czułości w trybach o ograniczonych zasobach.
Co to oznacza dla walki z opornymi infekcjami
W sumie wyniki przedstawiają C12a jako wszechstronną platformę konceptualną do monitorowania genów oporności na antybiotyki krążących między ludźmi, zwierzętami i środowiskiem. Podejście nie jest jeszcze testem klinicznym i wykrywa genetyczny potencjał oporności, a nie to, jak dana infekcja zareaguje na leczenie. Mimo to jego szybkość, niskie progi detekcji oraz kompatybilność zarówno z zaawansowanymi instrumentami, jak i prostymi narzędziami polowymi czynią go obiecującym elementem przyszłych systemów nadzoru. Ułatwiając wykrywanie punktów o wysokiej częstości oporności w szpitalach, gospodarstwach i ciekach wodnych, narzędzia oparte na CRISPR, takie jak C12a, mogą pomóc służbom zdrowia publicznego i badaczom działać szybciej i projektować mądrzejsze strategie zachowania skuteczności pozostałych antybiotyków.
Cytowanie: Vargas-Reyes, M., Alcántara, R., Alfonsi, S. et al. Versatile and portable Cas12a-mediated detection of antibiotic resistance markers. Sci Rep 16, 11509 (2026). https://doi.org/10.1038/s41598-026-42073-2
Słowa kluczowe: oporność na środki przeciwdrobnoustrojowe, diagnostyka CRISPR, Cas12a, geny oporności na antybiotyki, nadzór One Health