Clear Sky Science · nl
Veelzijdige en draagbare Cas12a-gebaseerde detectie van antibioticaresistentiemarkers
Waarom het volgen van onzichtbare ziekteverwekkers ertoe doet
Antibioticaresistentie klinkt abstract totdat een routineinfectie niet meer op medicijnen reageert. Bacteriën die onze geneesmiddelen kunnen negeren duiken niet alleen in ziekenhuizen op, maar ook op boerderijen en in rivieren en bodems. Om deze dreiging voor te blijven, hebben wetenschappers snelle, betaalbare methoden nodig om de genetische waarschuwingssignalen van resistentie waar ook ter wereld te detecteren. Dit artikel beschrijft een nieuwe laboratoriumtoolbox, genaamd C12a, die CRISPR-genkniptechnologie gebruikt om belangrijke resistentiegenen in bacteriën van mensen, dieren en het milieu aan te tonen.
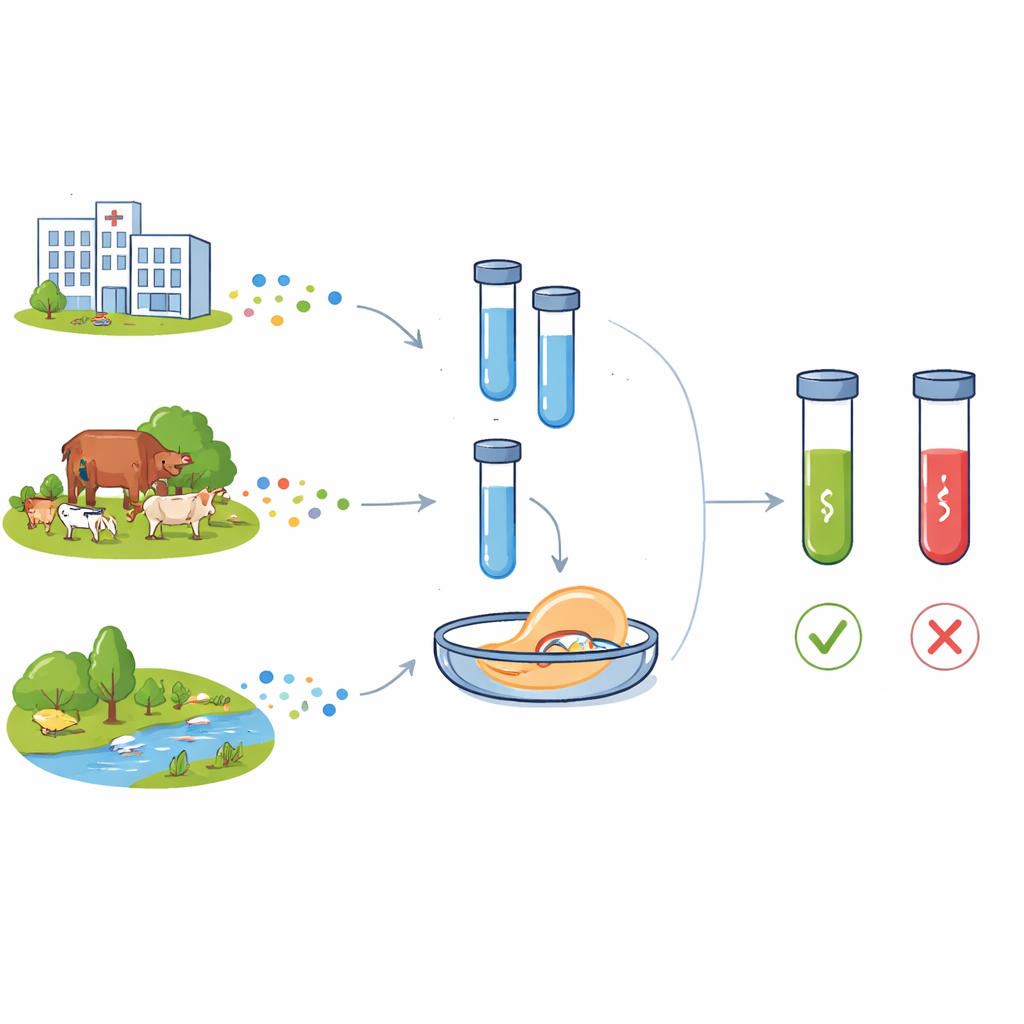
Een groeiend probleem dat ziekenhuismuren overstijgt
Moderne antibiotica hebben de geneeskunde getransformeerd, door ooit dodelijke infecties behandelbaar te maken en complexe chirurgie en intensive care mogelijk te maken. Maar intensief gebruik in de menselijke geneeskunde, de veehouderij en slecht behandeld afval heeft de evolutie en verspreiding van antimicrobiële resistentie versneld. Twee resistentiegenen zijn bijzonder zorgwekkend: blaCTX-M-15, dat bacteriën beschermt tegen een brede klasse beta-lactamantibiotica die bij mensen worden gebruikt, en floR, dat beschermt tegen amfenicol‑middelen die veel in dieren worden toegepast. Beide genen komen nu voor in bacteriën uit ziekenhuizen, gemeenschappen, boerderijen en water, en verplaatsen zich vaak tussen soorten via mobiele genetische elementen. Een ander genetisch element, het klasse-1-integron (opgespoord met het intI1-gen), draagt vaak clusters van resistentiegenen en wordt beschouwd als een merker voor sterke menselijke invloed op microbieel milieu.
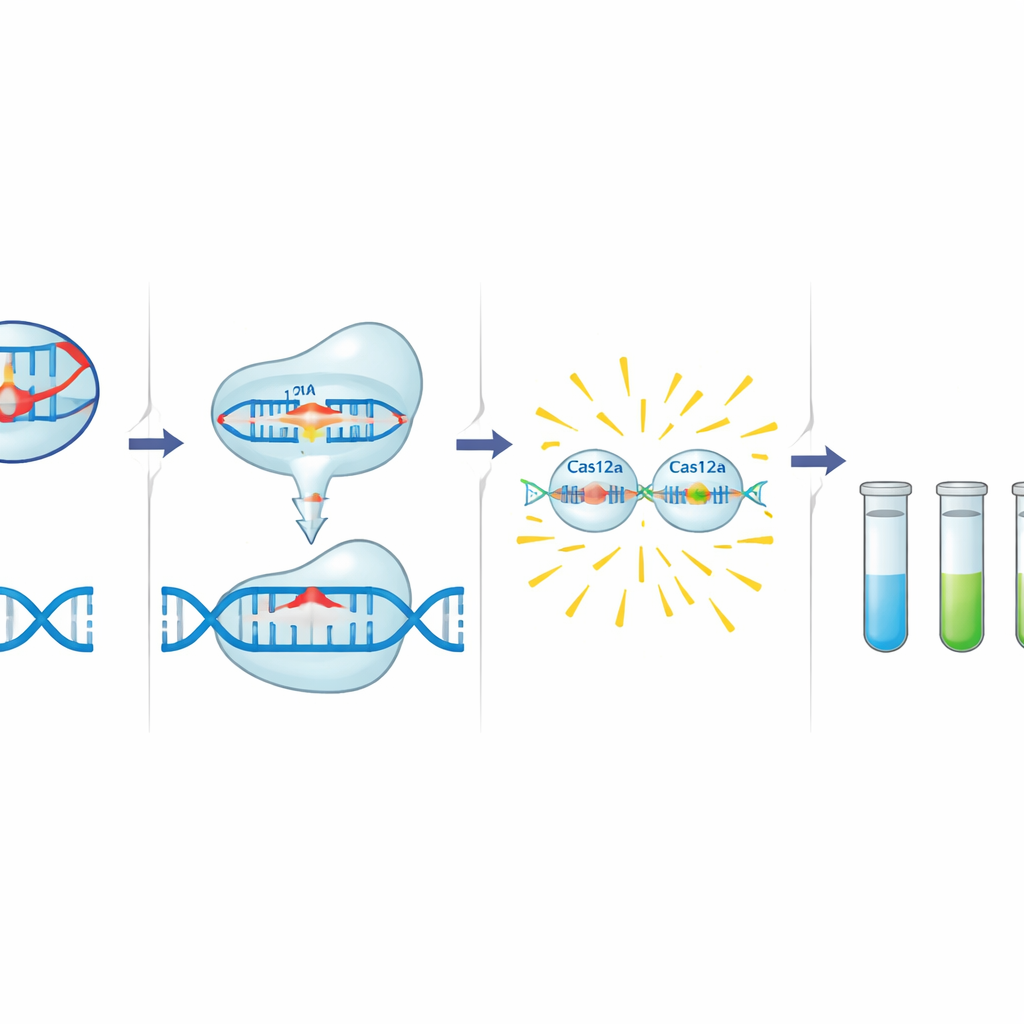
CRISPR omvormen tot een resistentiedetector
De C12a-toolbox bouwt voort op Cas12a, een CRISPR-geassocieerd enzym dat met een korte geleide‑RNA geprogrammeerd kan worden om een specifieke DNA-sequentie te herkennen. Wanneer Cas12a zijn doel naast een korte trigger‑motief vindt, knipt het eerst dat DNA en begint het vervolgens snel nabijgelegen enkelstrengs DNA af te breken. De auteurs benutten dit gedrag door een klein DNA-probe toe te voegen die is gemarkeerd met een fluorescentiekleurstof en een quencher. In aanwezigheid van een resistentiegen snijdt geactiveerde Cas12a de probe door en komt er een helder signaal vrij. Voor deze detectiestap amplificeert een standaard PCR-reactie eerst een klein deel van het doelgen dat zowel het Cas12a-triggermotief als de bindingsplaats van de guide bevat, wat een tweede laag specificiteit toevoegt. Het team ontwierp en optimaliseerde guides en primers voor drie doelen: blaCTX-M-15 (C12abCTX), floR (C12aFLO) en het klasse-1-integron-integrasegen intI1 (C12aINT).
Hoe gevoelig en betrouwbaar is de toolbox?
Om de prestaties te beoordelen, bepaalden de onderzoekers hoeveel DNA het systeem betrouwbaar kon detecteren. Met gezuiverde fragmenten van de doelgenen detecteerden C12abCTX en C12aFLO concentraties zo laag als respectievelijk 70 en 50 attomolair — ver onder wat zichtbaar is door PCR-producten simpelweg op een gel te lopen. Bij tests met echte bacteriekweken konden de assays ongeveer 77 cellen per milliliter voor blaCTX-M-15 en 173 cellen per milliliter voor floR detecteren. In verzamelingen van Escherichia coli uit ontlastingsmonsters van kinderen kwamen de resultaten van de C12a-toolbox overeen met standaard antibioticasusceptibiliteitstests en, waar beschikbaar, whole‑genome sequencing: monsters die genetisch positief waren voor de resistentiegenen gaven sterke fluorescentiesignalen, terwijl negatieve monsters op achtergrondniveau bleven.
Resistentiegenen koppelen aan breder risico
De auteurs onderzochten ook of hun hulpmiddelen bacteriën konden signaleren die meerdere resistentie-eigenschappen tegelijk dragen. Met C12aINT zochten ze in dezelfde isolaten naar het klasse-1-integron-integrasegen. Ze vonden intI1 in bijna alle monsters die ofwel blaCTX-M-15 of floR droegen. Genoomanalyses toonden aan dat deze integrons vaak clusters van genen huisvesten die resistentie tegen meerdere antibioticafamilies en zelfs tegen desinfectiemiddelen verlenen, hoewel de belangrijkste doelgenen van deze studie meestal elders in het genoom waren gelokaliseerd. Dit ondersteunt het idee dat het volgen van intI1 kan dienen als een handig proxy voor door mensen veroorzaakte antibiotica‑druk en multidrugresistentie, terwijl het tegelijkertijd het belang benadrukt van directe detectie van specifieke hoogrisicogenen.
Van hightechlab naar veldkit
Een belangrijke kracht van de C12a-toolbox is de aanpasbaarheid aan verschillende laboratoriumomgevingen. In een volledig uitgeruste setting werden reacties gemeten met een microplaatlezer, wat kwantitatieve curves in de tijd opleverde. In eenvoudigere laboratoria konden dezelfde reacties met een basis blauwe‑licht transilluminator worden beoordeeld, waarbij alleen buisjes met resistentiegenen oplichtten. Voor draagbare, ter plaatse testen verving het team de fluorescentie‑lezing door laterale‑flowstrips, vergelijkbaar met een zwangerschapstest, die alleen banden lieten zien wanneer de CRISPR‑reactie was geactiveerd. Over deze opstellingen en bemonsteringstypen heen — inclusief totaal DNA direct uit feces — werd de aanwezigheid of afwezigheid van de doelgenen consequent geïdentificeerd, met slechts bescheiden verliezen in gevoeligheid in laag‑resource modi.
Wat dit betekent voor het bestrijden van resistente infecties
Samen presenteren de resultaten C12a als een veelzijdig proof‑of‑conceptplatform om antibioticaresistentiegenen te volgen in mensen, dieren en het milieu. De aanpak is nog geen klinische diagnostiek en detecteert het genetische potentieel voor resistentie in plaats van hoe een specifieke infectie op behandeling zal reageren. Toch maken de snelheid, lage detectielimieten en compatibiliteit met zowel geavanceerde instrumenten als eenvoudige veldhulpmiddelen het tot een veelbelovende bouwsteen voor toekomstige surveillance‑systemen. Door het makkelijker te maken resistentiehotspots in ziekenhuizen, boerderijen en waterwegen te signaleren, kunnen CRISPR‑gebaseerde toolboxes zoals C12a volksgezondheidsinstanties en onderzoekers helpen sneller te reageren en slimmer te plannen om de effectiviteit van onze resterende antibiotica te behouden.
Bronvermelding: Vargas-Reyes, M., Alcántara, R., Alfonsi, S. et al. Versatile and portable Cas12a-mediated detection of antibiotic resistance markers. Sci Rep 16, 11509 (2026). https://doi.org/10.1038/s41598-026-42073-2
Trefwoorden: antimicrobiële resistentie, CRISPR-diagnostiek, Cas12a, antibioticaresistentiegenen, One Health surveillance