Clear Sky Science · sv
Integrativt ensemble‑inlärningsramverk för prognoser av kontrollerad läkemedelsfrisättning baserat på Raman‑spektroskopiska signaturer
Varför timing är viktigt för tabletter
Många läkemedel fungerar bäst när de löses upp långsamt och når precis rätt del av tarmen, till exempel kolon, i stället för att frisättas direkt i magen. Att designa dessa ”långverkande” och ”målinriktade” tabletter är komplicerat och kräver ofta många försök i laboratoriet. Denna studie visar hur kombinationen av ljus‑baserade mätningar av tablettbeläggningar och avancerade datormodeller kan förutsäga hur ett läkemedel kommer att frisättas över tid, vilket potentiellt kan minska utvecklingstid, kostnader och avfall.
Från belagda tabletter till smarta prognoser
Forskarna fokuserade på orala tabletter belagda med växtbaserade sockerarter kallade polysackarider, vilka används för att skydda ett läkemedel under passagen genom mag‑tarmkanalen och fördröja frisättningen tills det når kolon. I testfallet användes det vanliga antiinflammatoriska läkemedlet 5‑aminosalicylsyra, ofta använt vid tarmsjukdomar. Istället för att förlita sig enbart på konventionella upplösningstester använde de Ramanspektroskopi, en teknik som belyser ett prov och läser av ett molekylärt ”fingeravtryck” från det spridda ljuset. För varje av 155 belagda formuleringar fångade de mer än 1 500 spektrala drag, antecknade vilken typ av polysackarid och vätskemedium som användes, och mätte hur stor andel läkemedel som hade frisatts efter 2, 8 och 24 timmar under tarmliknande förhållanden.
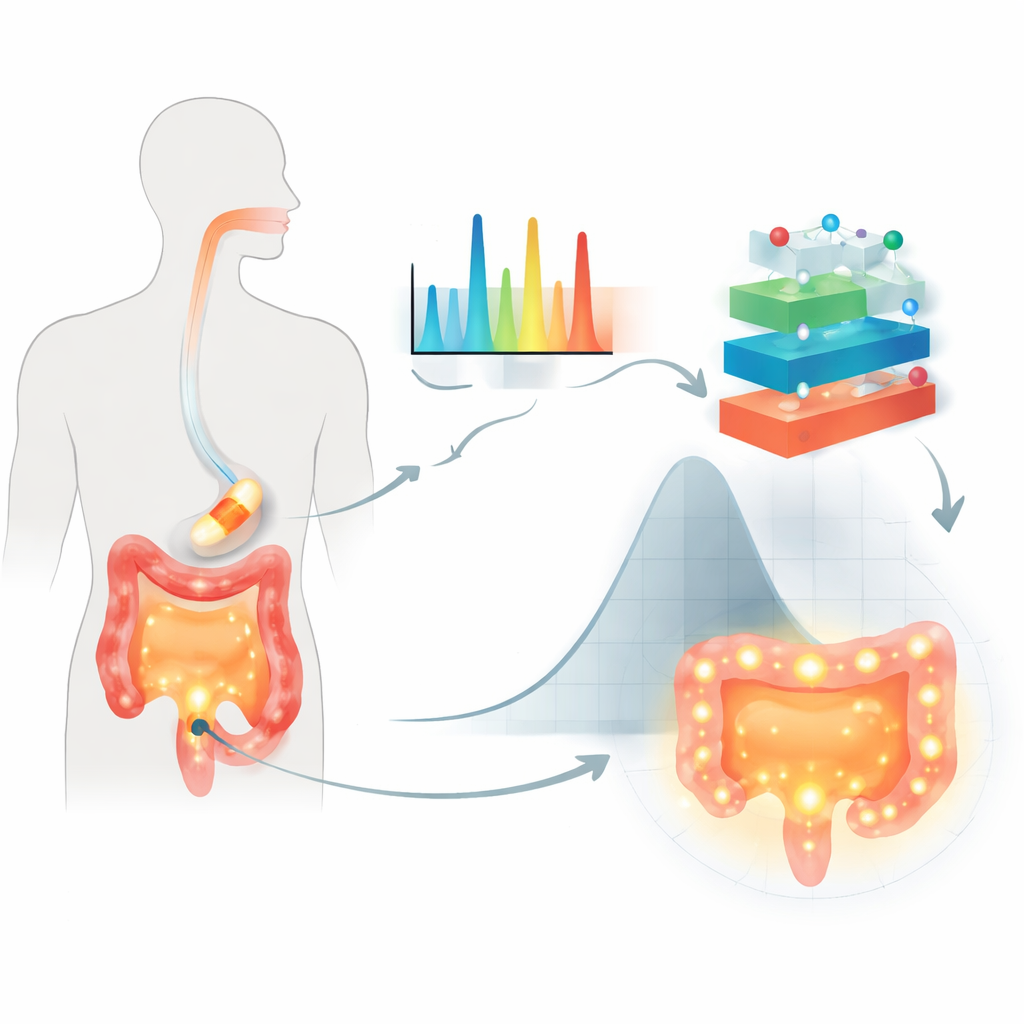
Varför gamla modeller inte räcker till
Traditionella ekvationer för läkemedelsfrisättning antar enkla strukturer och jämn diffusion, vilket ofta inte stämmer överens med den komplicerade verkligheten hos moderna beläggningar och föränderliga tarmmiljöer. De har också svårt att hantera stora, komplexa datamängder, såsom tusentals Raman‑egenskaper som kodar subtila skillnader i polymerstruktur och läkemedels–polymer‑interaktion. Äldre statistiska designmetoder kan hantera flera variabler, men blir opraktiska när många ingredienser och testförhållanden varierar samtidigt. Resultatet blir att viktiga kombinationer kan missas och att modellerna inte pålitligt förutsäger beteende i olika vätskor som efterliknar magen och tarmarna.
Att förena två modeller och två sökstrategier
För att hantera denna komplexitet byggde teamet ett flerskiktat inlärningssystem som kombinerar två maskininlärningsmetoder — XGBoost och AdaBoost — inom ett specialiserat ensemble kallat Damsphere Weighted Ensemble. Istället för att låta en modell dominera justerar ensemblen hur mycket den litar på varje metod baserat på deras prestation, och håller deras inflytande balanserat på en slags matematisk ”sfär”. Ovanpå detta turas två naturinspirerade sökprocedurer, Puma Optimizer och Black‑Winged Kite Algorithm, om att utforska och förfina de många rattar och vred (hyperparametrar) som styr hur modellerna lär sig. Den ena betonar bred utforskning av möjligheter; den andra fokuserar på finslipning av lovande lösningar. Tillsammans söker de efter inställningar som ger precisa, stabila prognoser utan att överanpassa data.
Att läsa tablettens molekylära fingeravtryck
Efter noggrann träning och kontroll med femfaldig korsvalidering och flera felmått förutsade ramverket läkemedelsfrisättning med mycket hög överensstämmelse jämfört med experimenten (förklarade över 99 % av variationen i datan). Lika viktigt var att författarna undersökte vilka indata som betydde mest. Enkla faktorer som tid och typ av medium — som representerar var tabletten kan befinna sig i kroppen — framstod som de starkaste drivkrafterna för frisättning, i linje med känt diffusions‑ och erosionbeteende. Vissa Raman‑band, kopplade till specifika egenskaper hos polysackaridbeläggningarna, stack också ut och länkade molekylär struktur till hur snabbt läkemedlet sippade ut. Statistiska tester bekräftade att dessa mönster inte bara var slumpmässiga egenheter i datasetet utan speglade konsekventa samband.
Vad detta innebär för framtidens läkemedel
För icke‑specialisten är huvudbudskapet att detta tillvägagångssätt fungerar som en smart simulator för belagda tabletter: mata in tablettens molekylära fingeravtryck och testförhållanden, så prognostiserar den hur mycket läkemedel som kommer att frisättas över tid. Även om det inte ersätter detaljerade fysiska modeller eller kliniska prövningar kan det snabbt sålla bland kandidatbeläggningar, avgränsa lovande recept och minska antalet laboratorieexperiment som behövs. Genom att minska materialanvändning och snabba upp utvecklingen stödjer ramverket grönare, mer effektiv läkemedelsdesign och ger en tydligare inblick i varför vissa beläggningar frisätter läkemedel långsamt och pålitligt medan andra inte gör det.
Citering: Albariqi, A.H., Safhi, A.Y., Alqahtani, S.S. et al. Integrative ensemble learning framework for forecasting controlled drug release based on Raman spectral signatures. Sci Rep 16, 11343 (2026). https://doi.org/10.1038/s41598-026-41837-0
Nyckelord: kontrollerad läkemedelsfrisättning, Ramanspektroskopi, maskininlärning, oral läkemedelsadministration, polymerbeläggningar