Clear Sky Science · es
Marco integrador de aprendizaje en conjunto para pronosticar la liberación controlada de fármacos basado en firmas espectrales Raman
Por qué importa el momento de liberación de las pastillas
Muchos medicamentos funcionan mejor cuando se disuelven lentamente y llegan al lugar preciso del intestino, como el colon, en lugar de liberarse todos de golpe en el estómago. Diseñar estas pastillas “de acción prolongada” y “dirigidas” es complicado y suele requerir muchos experimentos de ensayo y error en el laboratorio. Este estudio muestra cómo combinar mediciones ópticas de los revestimientos de las pastillas con modelos informáticos avanzados puede predecir cómo se liberará un fármaco a lo largo del tiempo, reduciendo potencialmente el tiempo de desarrollo, el coste y los residuos.
De tabletas recubiertas a predicciones inteligentes
Los investigadores se centraron en comprimidos orales recubiertos con azúcares de origen vegetal llamados polisacáridos, usados para proteger el fármaco durante su paso por el tracto digestivo y retrasar su liberación hasta alcanzar el colon. Su caso de prueba fue un antiinflamatorio común, el ácido 5‑aminosalicílico, empleado a menudo para tratar enfermedades intestinales. En lugar de depender únicamente de pruebas convencionales de disolución, usaron espectroscopía Raman, una técnica que ilumina una muestra y lee una “huella” molecular en la luz dispersada. Para cada una de las 155 formulaciones recubiertas registraron más de 1.500 características espectrales, anotaron qué tipo de polisacárido y medio líquido se usó, y midieron cuánto fármaco se había liberado tras 2, 8 y 24 horas en condiciones que imitan el intestino.
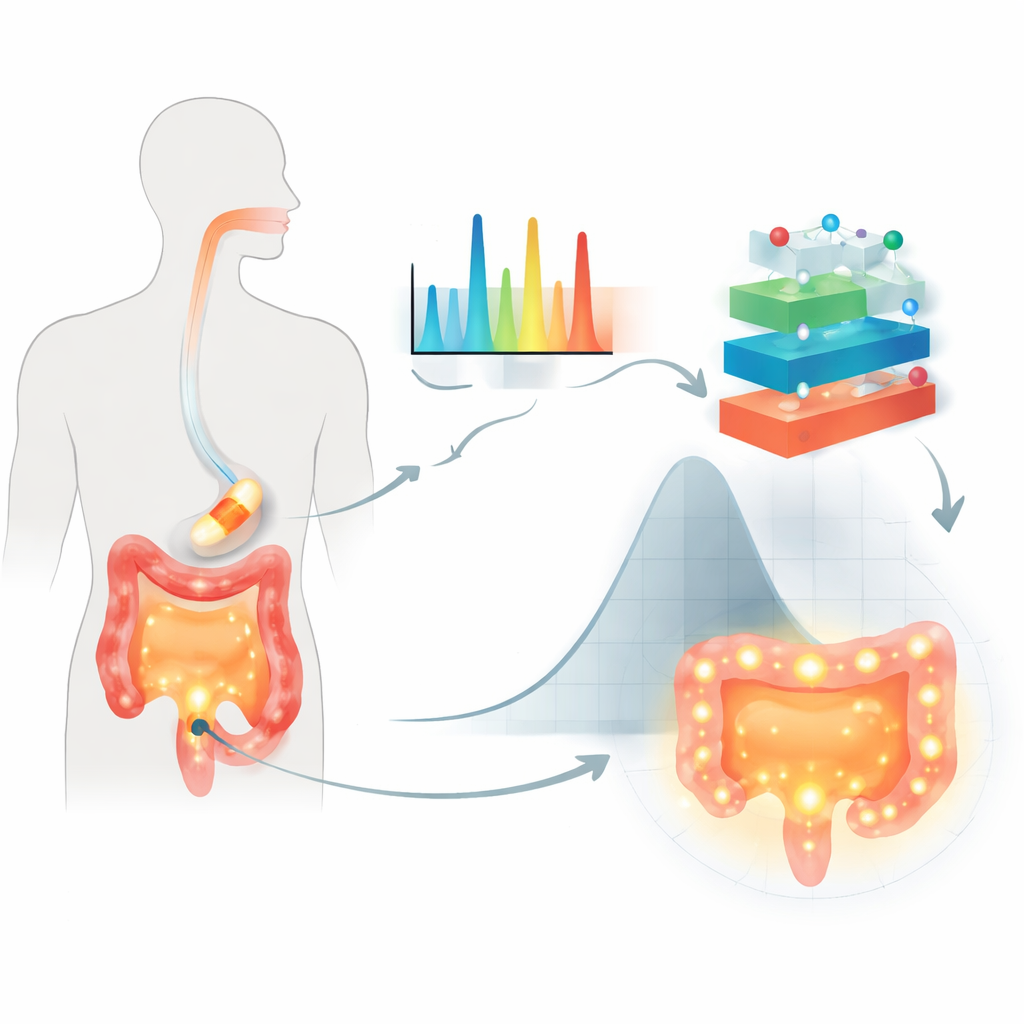
Por qué los modelos tradicionales se quedan cortos
Las ecuaciones tradicionales para la liberación de fármacos suponen estructuras simples y difusión suave, hipótesis que con frecuencia no reflejan la realidad compleja de los revestimientos modernos y los entornos intestinales cambiantes. Tampoco manejan bien conjuntos de datos grandes y complejos, como miles de características Raman que codifican diferencias sutiles en la estructura polimérica y la interacción fármaco‑polímero. Los métodos estadísticos clásicos de diseño pueden abordar múltiples variables, pero se vuelven engorrosos cuando cambian a la vez muchos ingredientes y condiciones de ensayo. El resultado es que combinaciones importantes pueden pasarse por alto y los modelos pueden no predecir con fiabilidad el comportamiento en medios distintos que simulan estómago e intestinos.
Combinando dos enfoques y dos estrategias de búsqueda
Para abordar esta complejidad, el equipo construyó un sistema de aprendizaje por capas que combina dos métodos de aprendizaje automático—XGBoost y AdaBoost—dentro de un ensamblado especializado llamado Damsphere Weighted Ensemble. En lugar de dejar que un modelo domine, el ensamblado ajusta cuánto confía en cada método según su rendimiento, manteniendo sus influencias equilibradas sobre una especie de “esfera” matemática. Encima de esto, dos procedimientos de búsqueda inspirados en la naturaleza, el Puma Optimizer y el Black‑Winged Kite Algorithm, se alternan explorando y afinando los múltiples controles (hiperparámetros) que rigen cómo aprenden los modelos. Uno enfatiza la exploración amplia de posibilidades; el otro se centra en el ajuste fino de soluciones prometedoras. Juntos buscan configuraciones que produzcan predicciones precisas y estables sin sobreajustar los datos.
Leyendo la huella molecular de la pastilla
Tras un entrenamiento y validación cuidadosos usando validación cruzada de cinco pliegues y múltiples medidas de error, el marco predijo la liberación del fármaco con una concordancia muy alta respecto a los experimentos (explicando más del 99% de la variación en los datos). Igualmente importante, los autores investigaron qué entradas eran las que más influían. Factores sencillos como el tiempo y el tipo de medio—representando dónde podría estar la pastilla en el cuerpo—surgieron como los principales determinantes de la liberación, en línea con el comportamiento conocido de difusión y erosión. Ciertas bandas Raman, asociadas a rasgos específicos de los recubrimientos polisacarídicos, también destacaron, vinculando la estructura molecular con la velocidad a la que el fármaco se filtraba. Pruebas estadísticas confirmaron que estos patrones no eran meras casualidades del conjunto de datos sino relaciones consistentes.
Qué significa esto para los medicamentos del futuro
Para un público no especializado, el mensaje clave es que este enfoque funciona como un simulador inteligente para pastillas recubiertas: introduce la huella molecular de la pastilla y las condiciones de ensayo, y predice cuánto fármaco se liberará a lo largo del tiempo. Aunque no reemplaza los modelos físicos detallados ni los ensayos clínicos, puede cribar rápidamente revestimientos candidatos, acotar recetas prometedoras y reducir el número de experimentos de laboratorio necesarios. Al disminuir el uso de materiales y acelerar el desarrollo, el marco favorece un diseño de fármacos más eficiente y sostenible, y ofrece una visión más clara de por qué algunos recubrimientos liberan fármacos lenta y confiablemente mientras que otros no.
Cita: Albariqi, A.H., Safhi, A.Y., Alqahtani, S.S. et al. Integrative ensemble learning framework for forecasting controlled drug release based on Raman spectral signatures. Sci Rep 16, 11343 (2026). https://doi.org/10.1038/s41598-026-41837-0
Palabras clave: liberación controlada de fármacos, espectroscopía Raman, aprendizaje automático, administración oral de fármacos, revestimientos poliméricos