Clear Sky Science · he
מסגרת למידה אנסמבל אינטגרטיבית לחיזוי שחרור מבוקר של תרופות המבוססת על חתימות ספקטרליות רמאניות
למה התזמון חשוב בכדורים
תרופות רבות פועלות בצורה הטובה ביותר כאשר הן נמסות לאט ומגיעות לנקודה המדויקת במעי, לדוגמה במעי הגס, במקום להשתחרר בבת אחת בקיבה. עיצוב כדורים "ארוכי‑טווח" ו"מכווני מטרה" מורכב ולעתים קרובות דורש ניסויים רבים של ניסיון וטעייה במעבדה. במחקר זה מראים כיצד שילוב מדידות מבוססות אור של ציפויי הכדורים עם מודלים חישוביים מתקדמים יכול לחזות כיצד תרופה תשתחרר לאורך זמן, ובכך לצמצם זמן פיתוח, עלות ופסולת.
מכדורים מצופים לניבויים חכמים
החוקרים התמקמו בטבליות דרך הפה המצופות בסוכרים מהצומח המכונים פוליסכרידים, המשמשים להגנה על התרופה בזמן שהיא עוברת במערכת העיכול ולעיכוב שחרורה עד שתגיע למעי הגס. מקרה המבחן שלהם היה תרופה אנטי‑דלקתית נפוצה, חומצה 5‑אמינוסליצילית, המיועדת לעיתים קרובות לטיפול במחלות מעיים. במקום להסתמך רק על בדיקות פירוק קונבנציונליות, הם השתמשו בספקטרוסקופיית רמנס — טכניקה שמאירה דגימה וקוראת "טביעת אצבע" מולקולרית מהאור המפוזר. עבור כל אחת מ‑155 הנוסחאות המצופות תועדו יותר מ‑1,500 תכונות ספקטרליות, נרשם סוג הפוליסכריד והנוזל בו השתמשו, ונמדד כמה תרופה שוחררה לאחר 2, 8 ו‑24 שעות בתנאים המדמים את מערכת העיכול.
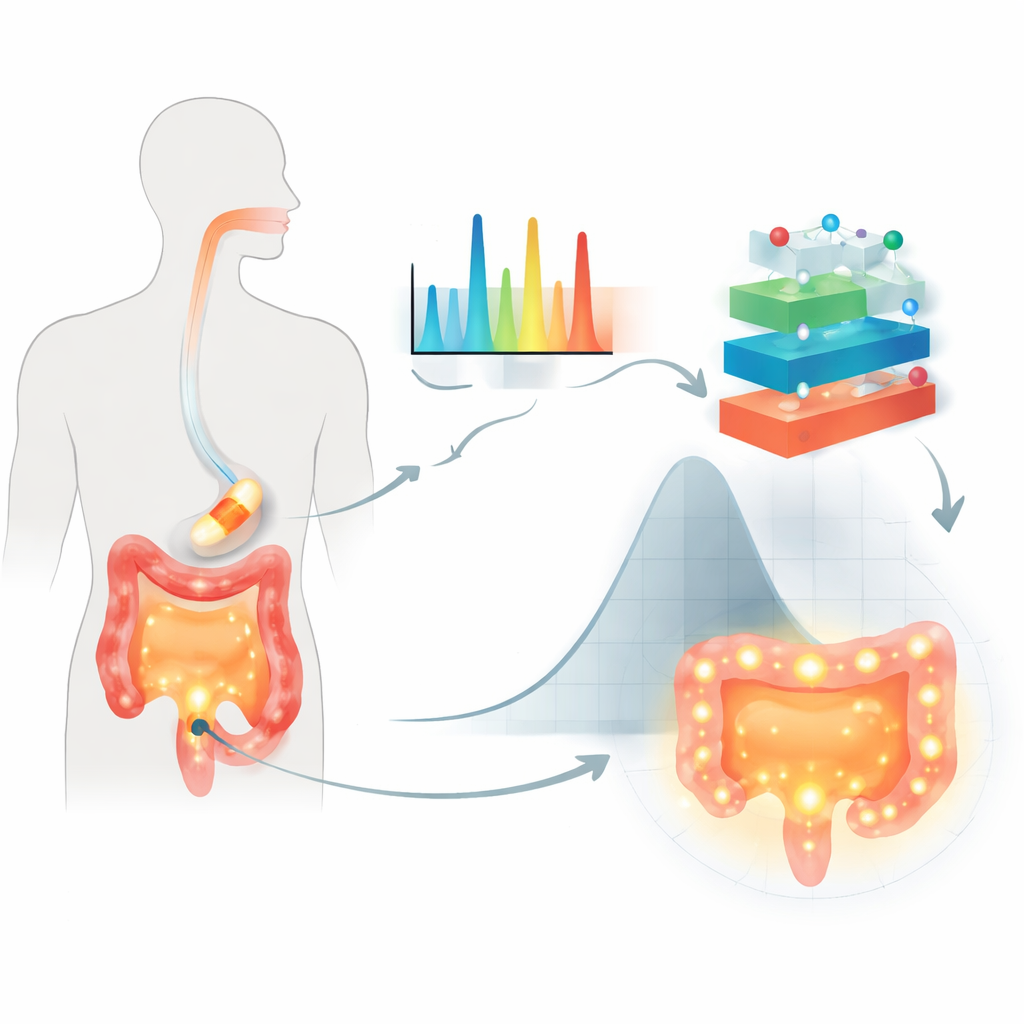
מדוע מודלים ישנים לא עונים על הצרכים
משוואות מסורתיות לשחרור תרופות מניחות מבנים פשוטים ודיפוזיה חלקה, שאינם תואמים לעתים קרובות את המציאות הסבוכה של ציפויים מודרניים וסביבות מעי משתנות. הן מתקשות גם עם מאגרי נתונים גדולים ומורכבים, כגון אלפי תכונות רמאניות שמקודדות הבדלים עדינים במבנה הפולימר ובאינטראקציה בין התרופה לפולימר. שיטות עיצוב סטטיסטיות ישנות יכולות להתמודד עם כמה משתנים, אך נעשות מסורבלות כאשר מרכיבים ותנאי בדיקה רבים משתנים בו‑זמנית. התוצאה היא ששילובים חשובים עלולים להחמצה, והמודלים לא בהכרח חוזים באופן אמין התנהגות בחומרים נוזליים שונים המדמים את הקיבה והמעיים.
שילוב שתי שיטות חשיבה ושתי אסטרטגיות חיפוש
כדי להתמודד עם מורכבות זו, הקבוצה בנתה מערכת למידה פורצת שכבות המשלבת שתי שיטות למידת מכונה — XGBoost ו‑AdaBoost — בתוך אנסמבל מיוחד שנקרא Damsphere Weighted Ensemble. במקום לאפשר למודל אחד לשלוט, האנסמבל מתאים כמה הוא סומך על כל שיטה בהתבסס על ביצועיה, ושומר על איזון השפעותיהן על "כדור" מתמטי. מעל לכך, שני נהלי חיפוש בהשראת טבע — Puma Optimizer ו‑Black‑Winged Kite Algorithm — מחליפים זה את זה בחקר וכיול של כפתורי הבקרה הרבים (היפרפרמטרים) שקובעים כיצד המודלים לומדים. אחד מדגיש חיפוש רחב של אפשרויות; השני מתמקד בכיול עדין של פתרונות מבטיחים. יחד הם מחפשים הגדרות המניבות תחזיות מדויקות ויציבות בלי התאמה יתרה לנתונים.
קריאת טביעת האצבע המולקולרית של הכדור
לאחר אימון ובקרה קפדניים באמצעות חלוקת חמש‑קיפול ומדדי שגיאה מרובים, המסגרת חזה שחרור תרופה בהתאמה גבוהה לניסויים (הסבירה מעל 99% מהשונות בנתונים). כמו כן, המחברים בדקו אילו קלטים חשובים ביותר. גורמים פשוטים כגון הזמן וסוג המדיום — המייצג את מיקום הכדור בגוף — התגלו ככוחות המניעים החזקים ביותר של השחרור, בהתאם להתנהגות דיפוזיה ואבולוציה ידועה. פסי רמנס מסוימים, הקשורים לתכונות ספציפיות של ציפויי הפוליסכריד, בלטו גם הם, וקישרו בין המבנה המולקולרי למהירות הדליפה של התרופה. בדיקות סטטיסטיות אישרו שמבנים אלה אינם סתם שגיאות אקראיות במאגר הנתונים, אלא משקפים יחסים עקביים.
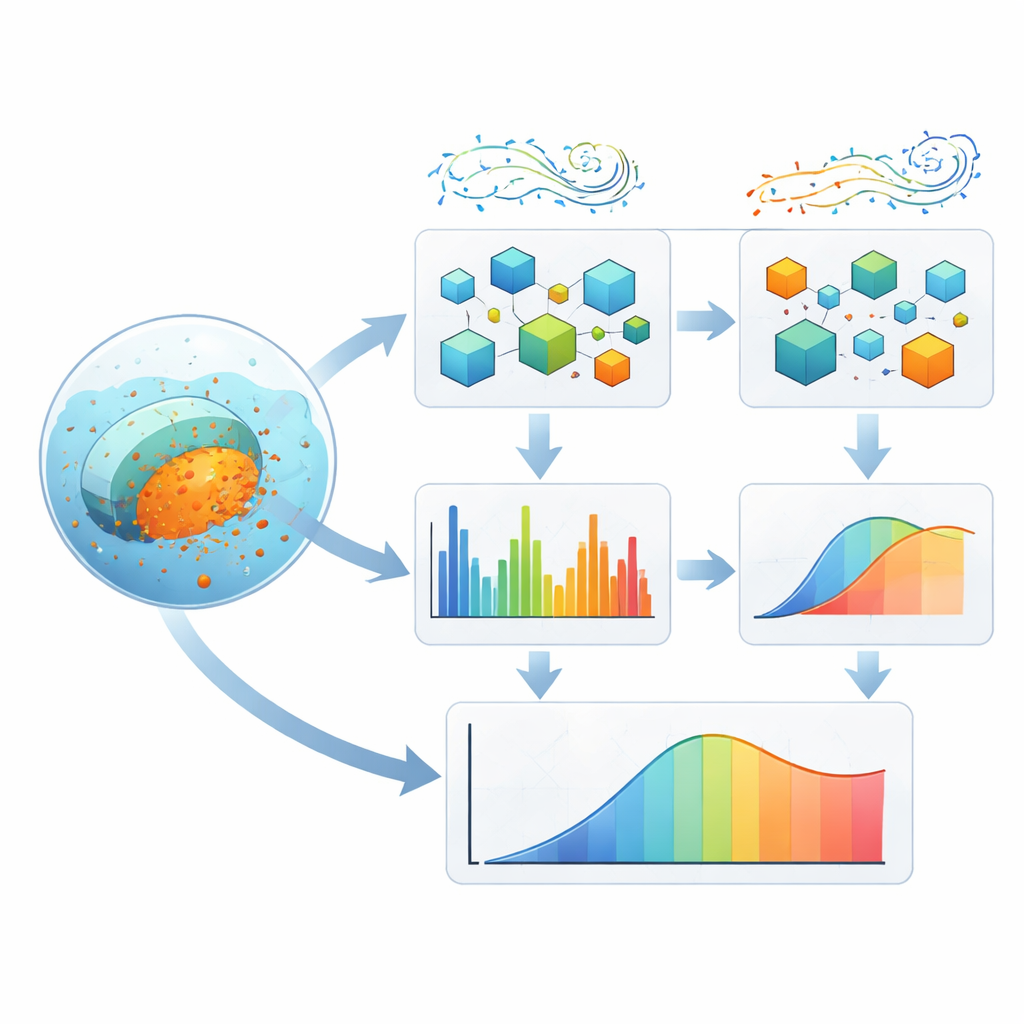
מה משמעות הדבר עבור תרופות עתידיות
עבור הקורא שאינו מומחה, המסר המרכזי הוא שהגישה הזו מתפקדת כסימולטור חכם לכדורים מצופים: מזינים את טביעת האצבע המולקולרית של הכדור ותנאי הבדיקה — והיא חוזה כמה תרופה תשוחרר לאורך זמן. אמנם היא אינה מחליפה מודלים פיזיקליים מפורטים או ניסויים קליניים, אך היא יכולה במהירות לסנן ציפויים מועמדים, לצמצם מתכונים מבטיחים ולהפחית את מספר ניסויי המעבדה הנדרשים. על ידי הקטנת צריכת החומר ומהירות הפיתוח, המסגרת תומכת בעיצוב תרופות יעיל וידידותי יותר לסביבה ומעניקה תובנה ברורה יותר מדוע ציפויים מסוימים משחררים תרופות לאט ובצורה מהימנה בעוד אחרים לא.
ציטוט: Albariqi, A.H., Safhi, A.Y., Alqahtani, S.S. et al. Integrative ensemble learning framework for forecasting controlled drug release based on Raman spectral signatures. Sci Rep 16, 11343 (2026). https://doi.org/10.1038/s41598-026-41837-0
מילות מפתח: שחרור מבוקר של תרופות, ספקטרוסקופיית רמנס, למידת מכונה, אספקת תרופות דרך הפה, ציפויי פולימר