Clear Sky Science · fr
Cadre d’apprentissage ensembliste intégré pour prévoir la libération contrôlée de médicaments à partir de signatures spectrales Raman
Pourquoi le moment compte pour les comprimés
De nombreux médicaments sont plus efficaces lorsqu’ils se dissolvent lentement et atteignent précisément la bonne zone de l’intestin, comme le côlon, plutôt que de se libérer d’un coup dans l’estomac. Concevoir ces comprimés « à action prolongée » et « ciblés » est délicat et exige souvent de nombreux essais‑erreurs en laboratoire. Cette étude montre comment la combinaison de mesures optiques des pelliculages et de modèles informatiques avancés peut prédire la cinétique de libération d’un médicament, réduisant potentiellement le temps, le coût et les déchets liés au développement.
Des comprimés enrobés aux prédictions intelligentes
Les chercheurs se sont concentrés sur des comprimés oraux enrobés de sucres d’origine végétale appelés polysaccharides, utilisés pour protéger le principe actif pendant son transit dans le tube digestif et retarder sa libération jusqu’au côlon. Leur cas test était un anti‑inflammatoire courant, l’acide 5‑aminosalicylique, fréquemment employé pour traiter les maladies intestinales. Plutôt que de s’appuyer uniquement sur des tests de dissolution classiques, ils ont utilisé la spectroscopie Raman, une technique qui éclaire un échantillon et lit un « empreinte » moléculaire dans la lumière diffusée. Pour chacune des 155 formulations enrobées, ils ont capturé plus de 1 500 caractéristiques spectrales, enregistré le type de polysaccharide et le milieu liquide utilisés, et mesuré la fraction de médicament libérée après 2, 8 et 24 heures dans des conditions simulant le tube digestif.
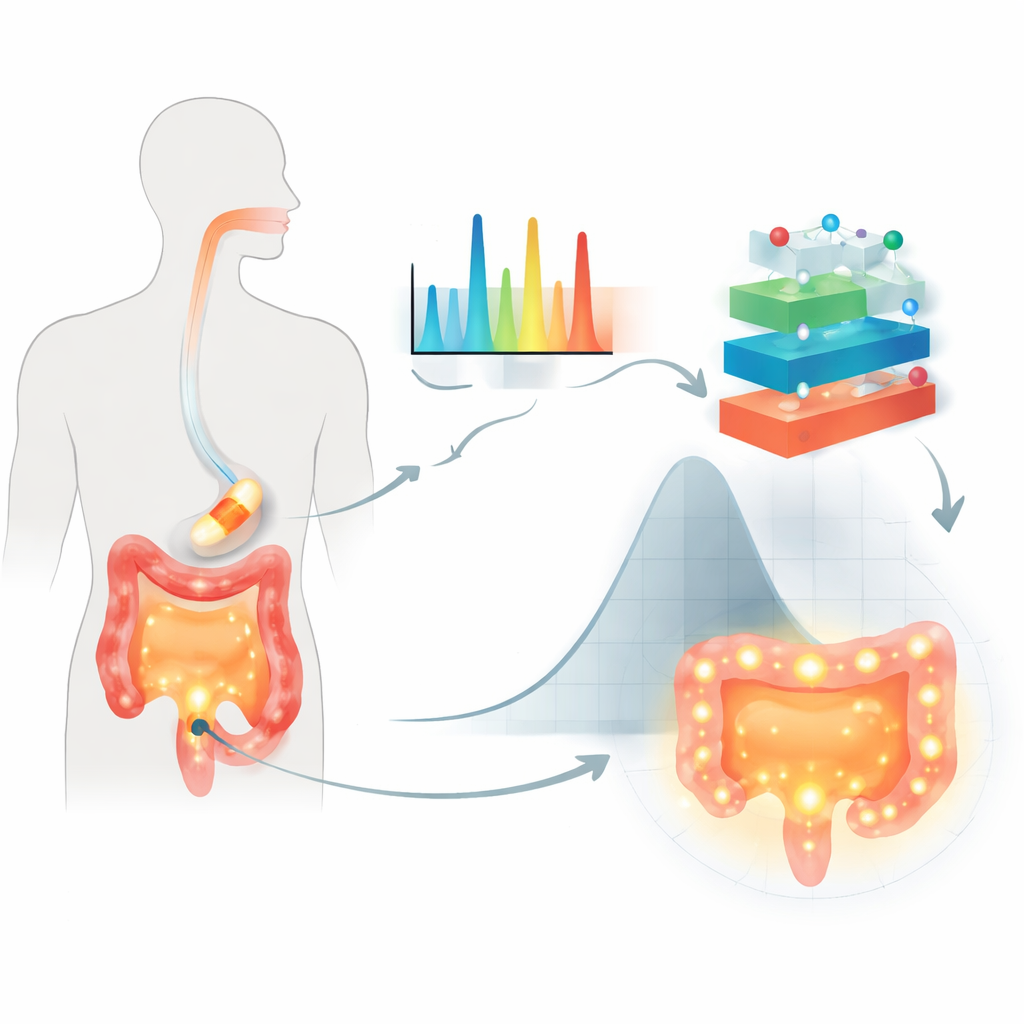
Pourquoi les modèles anciens montrent leurs limites
Les équations traditionnelles de libération supposent des structures simples et une diffusion régulière, ce qui ne correspond souvent pas à la réalité complexe des enrobages modernes et des environnements intestinaux changeants. Elles peinent aussi à gérer de grands jeux de données complexes, comme des milliers de caractéristiques Raman qui codent des différences subtiles de structure polymère et d’interaction médicament‑polymère. Les anciennes méthodes statistiques de planification d’expériences peuvent traiter plusieurs variables, mais deviennent ingérables quand de nombreux ingrédients et conditions d’essai varient simultanément. En conséquence, des combinaisons importantes peuvent être manquées et les modèles risquent de ne pas prédire de façon fiable le comportement dans différents fluides mimant l’estomac et les intestins.
Mélanger deux approches et deux stratégies de recherche
Pour affronter cette complexité, l’équipe a construit un système d’apprentissage en couches qui combine deux méthodes d’apprentissage automatique — XGBoost et AdaBoost — au sein d’un ensemble spécialisé appelé Damsphere Weighted Ensemble. Plutôt que de laisser un modèle dominer, l’ensemble ajuste le poids accordé à chaque méthode selon ses performances, maintenant leurs influences équilibrées sur une sorte de « sphère » mathématique. Par dessus cela, deux procédures de recherche inspirées de la nature, le Puma Optimizer et l’algorithme Black‑Winged Kite, se relaient pour explorer et affiner les nombreux réglages (hyperparamètres) qui gouvernent l’apprentissage des modèles. L’un privilégie une exploration large des possibilités ; l’autre se concentre sur l’affinage des solutions prometteuses. Ensemble, ils cherchent des configurations qui offrent des prédictions précises et stables sans surajuster les données.
Lire l’empreinte moléculaire du comprimé
Après un entraînement et une validation rigoureux par validation croisée à cinq volets et plusieurs mesures d’erreur, le cadre a prédit la libération du médicament avec un très bon accord avec les expériences (expliquant plus de 99 % de la variation des données). Autre point important, les auteurs ont examiné quelles entrées avaient le plus d’impact. Des facteurs simples comme le temps et le type de milieu — représentant l’emplacement possible du comprimé dans le corps — se sont révélés être les principaux moteurs de la libération, en accord avec le comportement connu de diffusion et d’érosion. Certaines bandes Raman, liées à des caractéristiques spécifiques des enrobages polysaccharidiques, se sont également distinguées, reliant la structure moléculaire à la vitesse de diffusion du médicament. Des tests statistiques ont confirmé que ces motifs n’étaient pas de simples artefacts aléatoires du jeu de données, mais reflétaient des relations cohérentes.
Ce que cela signifie pour les médicaments de demain
Pour un non‑spécialiste, le message clé est que cette approche fonctionne comme un simulateur intelligent pour comprimés enrobés : on entre l’empreinte moléculaire du comprimé et les conditions d’essai, et il prédit la quantité de médicament qui sera libérée au fil du temps. Bien que cela ne remplace pas les modèles physiques détaillés ni les essais cliniques, cela permet de présélectionner rapidement des enrobages candidats, de réduire le nombre de recettes à tester et de diminuer le nombre d’expériences en laboratoire nécessaires. En réduisant l’utilisation de matériaux et en accélérant le développement, le cadre favorise une conception de médicaments plus verte et efficiente et offre une vision plus claire des raisons pour lesquelles certains enrobages libèrent les médicaments lentement et de manière fiable, tandis que d’autres ne le font pas.
Citation: Albariqi, A.H., Safhi, A.Y., Alqahtani, S.S. et al. Integrative ensemble learning framework for forecasting controlled drug release based on Raman spectral signatures. Sci Rep 16, 11343 (2026). https://doi.org/10.1038/s41598-026-41837-0
Mots-clés: libération contrôlée de médicament, spectroscopie Raman, apprentissage automatique, administration orale de médicaments, revêtements polymères