Clear Sky Science · ar
إطار تعلم تجميعي تكاملي لتوقع إطلاق الدواء المسيطر استنادًا إلى توقيعات طيف رامان
لماذا التوقيت مهم للأقراص
تعمل العديد من الأدوية بشكل أفضل عندما تذوب ببطء وتصل إلى الموضع المناسب في الأمعاء، مثل القولون، بدلًا من إطلاقها دفعة واحدة في المعدة. تصميم هذه الأقراص «طويلة المدى» والموجهة أمر معقد وعادةً ما يتطلب تجارب مخبرية عديدة عبر التجربة والخطأ. تُظهر هذه الدراسة كيف أن الجمع بين قياسات ضوئية لطلاءات الأقراص ونماذج حاسوبية متقدمة يمكن أن يتنبأ بكيفية إطلاق الدواء بمرور الوقت، مما قد يقلص وقت التطوير والتكلفة والنفايات.
من الأقراص المطلية إلى التنبؤات الذكية
ركز الباحثون على الأقراص الفموية المطلية بسكريات نباتية تُسمى متعددات السكاريد، والمستخدمة لحماية الدواء أثناء مروره في القناة الهضمية وتأخير إطلاقه حتى يصل إلى القولون. كانت حالة الاختبار دواءً مضادًا للالتهاب شائعًا، حمض 5‑أمينوساليسيليك، المستخدم غالبًا لعلاج أمراض الأمعاء. بدلًا من الاعتماد فقط على اختبارات الانحلال التقليدية، استخدموا مطيافية رامان، وهي تقنية تسلط ضوءًا على العينة وتقرأ «بصمة» جزيئية من الضوء المبعثر. لكلٍّ من 155 تركيبة مطلية، سجّلوا أكثر من 1500 ميزة طيفية، وثّقوا نوع متعدد السكاريد والوسط السائلي المستخدم، وقيَسوا كمية الدواء المطروحة بعد 2 و8 و24 ساعة تحت ظروف تحاكي الأمعاء.
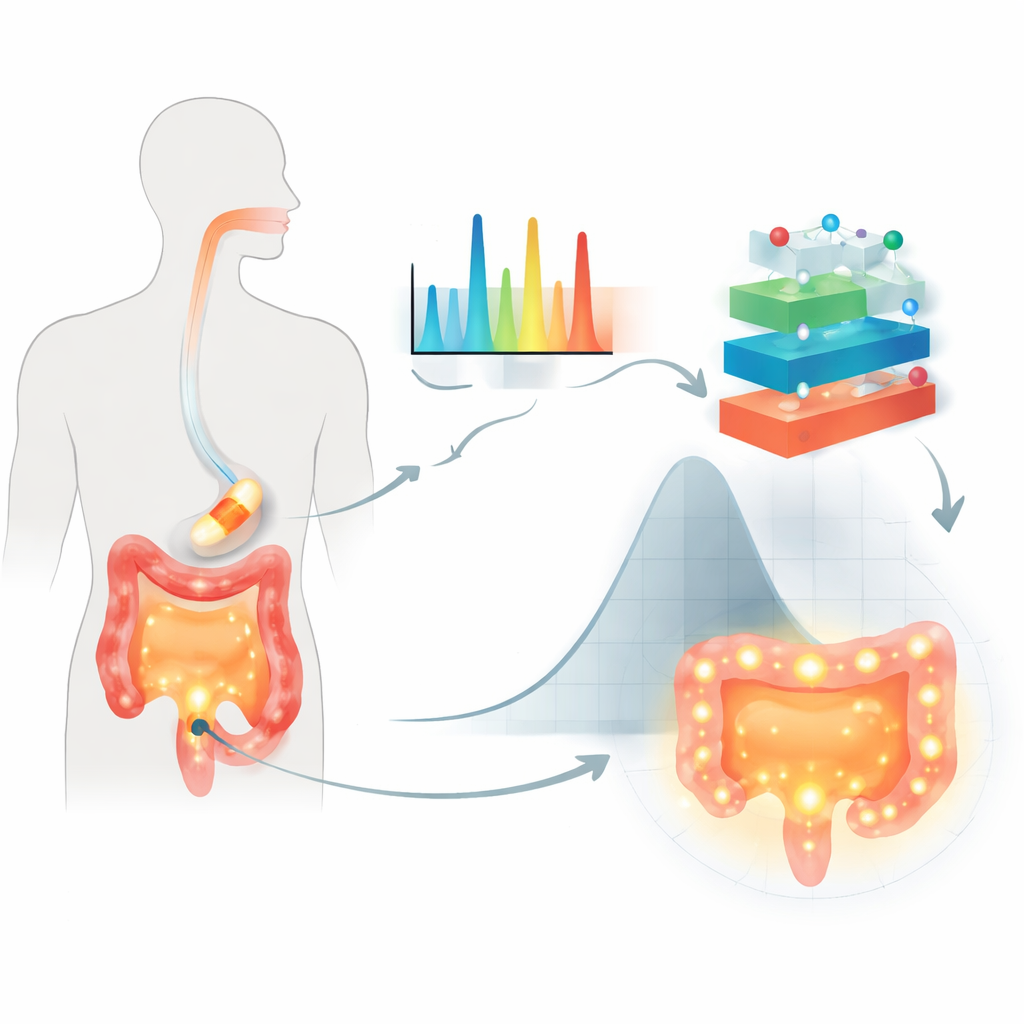
لماذا النماذج القديمة تقصر
تفترض المعادلات التقليدية لإطلاق الدواء تراكيب بسيطة وانتشارًا سلسًا، وهو ما غالبًا لا يتطابق مع واقع الطلاءات المعقدة والبيئات المعوية المتغيرة. كما أنها تواجه صعوبة مع مجموعات البيانات الكبيرة والمعقدة، مثل آلاف ميزات رامان التي تُشفّر اختلافات دقيقة في بنية البوليمر وتفاعل الدواء مع البوليمر. يمكن لأساليب التصميم الإحصائي القديمة التعامل مع متغيرات متعددة، لكنها تصبح صعبة عند تغير العديد من المكونات وظروف الاختبار معًا. النتيجة هي أن توليفات مهمة قد تُغفل، وقد لا تتنبأ النماذج بثقة عبر سوائل مختلفة تحاكي المعدة والأمعاء.
مزج عقلين واستراتيجيتين للبحث
لمعالجة هذه التعقيدات، بنى الفريق نظام تعلم طبقي يجمع بين طريقتين في تعلم الآلة — XGBoost وAdaBoost — داخل تجميعة متخصّصة تسمى تجمع الوزن الكروي Damsphere Weighted Ensemble. بدلاً من السماح لنموذج واحد بالهيمنة، تضبط التجميعة مقدار الثقة في كل طريقة اعتمادًا على أدائها، محافظةً على توازن تأثيراتهما على «كرة» رياضية من الوزن. إضافة إلى ذلك، يقوم إجراءان للبحث مستوحى من الطبيعة، مُحسّن بوما وخوارزمية الكِتْر الأسود‑الجناح، بالتناوب في استكشاف وتحسين العديد من المقاييس والتحكمات (الفرط‑معاملات) التي تضبط كيفية تعلم النماذج. يركّز أحدهما على استكشاف واسع للخيارات؛ بينما يركز الآخر على تحسين الدقة للحلول الواعدة. معًا، يبحثان عن إعدادات تُنتج تنبؤات دقيقة ومستقرة دون الإفراط في ملاءمة البيانات.
قراءة بصمة الدواء الجزيئية
بعد تدريب دقيق وفحص باستخدام التحقق المتقاطع بخمس طيات ومقاييس خطأ متعددة، تنبأ الإطار بإطلاق الدواء باتساق عالٍ جدًا مع التجارب (مفسرًا أكثر من 99% من التباين في البيانات). وبقدر أهمية ذلك، استقصى المؤلفون أي المدخلات كانت الأكثر تأثيرًا. ظهرت عوامل بسيطة مثل الزمن ونوع الوسط — ممثلةً موقع القرص المحتمل في الجسم — كأقوى محركات للإطلاق، بما يتوافق مع سلوك الانتشار والتآكل المعروف. كما برزت نطاقات رامان معينة مرتبطة بميزات محددة لطلاءات متعددات السكاريد، رابطًةً البنية الجزيئية بسرعة تسرب الدواء. أكدت الاختبارات الإحصائية أن هذه الأنماط لم تكن مجرّد صدفة في مجموعة البيانات بل عكست علاقات متسقة.
ماذا يعني هذا للأدوية المستقبلية
لغير المتخصص، الرسالة الرئيسية هي أن هذه المقاربة تعمل كمحاكي ذكي للأقراص المطلية: أدخِل بصمة الدواء الجزيئية وظروف الاختبار، فيتنبأ بكمية الدواء المطروحة عبر الزمن. وبينما لا تحل محل النماذج الفيزيائية التفصيلية أو التجارب السريرية، يمكنها فحص الطلاءات المرشحة بسرعة، وتقليل نطاق الوصفات الواعدة، وخفض عدد التجارب المخبرية المطلوبة. من خلال تقليل استهلاك المواد وتسريع التطوير، يدعم الإطار تصميم أدوية أكثر كفاءة وصدارة بيئية، ويقدّم نافذة أوضح لسبب إطلاق بعض الطلاءات للأدوية ببطء وبثبات بينما تفشل أخرى في ذلك.
الاستشهاد: Albariqi, A.H., Safhi, A.Y., Alqahtani, S.S. et al. Integrative ensemble learning framework for forecasting controlled drug release based on Raman spectral signatures. Sci Rep 16, 11343 (2026). https://doi.org/10.1038/s41598-026-41837-0
الكلمات المفتاحية: إطلاق دواء مسيطر, مطيافية رامان, تعلم الآلة, توصيل الدواء عن طريق الفم, طلاءات البوليمر