Clear Sky Science · pl
Integracyjny system uczenia zespołowego do prognozowania kontrolowanego uwalniania leku na podstawie sygnatur widm Ramanowskich
Dlaczego czas ma znaczenie dla tabletek
Wiele leków działa najlepiej, gdy rozpuszcza się stopniowo i dociera we właściwe miejsce w jelitach, na przykład do okrężnicy, zamiast uwalniać się jednorazowo w żołądku. Projektowanie takich „długodziałających” i „ukierunkowanych” tabletek jest trudne i zwykle wymaga wielu eksperymentów metodą prób i błędów. W tym badaniu pokazano, jak łączenie pomiarów optycznych powłok tabletek z zaawansowanymi modelami komputerowymi może przewidywać, jak lek będzie uwalniany w czasie, co potencjalnie skraca czas opracowywania, koszty i ilość odpadów.
Od powlekanych pigułek do inteligentnych prognoz
Naukowcy skupili się na tabletkach doustnych powlekanych polisacharydami pochodzenia roślinnego, stosowanymi do ochrony leku podczas przechodzenia przez przewód pokarmowy i opóźnienia jego uwolnienia do momentu dotarcia do okrężnicy. Przykładem testowym był powszechny lek przeciwzapalny, kwas 5‑aminosalicylowy, często stosowany w chorobach jelit. Zamiast polegać wyłącznie na konwencjonalnych testach rozpuszczania, użyli spektroskopii Ramana — techniki, która oświetla próbkę i odczytuje molekularny „odcisk palca” ze światła rozproszonego. Dla każdej z 155 formuł powłok zarejestrowali ponad 1 500 cech widmowych, zanotowali rodzaj polisacharydu i medium płynnego oraz zmierzyli, ile leku zostało uwolnione po 2, 8 i 24 godzinach w warunkach przypominających jelito.
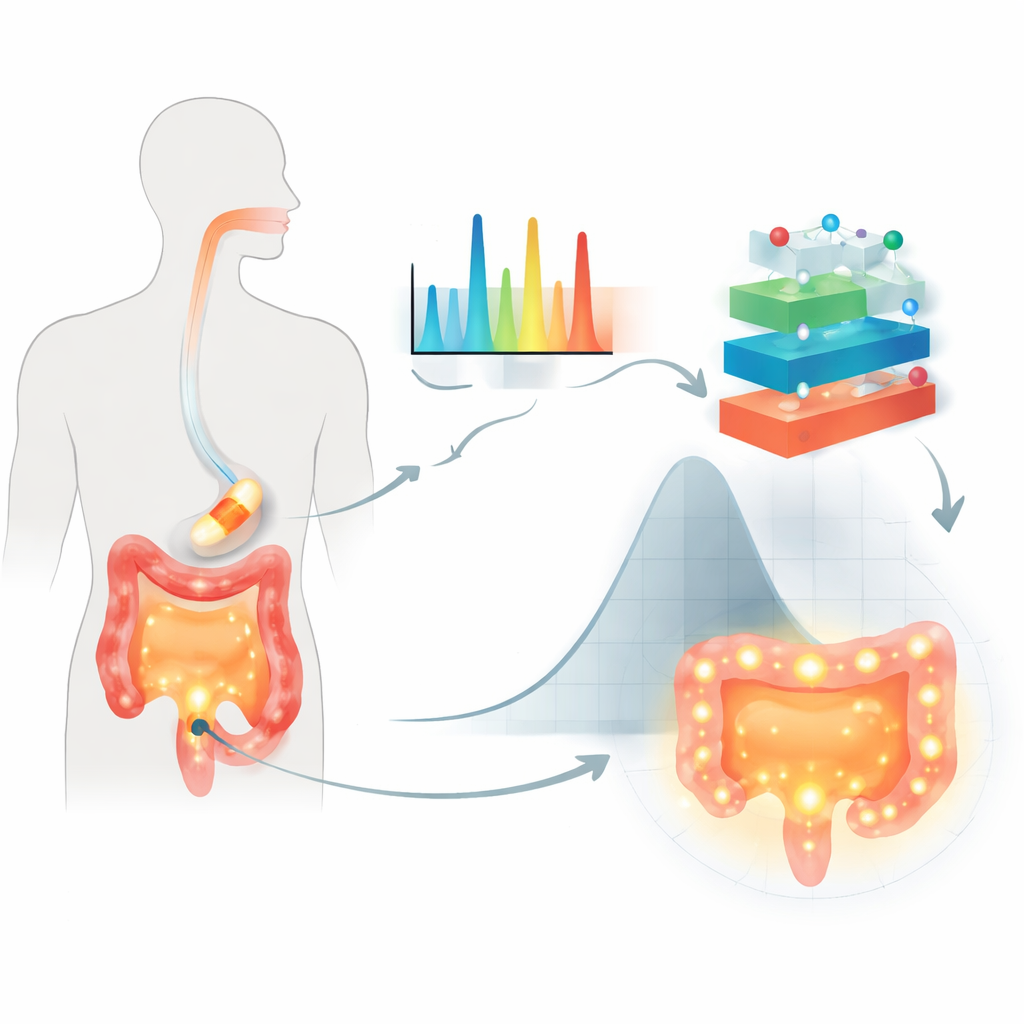
Dlaczego stare modele zawodzą
Tradycyjne równania opisujące uwalnianie leku zakładają proste struktury i gładką dyfuzję, co często nie odpowiada złożonej rzeczywistości nowoczesnych powłok i zmieniających się warunków w przewodzie pokarmowym. Mają też trudności z obsługą dużych, złożonych zestawów danych, takich jak tysiące cech Ramanowskich kodujących subtelne różnice w strukturze polimerów i interakcji lek–polimer. Starsze metody statystycznego projektowania potrafią uwzględniać wiele zmiennych, ale stają się nieporęczne, gdy naraz zmienia się wiele składników i warunków testowych. W efekcie ważne kombinacje mogą zostać pominięte, a modele mogą nie przewidywać wiarygodnie zachowania w różnych płynach imitujących żołądek i jelita.
Połączenie dwóch umysłów i dwóch strategii poszukiwań
Aby sprostać tej złożoności, zespół zbudował warstwowy system uczący łączący dwie metody uczenia maszynowego — XGBoost i AdaBoost — w specjalnym zespole zwanym Damsphere Weighted Ensemble. Zamiast dopuścić do dominacji jednego modelu, zespół dostosowuje poziom zaufania do każdej metody w oparciu o jej skuteczność, utrzymując ich wpływy w równowadze na pewnego rodzaju matematycznej „sferze”. Na to wszystko nałożone są dwie z natury inspirowane procedury poszukiwania, Puma Optimizer i Black‑Winged Kite Algorithm, które na przemian eksplorują i dopracowują liczne pokrętła i regulatory (hiperparametry) kontrolujące sposób uczenia modeli. Jeden z nich kładzie nacisk na szerokie przeszukiwanie możliwości; drugi skupia się na dopracowywaniu obiecujących rozwiązań. Razem poszukują ustawień generujących dokładne, stabilne prognozy bez nadmiernego dopasowania do danych.
Odczytanie molekularnego odcisku pigułki
Po starannym trenowaniu i weryfikacji przy użyciu walidacji krzyżowej pięciokrotnej oraz wielorakich miar błędu, system przewidywał uwalnianie leku z bardzo wysoką zgodnością z eksperymentami (wyjaśniając ponad 99% zmienności w danych). Równie istotne było zbadanie, które wejścia miały największe znaczenie. Proste czynniki, takie jak czas i rodzaj medium — obrazujące, gdzie pigułka może się znajdować w organizmie — okazały się najsilniejszymi czynnikami napędzającymi uwalnianie, zgodnie ze znanym zachowaniem dyfuzji i erozji. Pewne pasma Ramana powiązane z określonymi cechami powłok polisacharydowych również się wyróżniały, łącząc strukturę molekularną z szybkością, z jaką lek przenikał na zewnątrz. Testy statystyczne potwierdziły, że te wzorce nie były jedynie losowymi osobliwościami zestawu danych, lecz odzwierciedlały spójne zależności.
Co to oznacza dla przyszłych leków
Dla laika kluczowe przesłanie jest takie, że to podejście działa jak inteligentny symulator powlekanych tabletek: podaj molekularny odcisk pigułki i warunki testowe, a system przewidzi, ile leku zostanie uwolnione w czasie. Choć nie zastępuje szczegółowych modeli fizycznych ani badań klinicznych, może szybko przesiewać kandydatów na powłoki, zawężać obiecujące receptury i zmniejszać liczbę potrzebnych eksperymentów laboratoryjnych. Poprzez ograniczenie zużycia materiałów i przyspieszenie rozwoju, system wspiera bardziej ekologiczne i efektywne projektowanie leków oraz daje jaśniejszy wgląd w to, dlaczego niektóre powłoki uwalniają leki powoli i niezawodnie, a inne nie.
Cytowanie: Albariqi, A.H., Safhi, A.Y., Alqahtani, S.S. et al. Integrative ensemble learning framework for forecasting controlled drug release based on Raman spectral signatures. Sci Rep 16, 11343 (2026). https://doi.org/10.1038/s41598-026-41837-0
Słowa kluczowe: kontrolowane uwalnianie leku, spektroskopia Ramanowska, uczenie maszynowe, doustne podawanie leku, powłoki polimerowe