Clear Sky Science · pt
Estrutura integrativa de aprendizado em conjunto para prever liberação controlada de fármacos com base em assinaturas espectrais de Raman
Por que o tempo importa para comprimidos
Muitos medicamentos funcionam melhor quando se dissolvem lentamente e chegam ao local certo no intestino, como o cólon, em vez de liberarem tudo de uma vez no estômago. Projetar esses comprimidos “de longa ação” e “direcionados” é complicado e geralmente requer muitos experimentos de tentativa e erro em laboratório. Este estudo mostra como combinar medidas baseadas em luz dos revestimentos dos comprimidos com modelos computacionais avançados pode prever como um fármaco será liberado ao longo do tempo, potencialmente reduzindo o tempo de desenvolvimento, custo e desperdício.
De comprimidos revestidos a previsões inteligentes
Os pesquisadores focaram em comprimidos orais revestidos com açúcares de origem vegetal chamados polissacarídeos, usados para proteger um fármaco enquanto ele percorre o trato digestivo e para atrasar sua liberação até atingir o cólon. O caso teste foi um anti‑inflamatório comum, o ácido 5‑aminossalicílico, frequentemente usado no tratamento de doenças intestinais. Em vez de depender apenas de testes convencionais de dissolução, utilizaram espectroscopia Raman, uma técnica que ilumina a amostra e lê uma “impressão digital” molecular a partir da luz espalhada. Para cada uma das 155 formulações revestidas, capturaram mais de 1.500 características espectrais, registraram que tipo de polissacarídeo e meio líquido foram usados e mediram quanto fármaco havia sido liberado após 2, 8 e 24 horas em condições que imitam o intestino.
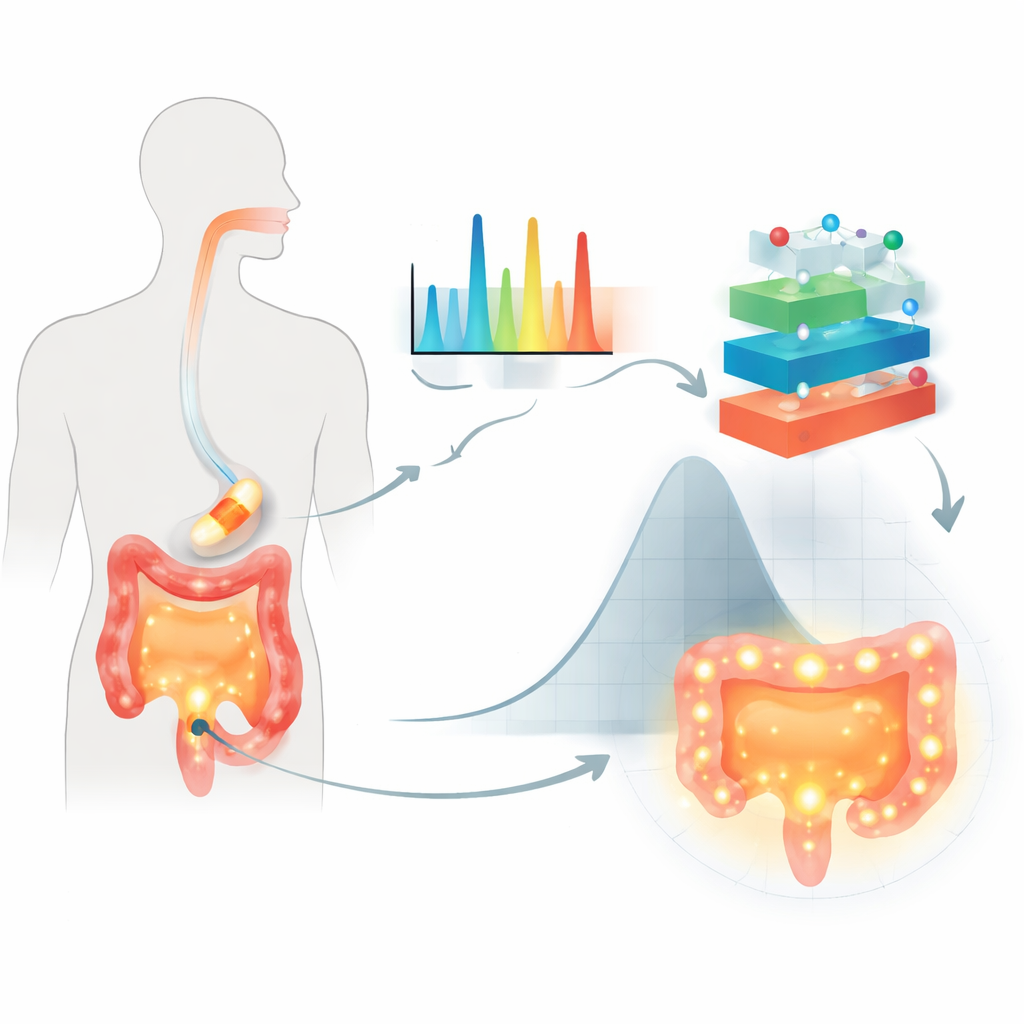
Por que modelos antigos não bastam
Equações tradicionais para liberação de fármacos assumem estruturas simples e difusão suave, o que muitas vezes não corresponde à realidade complexa dos revestimentos modernos e aos ambientes intestinais variáveis. Elas também têm dificuldade com conjuntos de dados grandes e complexos, como milhares de características Raman que codificam diferenças sutis na estrutura do polímero e na interação fármaco–polímero. Métodos estatísticos mais antigos conseguem lidar com múltiplas variáveis, mas ficam impraticáveis quando muitos ingredientes e condições de teste mudam ao mesmo tempo. O resultado é que combinações importantes podem ser perdidas e os modelos podem não prever de forma confiável o comportamento em diferentes fluidos que mimetizam estômago e intestinos.
Combinando duas mentes e duas estratégias de busca
Para enfrentar essa complexidade, a equipe construiu um sistema de aprendizado em camadas que combina dois métodos de aprendizado de máquina — XGBoost e AdaBoost — dentro de um ensemble especializado chamado Damsphere Weighted Ensemble. Em vez de deixar um único modelo dominar, o ensemble ajusta quanto confia em cada método com base em seu desempenho, mantendo suas influências equilibradas em uma espécie de “esfera” matemática. Sobre isso, dois procedimentos de busca inspirados na natureza, o Puma Optimizer e o Black‑Winged Kite Algorithm, se revezam explorando e refinando os inúmeros botões e ajustes (hiperparâmetros) que controlam como os modelos aprendem. Um enfatiza a exploração ampla de possibilidades; o outro foca no refinamento de soluções promissoras. Juntos, procuram configurações que produzam previsões precisas e estáveis sem overfitting dos dados.
Lendo a impressão digital molecular do comprimido
Após treinamento e verificação cuidadosos usando validação cruzada em cinco partes e múltiplas medidas de erro, a estrutura previu a liberação do fármaco com concordância muito alta em relação aos experimentos (explicando mais de 99% da variação dos dados). Igualmente importante, os autores investigaram quais entradas eram mais relevantes. Fatores simples, como o tempo e o tipo de meio — representando onde o comprimido pode estar no corpo — emergiram como os principais determinantes da liberação, em concordância com o comportamento conhecido de difusão e erosão. Certas bandas Raman, ligadas a características específicas dos revestimentos polissacarídicos, também se destacaram, conectando a estrutura molecular à velocidade com que o fármaco vazava. Testes estatísticos confirmaram que esses padrões não eram apenas casualidades do conjunto de dados, mas refletiam relações consistentes.
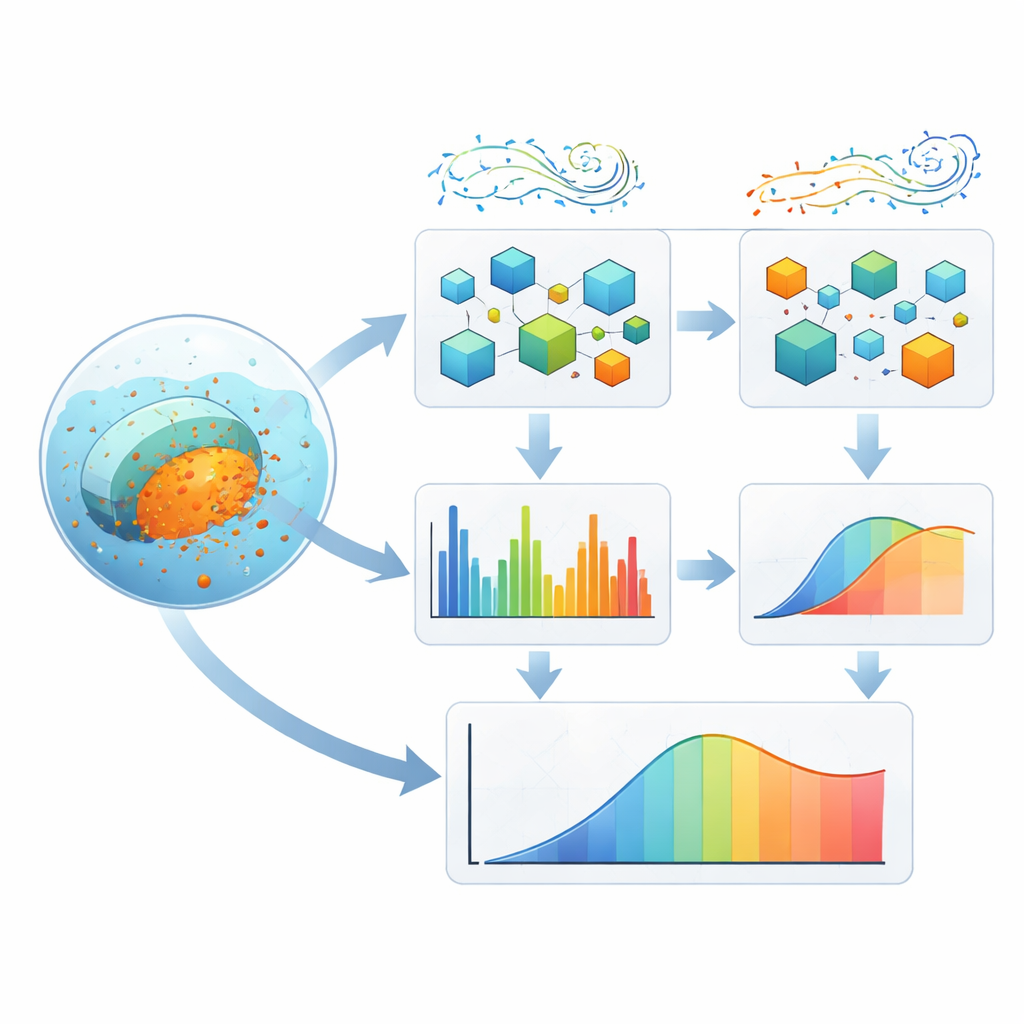
O que isso significa para medicamentos futuros
Para um não especialista, a mensagem principal é que essa abordagem funciona como um simulador inteligente para comprimidos revestidos: informe a impressão digital molecular do comprimido e as condições de teste, e ela prevê quanto fármaco será liberado ao longo do tempo. Embora não substitua modelos físicos detalhados ou ensaios clínicos, pode rapidamente triagem de revestimentos candidatos, estreitar receitas promissoras e reduzir o número de experimentos laboratoriais necessários. Ao cortar o uso de material e acelerar o desenvolvimento, a estrutura apoia um projeto de fármacos mais eficiente e sustentável e oferece uma visão mais clara do porquê alguns revestimentos liberam fármacos de forma lenta e confiável enquanto outros não.
Citação: Albariqi, A.H., Safhi, A.Y., Alqahtani, S.S. et al. Integrative ensemble learning framework for forecasting controlled drug release based on Raman spectral signatures. Sci Rep 16, 11343 (2026). https://doi.org/10.1038/s41598-026-41837-0
Palavras-chave: liberação controlada de fármacos, espectroscopia Raman, aprendizado de máquina, administração oral de medicamentos, revestimentos poliméricos