Clear Sky Science · nl
Integratief ensemble‑leerraamwerk voor het voorspellen van gecontroleerde medicijnafgifte op basis van Raman‑spectrale signaturen
Waarom timing belangrijk is voor pillen
Veel medicijnen werken het beste wanneer ze langzaam oplossen en op precies de juiste plek in het darmkanaal aankomen, bijvoorbeeld in de dikke darm, in plaats van alles tegelijk in de maag vrij te geven. Het ontwerpen van deze "langwerkende" en "gericht afleverende" tabletten is ingewikkeld en vereist meestal veel proef‑en‑foutexperimenten in het laboratorium. Deze studie laat zien hoe het combineren van lichtgebaseerde metingen van de coating van een tablet met geavanceerde computermodellen kan voorspellen hoe een medicijn in de tijd wordt afgegeven, waardoor ontwikkeltijd, kosten en afval mogelijk worden verminderd.
Van gecoate pillen naar slimme voorspellingen
De onderzoekers richtten zich op orale tabletten die zijn gecoat met plantaardige suikers, polysachariden genoemd, die worden gebruikt om een medicijn te beschermen tijdens zijn reis door het spijsverteringskanaal en om de afgifte uit te stellen totdat het de dikke darm bereikt. Hun testgeval was een veelgebruikt ontstekingsremmend middel, 5‑aminosalicylzuur, vaak toegepast bij darmziekten. In plaats van alleen te vertrouwen op conventionele dissolutieproeven gebruikten ze Raman‑spectroscopie, een techniek die licht op een monster schijnt en uit het verstrooide licht een moleculair "vingerafdruk" leest. Voor elk van de 155 gecoate formuleringen legden ze meer dan 1.500 spectrale kenmerken vast, noteerden welk type polysacharide en welk vloeibaar medium werd gebruikt en maten hoeveel medicijn er na 2, 8 en 24 uur onder darmachtige omstandigheden was vrijgekomen.
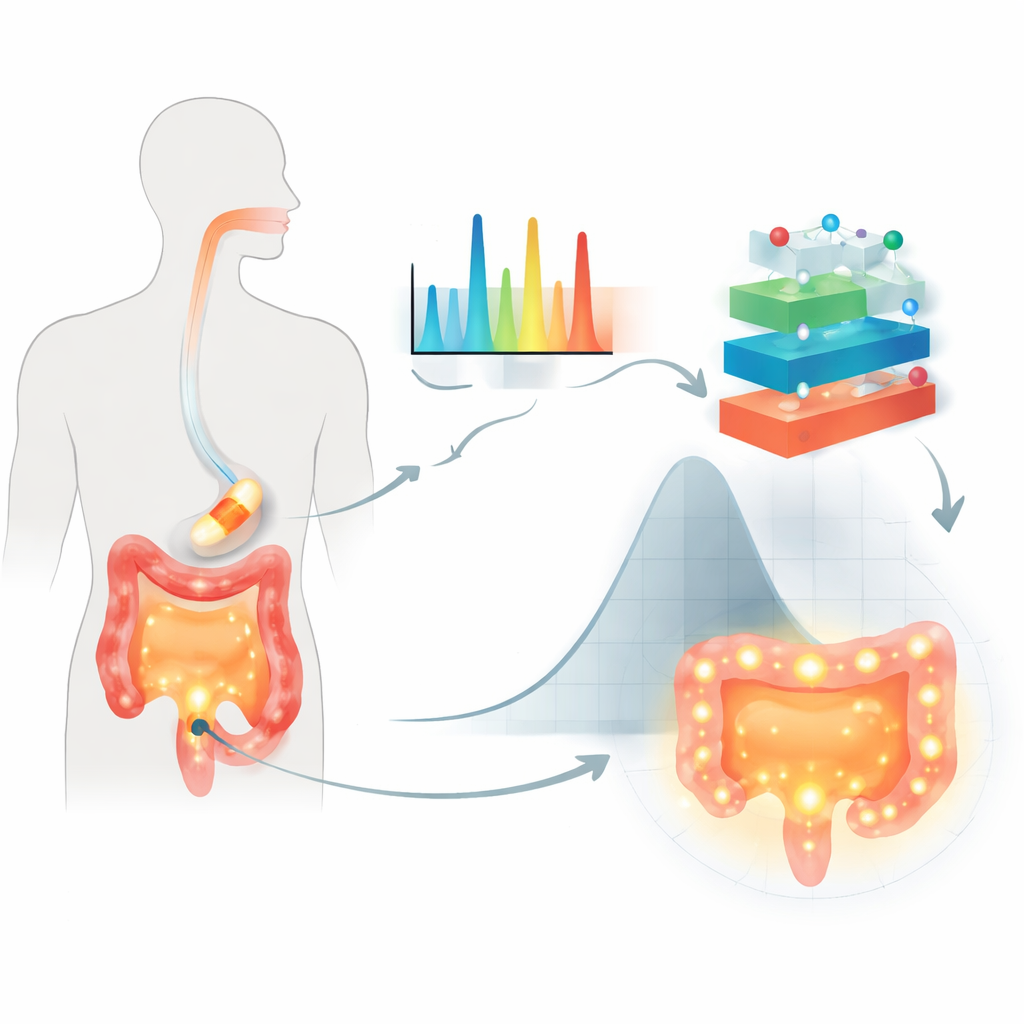
Waarom oude modellen tekortschieten
Traditionele vergelijkingen voor medicijnafgifte veronderstellen eenvoudige structuren en soepele diffusie, wat vaak niet overeenkomt met de verwarde realiteit van moderne coatings en veranderende darmomstandigheden. Ze hebben ook moeite met grote, complexe datasets, zoals duizenden Raman‑kenmerken die subtiele verschillen in polymeerstructuur en interactie tussen medicijn en polymeer coderen. Oudere statistische ontwerpmethoden kunnen met meerdere variabelen omgaan, maar worden onhandelbaar wanneer veel ingrediënten en testcondities tegelijk variëren. Het gevolg is dat belangrijke combinaties gemist kunnen worden en dat modellen mogelijk geen betrouwbare voorspellingen doen over gedrag in verschillende vloeistoffen die maag en darmen nabootsen.
Het samenbrengen van twee denkwijzen en twee zoekstrategieën
Om deze complexiteit aan te pakken bouwde het team een gelaagd leersysteem dat twee machine‑learningmethoden combineert—XGBoost en AdaBoost—binnen een gespecialiseerd ensemble genaamd Damsphere Weighted Ensemble. In plaats van één model de overhand te laten krijgen, past het ensemble aan hoeveel vertrouwen het in elke methode stelt op basis van hun prestaties, waardoor hun invloeden in balans blijven op een soort wiskundige "bol". Daarnaast nemen twee door de natuur geïnspireerde zoekprocedures, de Puma Optimizer en het Black‑Winged Kite Algorithm, beurtelings de taak op zich om de vele knoppen en instellingen (hyperparameters) die het leerproces bepalen te verkennen en te verfijnen. De een benadrukt brede verkenning van mogelijkheden; de ander richt zich op het fijn afstemmen van veelbelovende oplossingen. Gezamenlijk zoeken ze naar instellingen die nauwkeurige, stabiele voorspellingen opleveren zonder overfitting van de data.
Het lezen van de moleculaire vingerafdruk van de pil
Na zorgvuldige training en validatie met vijfvoudige cross‑validatie en meerdere foutmaten, voorspelde het raamwerk de medicijnafgifte met zeer hoge overeenstemming met experimenten (meer dan 99% van de variatie in de data verklaard). Net zo belangrijk onderzochten de auteurs welke invoeren het meest van belang waren. Eenvoudige factoren zoals tijd en het type medium—die aangeven waar de pil zich mogelijk in het lichaam bevindt—bleken de sterkste drijfveren van afgifte te zijn, in overeenstemming met bekend diffusi e‑ en erosiegedrag. Bepaalde Raman‑banden, gekoppeld aan specifieke kenmerken van de polysacharidecoatings, kwamen ook naar voren, waarmee moleculaire structuur werd verbonden met hoe snel het medicijn eruit sijpelde. Statistische tests bevestigden dat deze patronen geen willekeurige toevalligheden in de dataset waren, maar consistente verbanden weerspiegelen.
Wat dit betekent voor toekomstige medicijnen
Voor de niet‑specialist is de kernboodschap dat deze aanpak fungeert als een slimme simulator voor gecoate tabletten: voer de moleculaire vingerafdruk van de pil en de testomstandigheden in, en het voorspelt hoeveel medicijn er in de loop van de tijd zal vrijkomen. Hoewel het geen gedetailleerde fysieke modellen of klinische proeven vervangt, kan het snel kandidaat‑coatings screenen, veelbelovende recepten terugbrengen en het aantal benodigde laboratoriumexperimenten verminderen. Door materiaalgebruik te verkleinen en ontwikkeling te versnellen, ondersteunt het raamwerk een groenere, efficiëntere geneesmiddelontwerp en biedt het een helderder inzicht in waarom sommige coatings medicijnen langzaam en betrouwbaar vrijgeven terwijl andere dat niet doen.
Bronvermelding: Albariqi, A.H., Safhi, A.Y., Alqahtani, S.S. et al. Integrative ensemble learning framework for forecasting controlled drug release based on Raman spectral signatures. Sci Rep 16, 11343 (2026). https://doi.org/10.1038/s41598-026-41837-0
Trefwoorden: gecontroleerde medicijnafgifte, Raman‑spectroscopie, machine learning, orale geneesmiddelen toediening, polymeercoatings