Clear Sky Science · de
Integriertes Ensemble‑Lernframework zur Vorhersage kontrollierter Wirkstofffreisetzung anhand von Raman‑Spektralsignaturen
Warum der Zeitpunkt bei Pillen wichtig ist
Viele Medikamente wirken am besten, wenn sie sich langsam auflösen und genau an der richtigen Stelle im Darm, etwa im Kolon, freigesetzt werden, statt sich sofort im Magen zu entleeren. Solche „langwirksamen“ und „zielgerichteten“ Tabletten zu entwerfen ist anspruchsvoll und erfordert meist viele Versuchszyklen im Labor. Diese Studie zeigt, wie sich lichtbasierte Messungen von Tablettenbeschichtungen mit fortgeschrittenen Computermodellen kombinieren lassen, um vorherzusagen, wie ein Wirkstoff über die Zeit freigesetzt wird — und damit Entwicklungszeit, Kosten und Abfall reduziert werden könnten.
Von beschichteten Pillen zu intelligenten Vorhersagen
Die Forschenden konzentrierten sich auf orale Tabletten, die mit pflanzlichen Zuckern — sogenannten Polysacchariden — beschichtet sind. Diese schützen den Wirkstoff auf dem Weg durch den Verdauungstrakt und verzögern die Freisetzung bis zum Erreichen des Kolons. Als Fallbeispiel diente das häufig eingesetzte entzündungshemmende Mittel 5‑Aminosalicylsäure, das oft bei Darmerkrankungen verwendet wird. Statt sich nur auf herkömmliche Freisetzungstests zu stützen, nutzten sie die Raman‑Spektroskopie, ein Verfahren, das eine Probe mit Licht bestrahlt und aus dem gestreuten Licht ein molekulares „Fingerabdruck“-Spektrum liest. Für jede der 155 beschichteten Formulierungen erfassten sie mehr als 1.500 spektrale Merkmale, dokumentierten die verwendete Polysaccharidart und das Flüssigkeitsmedium und maßen den freigesetzten Wirkstoffanteil nach 2, 8 und 24 Stunden unter darmähnlichen Bedingungen.
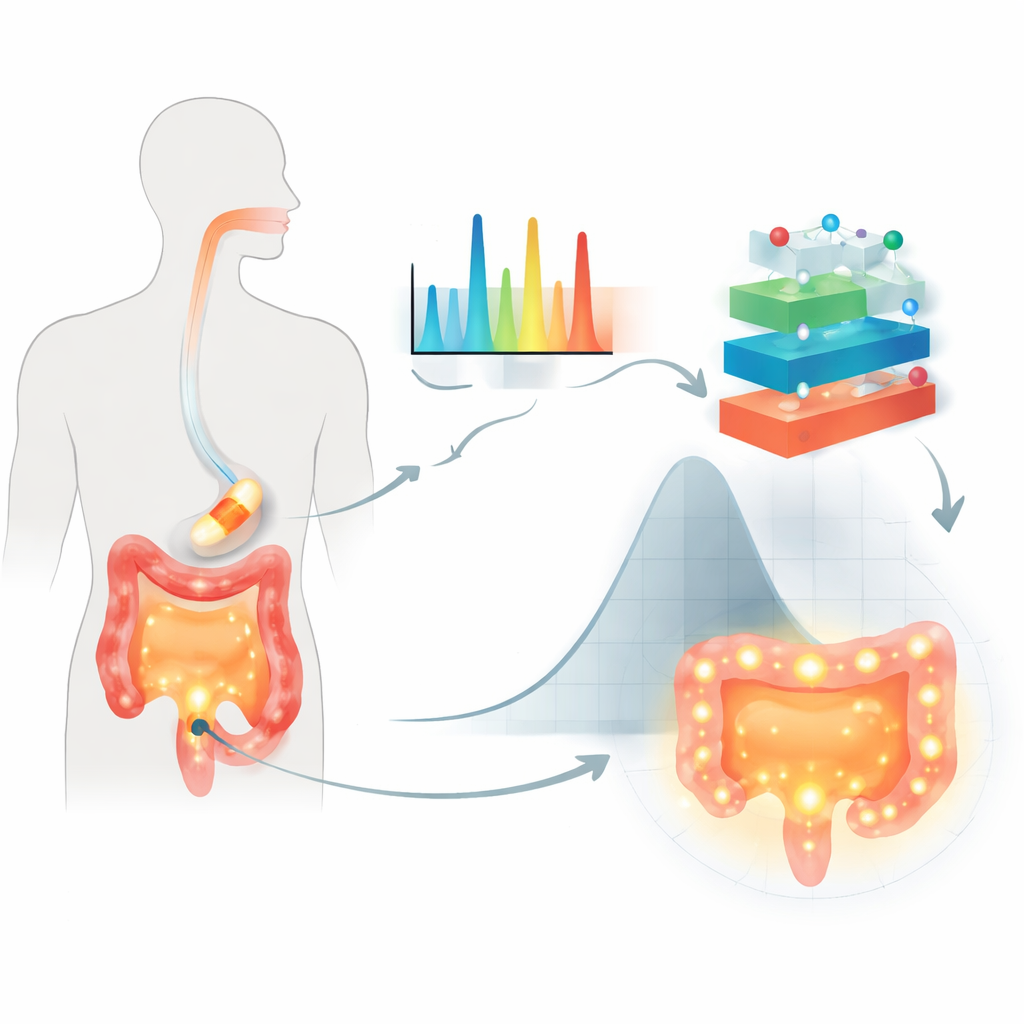
Warum klassische Modelle versagen
Traditionelle Gleichungen zur Wirkstofffreisetzung gehen von einfachen Strukturen und gleichmäßiger Diffusion aus, was häufig nicht der vernetzten Realität moderner Beschichtungen und sich verändernder Darmbedingungen entspricht. Sie tun sich zudem schwer mit großen, komplexen Datensätzen, etwa Tausenden von Raman‑Merkmalen, die feine Unterschiede in der Polymerstruktur und in Wechselwirkungen zwischen Wirkstoff und Polymer kodieren. Ältere statistische Designmethoden können zwar mehrere Variablen handhaben, werden aber unhandlich, wenn viele Zutaten und Testbedingungen gleichzeitig variieren. Dadurch können wichtige Kombinationen übersehen werden und Modelle versagen bei der zuverlässigen Vorhersage des Verhaltens in unterschiedlichen Magensaft‑ und Darm‑Simulationsmedien.
Zwei Methoden und zwei Suchstrategien vereinen
Um diese Komplexität anzugehen, bauten die Autoren ein geschichtetes Lernsystem, das zwei Methoden des maschinellen Lernens — XGBoost und AdaBoost — in einem spezialisierten Ensemble kombiniert, genannt Damsphere Weighted Ensemble. Anstatt ein Modell dominieren zu lassen, passt das Ensemble an, wie viel Vertrauen es jeder Methode entgegenbringt, abhängig von ihrer Performance, und hält deren Einflüsse auf einer Art mathematischer „Sphäre“ ausbalanciert. Darüber hinaus wechseln sich zwei von der Natur inspirierte Suchverfahren — der Puma Optimizer und der Black‑Winged Kite Algorithmus — beim Erkunden und Verfeinern der zahlreichen Stellschrauben (Hyperparameter) ab, die steuern, wie die Modelle lernen. Das eine Verfahren betont breite Exploration der Möglichkeiten; das andere fokussiert Feinabstimmung vielversprechender Lösungen. Gemeinsam suchen sie nach Einstellungen, die genaue, stabile Vorhersagen liefern, ohne die Daten zu überanpassen.
Den molekularen Fingerabdruck der Pille lesen
Nach sorgfältigem Training und Validierung mittels Fünffach‑Cross‑Validation und mehreren Fehlermaßen sagte das Framework die Wirkstofffreisetzung mit sehr hoher Übereinstimmung zu den Experimenten voraus (es erklärte über 99 % der Variation in den Daten). Ebenso wichtig: Die Autoren analysierten, welche Eingaben am wichtigsten waren. Einfache Faktoren wie die Zeit und die Art des Mediums — was den Ort im Körper repräsentiert — erwiesen sich als die stärksten Treiber der Freisetzung, im Einklang mit bekanntem Diffusions‑ und Erosionsverhalten. Bestimmte Raman‑Banden, die mit spezifischen Merkmalen der Polysaccharidbeschichtungen verknüpft sind, traten ebenfalls hervor und verbanden molekulare Struktur mit der Geschwindigkeit, mit der der Wirkstoff austrat. Statistische Tests bestätigten, dass diese Muster keine bloßen Zufälligkeiten des Datensatzes waren, sondern konsistente Zusammenhänge widerspiegeln.
Was das für künftige Medikamente bedeutet
Für Nicht‑Spezialisten ist die Kernbotschaft: Dieser Ansatz wirkt wie ein intelligenter Simulator für beschichtete Tabletten — man gibt den molekularen Fingerabdruck der Pille und die Testbedingungen ein, und er prognostiziert, wie viel Wirkstoff über die Zeit freigesetzt wird. Er ersetzt nicht detaillierte physikalische Modelle oder klinische Studien, kann aber Kandidatenbeschichtungen schnell sichten, vielversprechende Rezepturen eingrenzen und die Zahl benötigter Laborversuche reduzieren. Durch geringeren Materialverbrauch und schnellere Entwicklung unterstützt das Framework umweltfreundlichere, effizientere Medikamentenentwicklung und liefert zugleich klarere Einblicke, warum manche Beschichtungen Wirkstoffe langsam und zuverlässig freisetzen, während andere dies nicht tun.
Zitation: Albariqi, A.H., Safhi, A.Y., Alqahtani, S.S. et al. Integrative ensemble learning framework for forecasting controlled drug release based on Raman spectral signatures. Sci Rep 16, 11343 (2026). https://doi.org/10.1038/s41598-026-41837-0
Schlüsselwörter: kontrollierte Wirkstofffreisetzung, Raman‑Spektroskopie, maschinelles Lernen, orale Wirkstofffreisetzung, Polymerbeschichtungen