Clear Sky Science · it
Framework di apprendimento ensemble integrativo per la previsione del rilascio controllato di farmaci basato sulle firme spettrali Raman
Perché il tempo è importante per le pillole
Molti farmaci funzionano meglio quando si dissolvono lentamente e arrivano nel punto giusto dell’intestino, come il colon, invece di rilasciarsi tutti in una volta nello stomaco. Progettare queste pillole “a lunga durata” e “a rilascio mirato” è complesso e solitamente richiede numerosi esperimenti di laboratorio basati su tentativi ed errori. Questo studio mostra come la combinazione di misure ottiche dei rivestimenti delle compresse con modelli computazionali avanzati possa prevedere come un farmaco verrà rilasciato nel tempo, riducendo potenzialmente tempi di sviluppo, costi e rifiuti.
Dalle compresse rivestite a previsioni intelligenti
I ricercatori si sono concentrati su compresse orali rivestite con zuccheri di origine vegetale chiamati polisaccaridi, impiegati per proteggere il farmaco durante il transito nel tratto digestivo e ritardarne il rilascio fino al colon. Il caso di studio era un comune farmaco antinfiammatorio, l’acido 5-aminosalicilico, spesso usato per trattare le malattie intestinali. Invece di affidarsi solo ai test convenzionali di dissoluzione, hanno utilizzato la spettroscopia Raman, una tecnica che illumina un campione e legge un “impronta” molecolare dalla luce diffusa. Per ciascuna delle 155 formulazioni rivestite hanno acquisito oltre 1.500 caratteristiche spettrali, registrato il tipo di polisaccaride e il mezzo liquido impiegato, e misurato la quantità di farmaco rilasciata dopo 2, 8 e 24 ore in condizioni che simulano l’intestino.
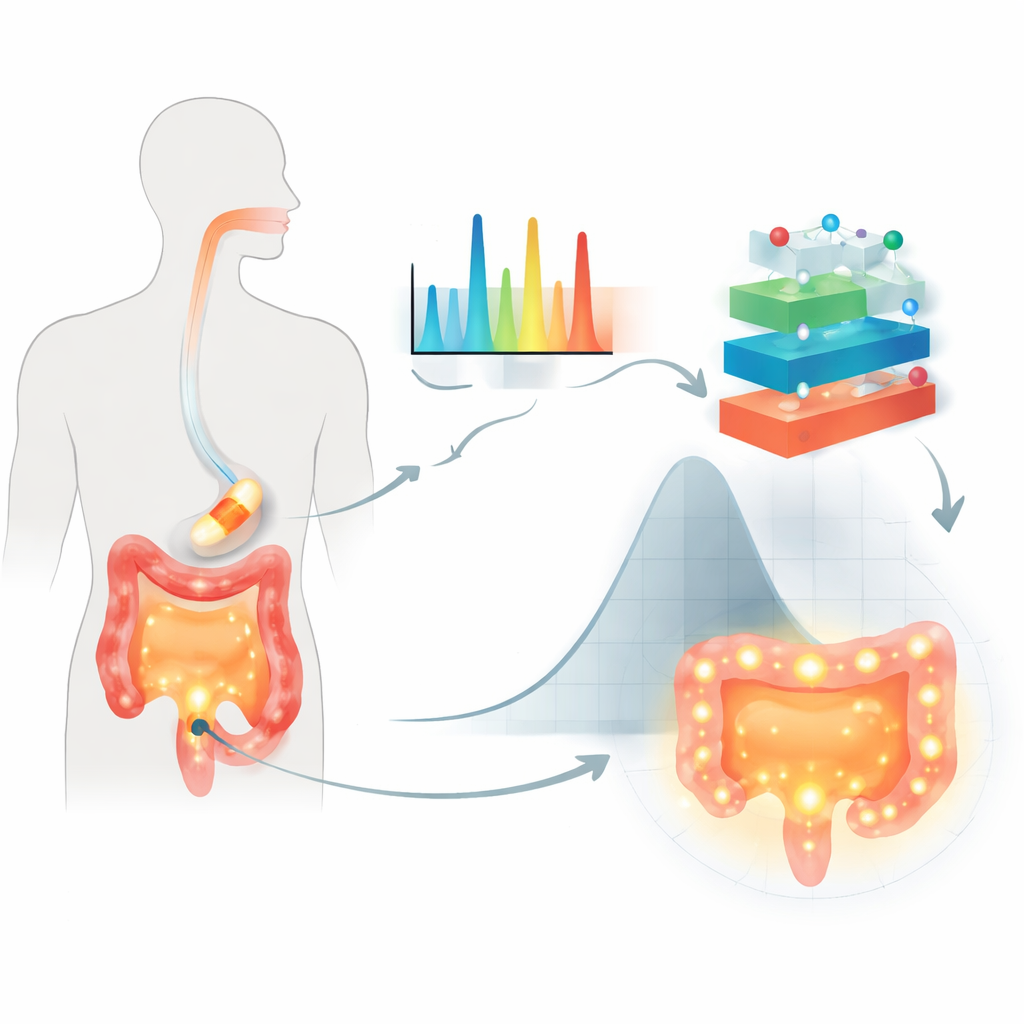
Perché i modelli tradizionali non sono sufficienti
Le equazioni tradizionali per il rilascio del farmaco assumono strutture semplici e diffusione regolare, che spesso non corrispondono alla realtà intrecciata dei rivestimenti moderni e ai cambiamenti dell’ambiente intestinale. Faticano inoltre a gestire dataset ampi e complessi, come migliaia di caratteristiche Raman che codificano sottili differenze nella struttura dei polimeri e nelle interazioni farmaco–polimero. I metodi statistici più datati possono trattare molte variabili, ma diventano ingombranti quando cambiano contemporaneamente numerosi ingredienti e condizioni di prova. Il risultato è che combinazioni importanti possono passare inosservate e i modelli possono non prevedere in modo affidabile il comportamento nei diversi fluidi che simulano stomaco e intestino.
Fondere due approcci e due strategie di ricerca
Per affrontare questa complessità, il team ha costruito un sistema di apprendimento stratificato che combina due metodi di machine learning—XGBoost e AdaBoost—all’interno di un ensemble specializzato chiamato Damsphere Weighted Ensemble. Piuttosto che lasciare che un solo modello domini, l’ensemble aggiusta quanto ogni metodo viene preso in considerazione in base alle prestazioni, mantenendo i loro contributi bilanciati su una sorta di “sfera” matematica. Sopra a questo, due procedure di ricerca ispirate alla natura, il Puma Optimizer e l’algoritmo Black‑Winged Kite, si alternano nell’esplorare e perfezionare i numerosi parametri (iperparametri) che controllano l’apprendimento dei modelli. Una privilegia un’esplorazione ampia delle possibilità; l’altra si concentra sull’affinamento delle soluzioni promettenti. Insieme cercano impostazioni che producano previsioni accurate e stabili senza sovradattare i dati.
Leggere l’impronta molecolare della compressa
Dopo un’attenta fase di addestramento e verifica usando validazione incrociata a cinque ripetizioni e diverse misure di errore, il framework ha previsto il rilascio del farmaco con un’ottima corrispondenza agli esperimenti (spiegando oltre il 99% della variazione nei dati). Altrettanto importante, gli autori hanno indagato quali input fossero più rilevanti. Fattori semplici come il tempo e il tipo di mezzo—che rappresentano la posizione della compressa nel corpo—sono emersi come i principali determinanti del rilascio, in linea con i noti comportamenti di diffusione ed erosione. Alcune bande Raman, associate a caratteristiche specifiche dei rivestimenti polisaccaridici, si sono inoltre distinte, collegando la struttura molecolare alla velocità con cui il farmaco filtrava fuori. Test statistici hanno confermato che questi schemi non erano semplici coincidenze del dataset, ma riflettevano relazioni coerenti.
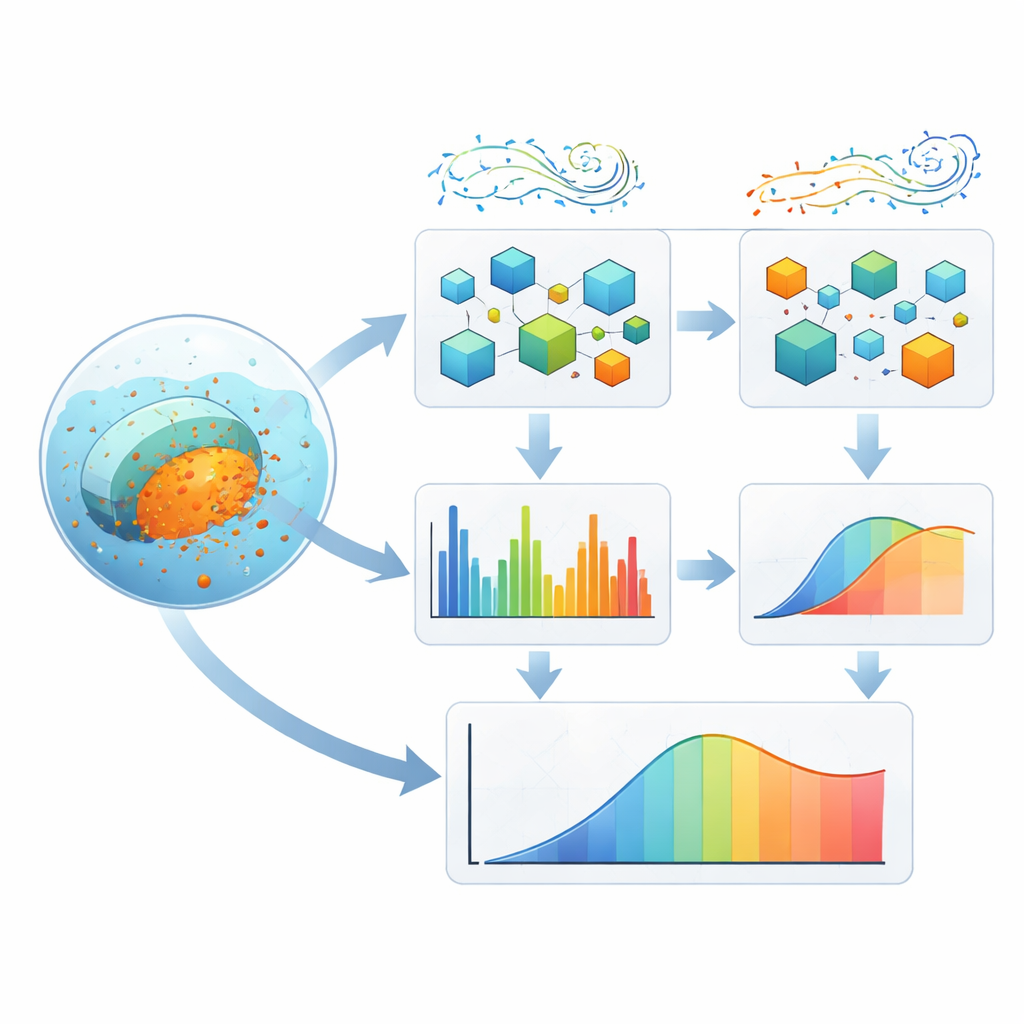
Cosa significa per i farmaci del futuro
Per un non specialista, il messaggio chiave è che questo approccio funziona come un simulatore intelligente per compresse rivestite: inserisci l’impronta molecolare della compressa e le condizioni di test, e prevede quanto farmaco verrà rilasciato nel tempo. Pur non sostituendo modelli fisici dettagliati o trial clinici, può rapidamente selezionare i rivestimenti candidati, restringere le ricette più promettenti e ridurre il numero di esperimenti di laboratorio necessari. Riducendo l’uso dei materiali e accelerando lo sviluppo, il framework favorisce una progettazione di farmaci più efficiente e sostenibile e offre una visione più chiara del perché alcuni rivestimenti rilasciano i farmaci in modo lento e affidabile mentre altri no.
Citazione: Albariqi, A.H., Safhi, A.Y., Alqahtani, S.S. et al. Integrative ensemble learning framework for forecasting controlled drug release based on Raman spectral signatures. Sci Rep 16, 11343 (2026). https://doi.org/10.1038/s41598-026-41837-0
Parole chiave: rilascio controllato di farmaci, spettroscopia Raman, apprendimento automatico, somministrazione orale di farmaci, rivestimenti polimerici