Clear Sky Science · sv
Pangenombaserad utformning av stam‑specifika primrar möjliggör exakt övervakning av bakterier i interventionstudier av mänskliga mikrobiomet
Varför det är viktigt att spåra hjälpsamma mikrober
Många av bakterierna vi hör talas om är stökiga, men några är tysta hjälpare som förvandlar mjölk till yoghurt, skyddar vår hud och kanske till och med dämpar inflammation i luftvägarna. Dessa ”goda bakterier” säljs som probiotika eller som striktare reglerade levande bioterapeutiska produkter, och de testas nu i mänskliga studier för hudproblem, allergier, mag‑tarmbesvär och mer. Ändå är en grundläggande fråga förvånansvärt svår att besvara: när vi ger människor en specifik bakteriestam, kan vi verkligen bevisa att just den stammen överlever och etablerar sig i kroppen, snarare än bara dess nära släktingar? Denna studie presenterar ett nytt sätt att spåra individuella bakteriestammar med hög precision, genom att utnyttja den växande mängden genomdata.
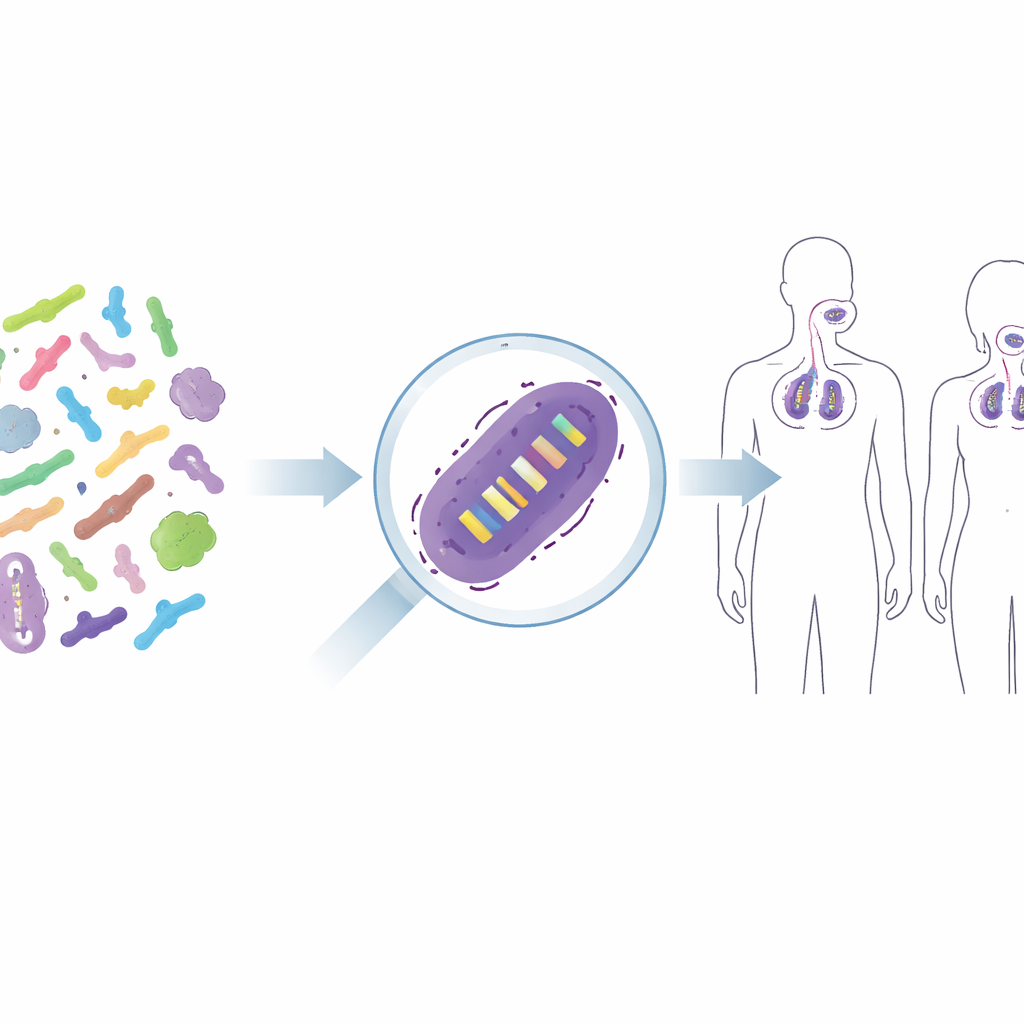
Från blandade mikrober till individuella stammar
Probiotiska produkter innehåller sällan bara ”bakterier” i allmänna termer; de innehåller noggrant utvalda stammar, som en särskild version av Lacticaseibacillus rhamnosus GG eller Lactiplantibacillus plantarum WCFS1. Dessa nära besläktade stammar kan skilja sig åt i hur de interagerar med vårt immunsystem eller hur väl de fäster vid hud‑ eller slemhinnevävnad, så forskare och tillsynsmyndigheter vill veta exakt vilken stam som finns kvar efter behandling. Traditionella metoder, som att odla bakterier på selektiva medier, berättar bara om breda grupper — till exempel totala mjölksyrabakterier — och misslyckas ofta när hjälpsamma stammar är i minoritet. Mer högteknologiska lösningar, som att tagga stammar med fluorescerande markörer eller DNA‑barcodes, skulle göra dem till genetiskt modifierade organismer, vilket ofta inte är acceptabelt för livsmedel eller mänskliga terapier. Utmaningen är att skilja nästan identiska stammar utan att förändra dem.
Bryta pangenomet för unika genetiska fingeravtryck
Författarna vände sig till begreppet ”pangenom”, hela uppsättningen gener som finns över många genom av samma art. Vissa gener delas av alla medlemmar (kärnan), medan andra bara finns i vissa stammar (den accessoriska delen). Genom att jämföra hundratals genom för flera arter av mjölksyrabakterier och en vanlig munbakterie sökte de efter gener som bara förekommer i en enda stam och inte i någon annan känd släkting. Dessa sällsynta gener fungerar som genetiska fingeravtryck. Teamet byggde en bioinformatisk pipeline som automatiskt sätter ihop pangenomet, tar bort nästan identiska dubblettgenom och flaggar stam‑unika gener. De dubbelkontrollerade sedan dessa kandidater mot bredare genomdatabaser för att försäkra sig om att liknande sekvenser inte dolde sig i andra arter.
Utformning av precisa molekylära ”streckkodsläsare”
När stam‑unika gener identifierats var nästa steg att bygga mycket specifika molekylära tester kring dem. Forskarna designade korta DNA‑stycken, kallade primrar, som binder endast till dessa unika gener. I en teknik känd som kvantitativ PCR (qPCR) fungerar dessa primrar som streckkodsläsare, som kopierar och upptäcker endast DNA från målstammen. Teamet skapade och optimerade primrar för sex stammar som spänner över olika arter, inklusive välanvända probiotika och nya kandidater isolerade från människokroppen. I laboratoriet testade de varje primerset inte bara på sin avsedda stam utan också på flera nära besläktade stammar från samma art. Tester visade stark amplifikation endast för målstammen, med minimal signal från de andra, vilket bekräftade att de valda genetiska fingeravtrycken verkligen var distinkta.
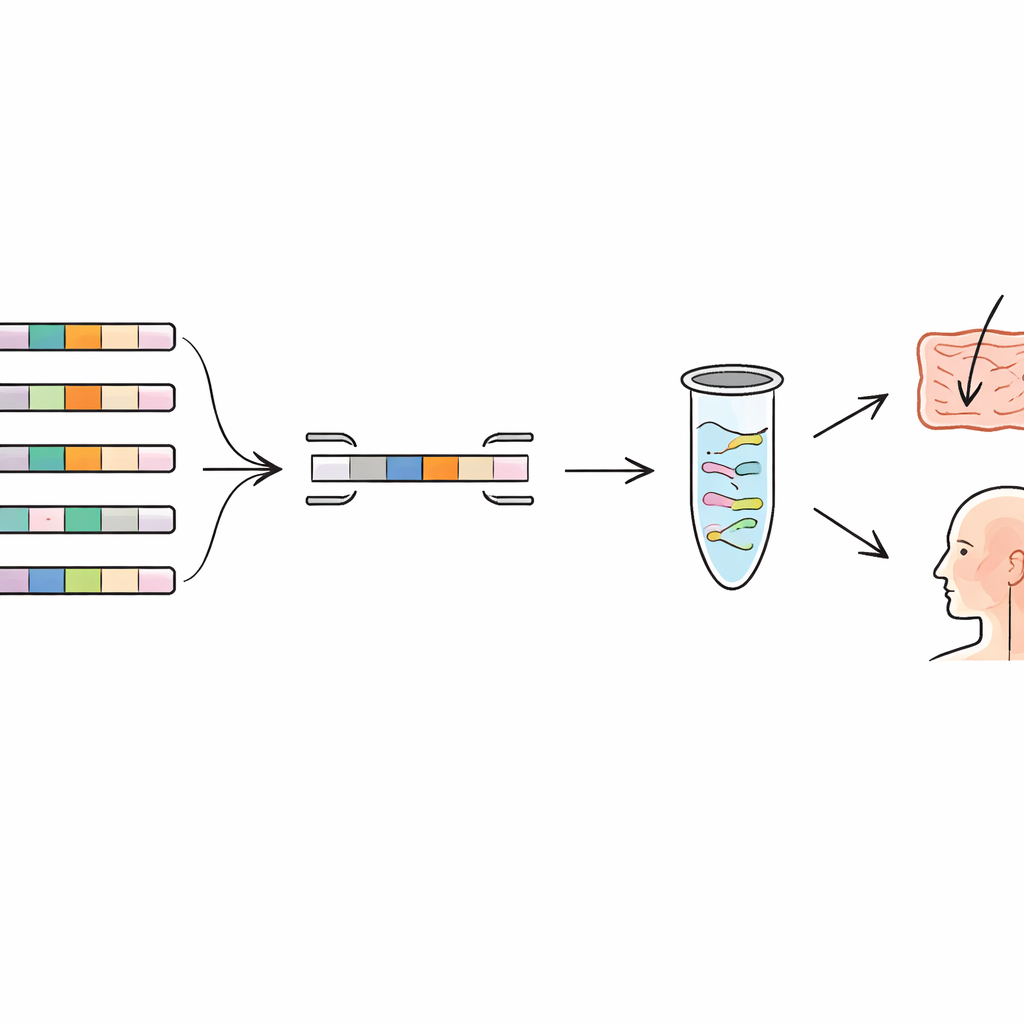
Följa probiotika på hud och i luftvägarna
För att se om denna metod fungerar hos riktiga människor applicerade författarna sina primrar på prover från tre placebokontrollerade humaninterventionsstudier. I en studie använde försökspersoner en ansiktskräm som innehöll två probiotikastammar; i andra fick deltagare en probiotikaspray för halsen eller en tuggbartablett. Med de nya qPCR‑testen kunde forskarna på ett tillförlitligt sätt detektera de tillsatta stammarna på huden och i övre luftvägarna hos behandlade deltagare, medan de nästan aldrig sågs i placebogrupperna. De observerade också hur signalen steg under användning och avklingade efter att behandlingen stoppats, vilket gav en tydlig bild av temporär kolonisation. I några fall uppträdde svagsignaler i kontrollerna, vilket påminde forskarna om att beakta naturlig bakgrundsbakterieflora och risken för mycket liten kontaminering, särskilt i kroppsytor med lågt bakterieantal.
Vad detta betyder för framtida mikrobiom‑terapier
I vardagstermer visar detta arbete hur man bygger en mycket skarp ”stamradar” utan att genetiskt förändra bakterierna själva. Genom att utnyttja subtila genetiska skillnader som avslöjas av storskaliga genomjämförelser kan forskare utforma qPCR‑tester som plockar ut en probiotikastam ur en mängd nära liknande. Detta gör det mycket enklare att besvara praktiska frågor: överlevde stammen produktens hållbarhet? Nådde den den avsedda kroppsplatsen? Hur länge stannade den och i vilka mängder? Eftersom metoden är transparent, billig och anpassningsbar till andra arter kan den bli ett standardverktyg för att utforma och testa nästa generationens probiotika och levande bioterapeutika, vilket tillför mer stringens och säkerhet till det snabbt växande fältet för mikrobiombaserade interventioner.
Citering: Eilers, T., Delanghe, L., De Boeck, I. et al. Pangenome-based design of strain-specific primers enables precise monitoring of bacteria in human microbiome intervention trials. Sci Rep 16, 11274 (2026). https://doi.org/10.1038/s41598-026-41449-8
Nyckelord: probiotika, mikrobiom, stamspårning, qPCR, pangenomanalys