Clear Sky Science · es
Diseño basado en el pangenoma de cebadores específicos de cepa que permite un seguimiento preciso de bacterias en ensayos de intervención del microbioma humano
Por qué importa rastrear microbios beneficiosos
Muchas de las bacterias de las que oímos hablar son problemáticas, pero algunas son aliadas discretas que convierten la leche en yogur, protegen nuestra piel e incluso pueden calmar la inflamación en las vías respiratorias. Estas “bacterias buenas” se comercializan como probióticos o como productos bioterapéuticos vivos más estrictamente regulados, y ahora se prueban en ensayos humanos para problemas de piel, alergias, trastornos digestivos y más. Sin embargo, una pregunta básica resulta sorprendentemente difícil de responder: cuando administramos a una persona una cepa bacteriana concreta, ¿podemos demostrar realmente que esa cepa exacta sobrevive y se establece en el organismo, y no solo sus parientes cercanos? Este estudio presenta una nueva forma de rastrear cepas bacterianas individuales con alta precisión, aprovechando la creciente cantidad de datos genómicos.
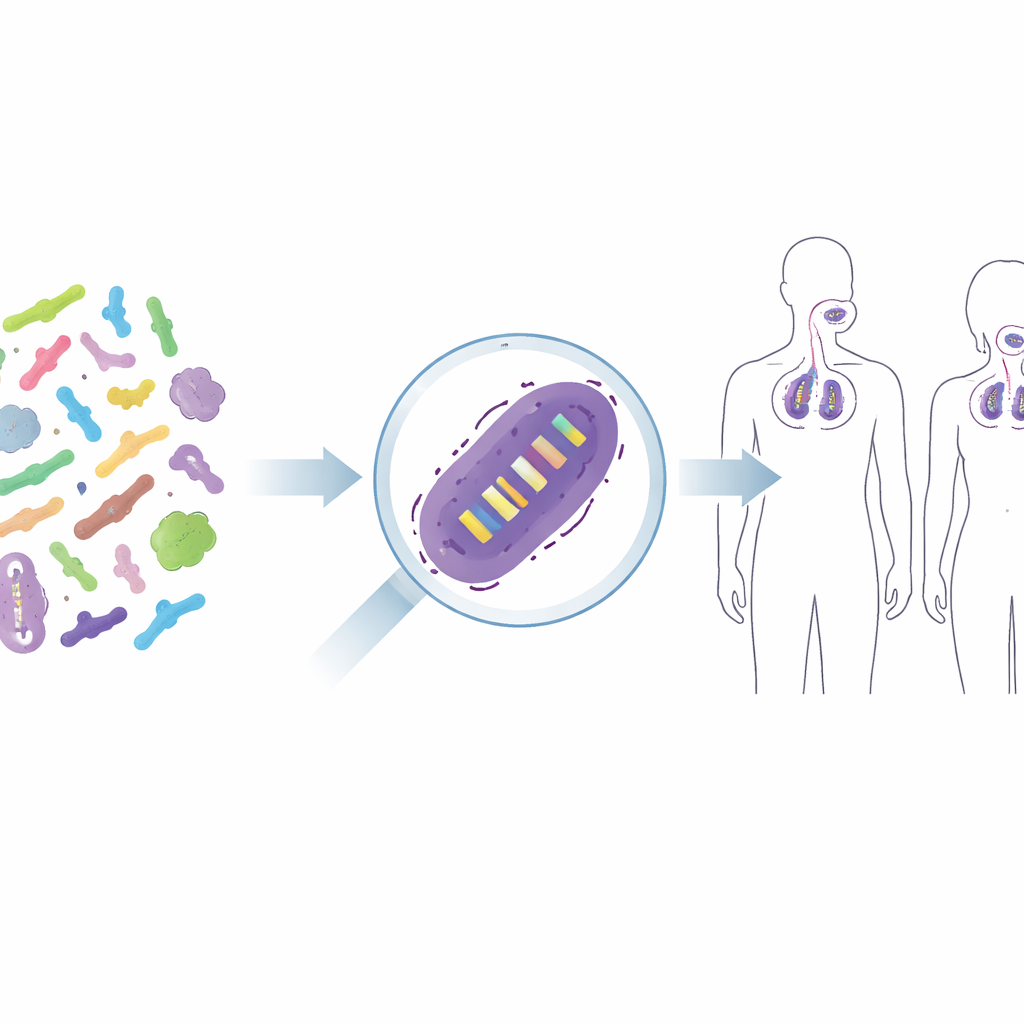
De microbios mixtos a cepas individuales
Los productos probióticos rara vez contienen simplemente “bacterias” en abstracto; contienen cepas escogidas cuidadosamente, como una versión particular de Lacticaseibacillus rhamnosus GG o Lactiplantibacillus plantarum WCFS1. Estas cepas estrechamente relacionadas pueden diferir en cómo interactúan con nuestro sistema inmune o en su capacidad para adherirse a la piel o a la garganta, por lo que investigadores y reguladores quieren saber exactamente qué cepa está presente tras el tratamiento. Los métodos tradicionales, como el cultivo en medios selectivos, solo informan sobre grupos amplios—por ejemplo, el total de bacterias lácticas—y a menudo fallan cuando las cepas beneficiosas están en inferioridad frente a otras. Soluciones más tecnológicas, como marcar cepas con marcadores fluorescentes o códigos de barras de ADN, convertirían a las cepas en organismos genéticamente modificados, algo que con frecuencia no es aceptable para alimentos o terapias humanas. El reto es distinguir cepas casi idénticas sin alterarlas.
Explorar el pangenoma en busca de huellas genéticas únicas
Los autores recurrieron al concepto de “pangenoma”, la colección completa de genes encontrada a lo largo de muchos genomas de la misma especie. Algunos genes son compartidos por todos los miembros (el núcleo), mientras que otros están presentes solo en ciertas cepas (la parte accesoria). Comparando cientos de genomas de varias especies de bacterias lácticas y de una bacteria común de la boca, buscaron genes que aparecieran únicamente en una cepa y no en ningún otro pariente conocido. Estos genes raros actúan como huellas genéticas. El equipo construyó una canalización bioinformática que ensambla automáticamente el pangenoma, elimina genomas prácticamente idénticos duplicados y marca genes únicos de cada cepa. Después cotejaron estos candidatos contra bases de datos genómicas más amplias para asegurarse de que no hubiera secuencias similares ocultas en otras especies.
Diseñar “lectores de códigos de barras” moleculares precisos
Una vez identificados los genes únicos de cada cepa, el siguiente paso fue construir pruebas moleculares altamente específicas en torno a ellos. Los investigadores diseñaron fragmentos cortos de ADN, llamados cebadores, que se unen solo a esos genes únicos. En una técnica conocida como reacción en cadena de la polimerasa cuantitativa (qPCR), estos cebadores actúan como lectores de códigos de barras, copiando y detectando únicamente el ADN de la cepa objetivo. El equipo creó y optimizó cebadores para seis cepas de distintas especies, incluidas probióticos de uso extendido y nuevos candidatos aislados del cuerpo humano. En el laboratorio, probaron cada conjunto de cebadores no solo en la cepa prevista sino también en varias cepas estrechamente relacionadas de la misma especie. Las pruebas mostraron amplificación fuerte únicamente para la cepa objetivo, con señal mínima en las otras, confirmando que las huellas genéticas elegidas eran realmente distintivas.
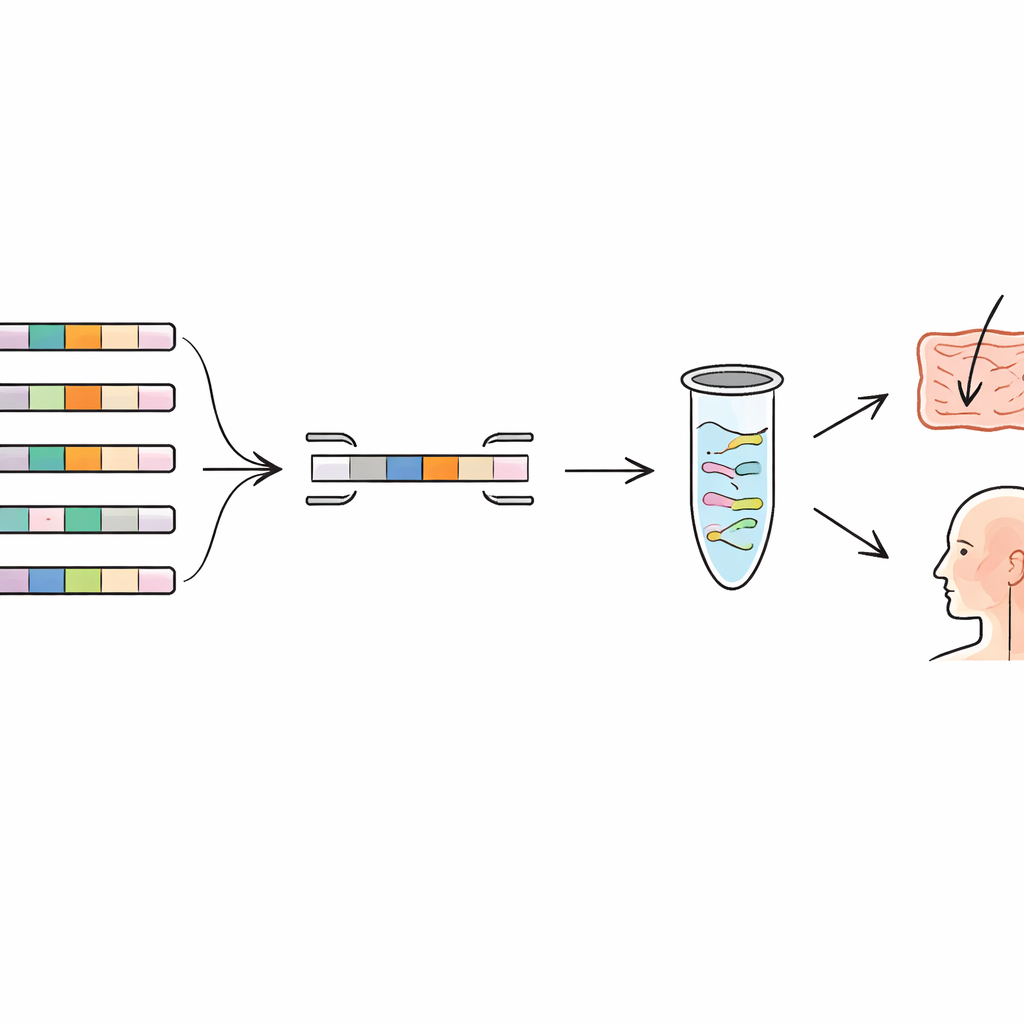
Rastreando probióticos en la piel y en las vías respiratorias
Para comprobar si este enfoque funciona en personas reales, los autores aplicaron sus cebadores a muestras de tres ensayos humanos aleatorizados con placebo. En un estudio, voluntarios usaron una crema facial que contenía dos cepas probióticas; en otros, las personas recibieron un spray faríngeo probiótico o una tableta masticable. Usando las nuevas pruebas por qPCR, los científicos pudieron detectar de forma fiable las cepas añadidas en la piel y en la parte superior del aparato respiratorio de los participantes tratados, mientras que casi nunca las encontraron en los grupos con placebo. También observaron cómo la señal aumentaba durante el uso y disminuía tras finalizar el tratamiento, ofreciendo una imagen clara de la colonización temporal. En algunos casos aparecieron señales de bajo nivel en los controles, lo que recuerda a los investigadores que consideren la presencia natural de bacterias de fondo y el riesgo de contaminación muy leve, especialmente en sitios del cuerpo con pocos microbios.
Qué significa esto para futuras terapias del microbioma
En términos cotidianos, este trabajo muestra cómo construir un “radar de cepas” muy preciso sin manipular genéticamente las bacterias. Al explotar diferencias genéticas sutiles reveladas por comparaciones genómicas a gran escala, los científicos pueden diseñar pruebas por qPCR que distingan una cepa probiótica entre una multitud de casi gemelas. Esto facilita responder preguntas prácticas: ¿sobrevivió la cepa durante la vida útil del producto? ¿llegó al sitio corporal objetivo? ¿Cuánto tiempo permaneció y en qué niveles? Dado que el método es transparente, económico y adaptable a otras especies, puede convertirse en una herramienta estándar para diseñar y evaluar la próxima generación de probióticos y bioterapéuticos vivos, aportando más rigor y seguridad al campo en rápido crecimiento de las intervenciones basadas en el microbioma.
Cita: Eilers, T., Delanghe, L., De Boeck, I. et al. Pangenome-based design of strain-specific primers enables precise monitoring of bacteria in human microbiome intervention trials. Sci Rep 16, 11274 (2026). https://doi.org/10.1038/s41598-026-41449-8
Palabras clave: probióticos, microbioma, seguimiento de cepas, qPCR, análisis de pangenoma