Clear Sky Science · fr
Conception de démarreurs spécifiques à la souche basée sur le pangenome permettant une surveillance précise des bactéries dans des essais d’intervention sur le microbiome humain
Pourquoi il est important de suivre les microbes utiles
Beaucoup des bactéries dont on entend parler sont des fauteurs de troubles, mais certaines sont des alliées discrètes qui transforment le lait en yaourt, protègent notre peau et peuvent même atténuer l’inflammation des voies respiratoires. Ces « bonnes bactéries » sont vendues comme probiotiques ou comme produits biothérapeutiques vivants soumis à une réglementation plus stricte, et elles sont désormais testées dans des essais humains pour des problèmes de peau, des allergies, des troubles digestifs, et plus encore. Pourtant, une question fondamentale est étonnamment difficile à trancher : lorsque l’on administre à une personne une souche bactérienne précise, peut‑on réellement prouver que cette souche exacte survit et s’implante dans l’organisme, plutôt que ses proches parentes ? Cette étude présente une nouvelle méthode pour suivre des souches bactériennes individuelles avec une grande précision, en tirant parti de l’abondance croissante des données génomiques.
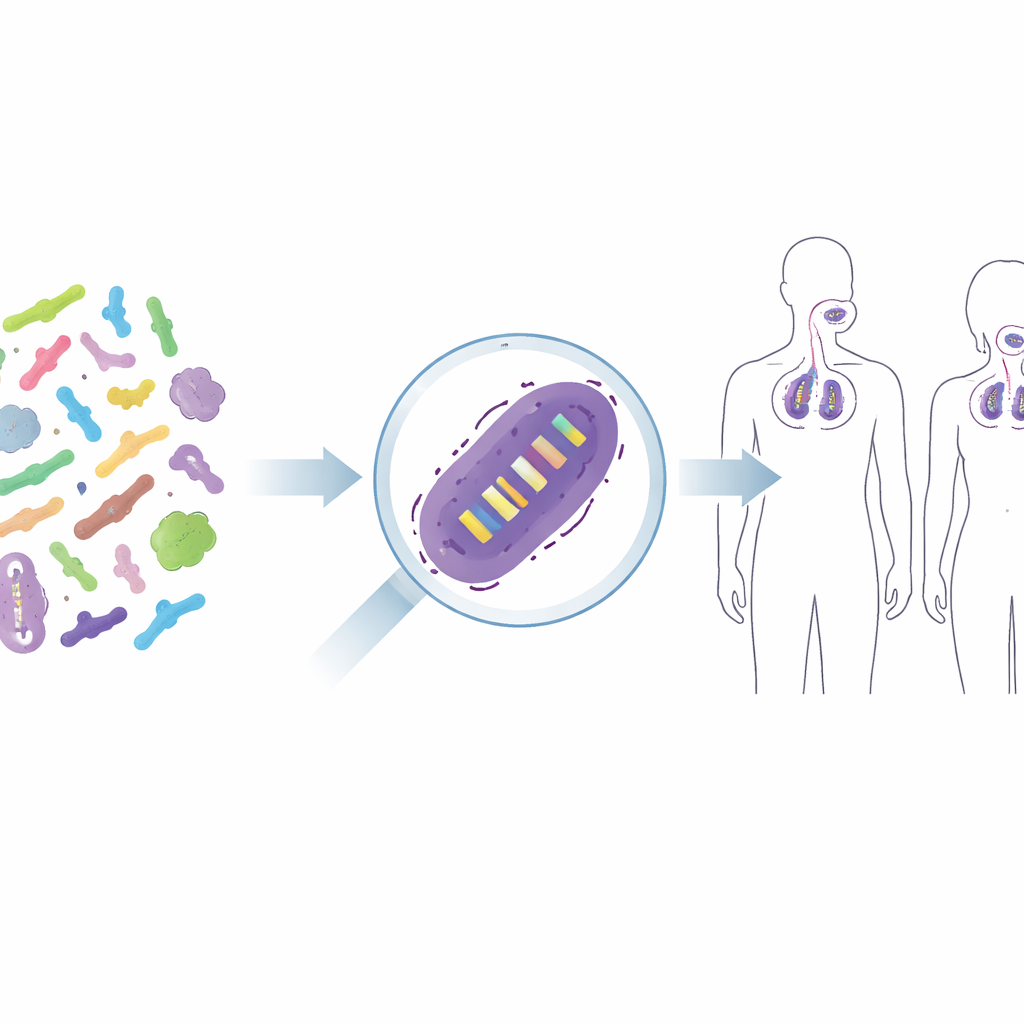
Des microbes mélangés aux souches individuelles
Les produits probiotiques ne contiennent que rarement des « bactéries » au sens vague ; ils renferment des souches soigneusement sélectionnées, comme une version particulière de Lacticaseibacillus rhamnosus GG ou de Lactiplantibacillus plantarum WCFS1. Ces souches étroitement apparentées peuvent différer quant à leur interaction avec notre système immunitaire ou leur capacité d’adhérence aux tissus cutanés ou pharyngés, aussi les chercheurs et les régulateurs veulent savoir exactement quelle souche est présente après le traitement. Les méthodes traditionnelles, comme la culture sur milieux sélectifs, n’indiquent que des groupes larges — par exemple le total des bactéries lactiques — et échouent souvent lorsque des souches utiles sont en faible nombre au regard d’autres. Des solutions plus high‑tech, comme le marquage des souches par fluorescence ou par codes-barres ADN, les transformeraient en organismes génétiquement modifiés, ce qui n’est souvent pas acceptable pour les aliments ou les thérapies humaines. Le défi consiste à distinguer des souches presque identiques sans les modifier.
Exploiter le pangenome pour trouver des empreintes génétiques uniques
Les auteurs se sont tournés vers le concept de « pangenome », l’ensemble complet des gènes retrouvés à travers de nombreux génomes d’une même espèce. Certains gènes sont partagés par tous les membres (le cœur), tandis que d’autres ne sont présents que dans certaines souches (la fraction accessoire). En comparant des centaines de génomes de plusieurs espèces de bactéries lactiques et d’une bactérie buccale commune, ils ont recherché des gènes présents uniquement dans une souche et absents chez tout autre parent connu. Ces gènes rares jouent le rôle d’empreintes génétiques. L’équipe a construit un pipeline bioinformatique qui assemble automatiquement le pangenome, élimine les génomes quasiment identiques en doublons et signale les gènes uniques à une souche. Ils ont ensuite vérifié ces candidats contre des bases de données génomiques plus large pour s’assurer que des séquences similaires ne se cachaient pas chez d’autres espèces.
Concevoir des « lecteurs de codes‑barres » moléculaires précis
Une fois les gènes uniques à la souche identifiés, l’étape suivante consistait à élaborer des tests moléculaires hautement spécifiques autour d’eux. Les chercheurs ont conçu de courts fragments d’ADN, appelés amorces, qui se lient uniquement à ces gènes uniques. Dans une technique connue sous le nom de PCR quantitative (qPCR), ces amorces fonctionnent comme des lecteurs de codes‑barres, copiant et détectant uniquement l’ADN de la souche cible. L’équipe a créé et optimisé des jeux d’amorces pour six souches couvrant différentes espèces, incluant des probiotiques largement utilisés et de nouveaux candidats isolés du corps humain. En laboratoire, ils ont testé chaque jeu d’amorces non seulement sur la souche visée mais aussi sur plusieurs souches étroitement apparentées de la même espèce. Les tests ont montré une amplification forte uniquement pour la souche cible, avec un signal minimal pour les autres, confirmant que les empreintes génétiques choisies étaient véritablement distinctives.
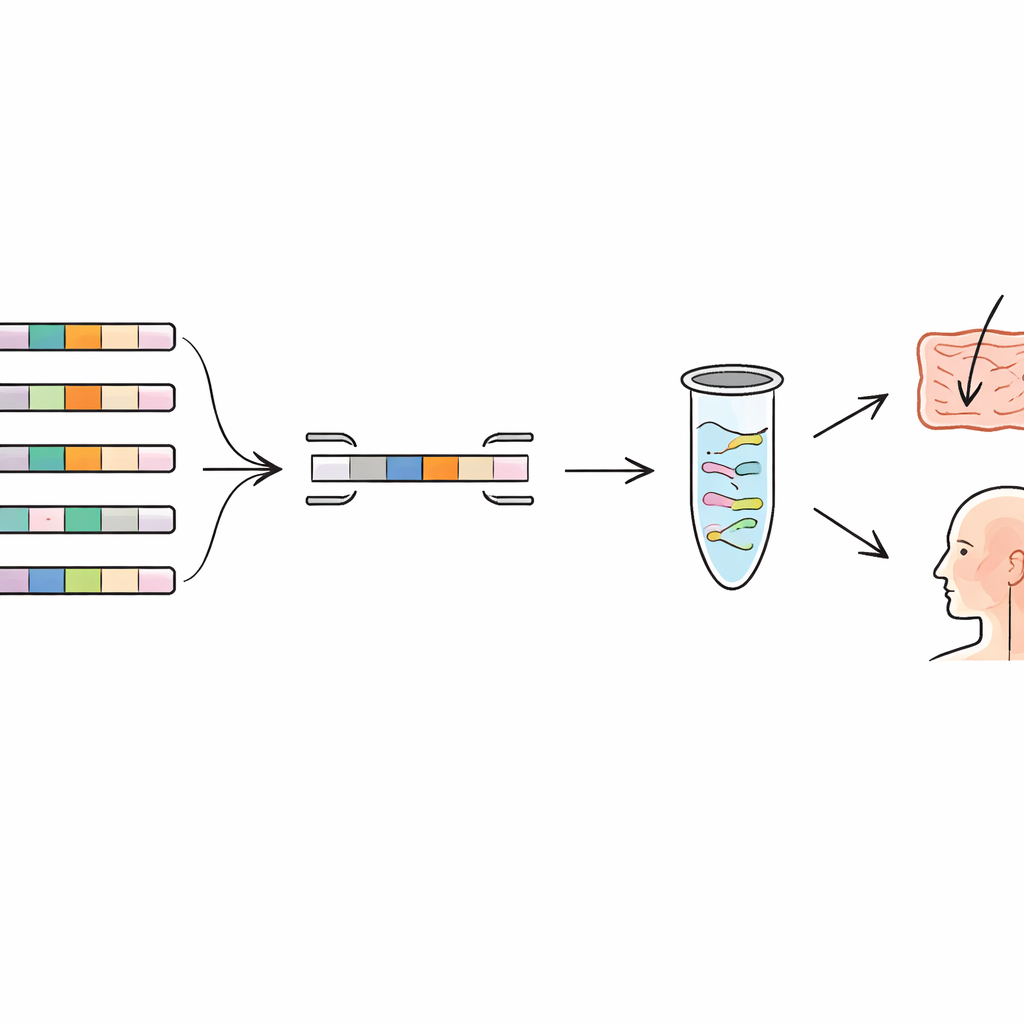
Suivre les probiotiques sur la peau et dans les voies respiratoires
Pour vérifier si cette approche fonctionne chez l’humain, les auteurs ont appliqué leurs amorces à des échantillons issus de trois essais d’intervention humains contrôlés par placebo. Dans une étude, des volontaires ont utilisé une crème pour le visage contenant deux souches probiotiques ; dans d’autres, des personnes ont reçu un spray buccal probiotique ou un comprimé à mâcher. Grâce aux nouveaux tests qPCR, les scientifiques ont pu détecter de manière fiable les souches ajoutées sur la peau et dans les voies respiratoires supérieures des participants traités, tandis qu’elles étaient presque absentes dans les groupes placebo. Ils ont également observé comment le signal augmentait pendant l’utilisation et diminuait après l’arrêt du traitement, donnant une image claire d’une colonisation temporaire. Dans quelques cas, de faibles signaux sont apparus chez les témoins, rappelant aux chercheurs de prendre en compte les bactéries naturellement présentes et le risque de très faibles contaminations, surtout sur des sites corporels à faible charge bactérienne.
Ce que cela signifie pour les thérapies microbiennes futures
Concrètement, ce travail montre comment construire un « radar de souches » très précis sans modifier génétiquement les bactéries elles‑mêmes. En exploitant des différences génétiques subtiles révélées par des comparaisons génomiques à grande échelle, les chercheurs peuvent concevoir des tests qPCR permettant d’isoler une souche probiotique parmi une foule de quasi‑semblables. Cela facilite grandement la réponse à des questions pratiques : la souche a‑t‑elle survécu à la durée de vie du produit ? A‑t‑elle atteint le site corporel ciblé ? Combien de temps est‑elle restée et à quelles concentrations ? Parce que la méthode est transparente, peu coûteuse et adaptable à d’autres espèces, elle peut devenir un outil standard pour la conception et l’évaluation des probiotiques de nouvelle génération et des produits biothérapeutiques vivants, apportant plus de rigueur et de sécurité au domaine en forte croissance des interventions basées sur le microbiome.
Citation: Eilers, T., Delanghe, L., De Boeck, I. et al. Pangenome-based design of strain-specific primers enables precise monitoring of bacteria in human microbiome intervention trials. Sci Rep 16, 11274 (2026). https://doi.org/10.1038/s41598-026-41449-8
Mots-clés: probiotiques, microbiome, suivi de souches, qPCR, analyse du pangenome