Clear Sky Science · ru
Проектирование штамм‑специфичных праймеров на основе пангенома позволяет точно отслеживать бактерии в клинических вмешательствах с участием микробиоты человека
Почему важно отслеживать полезные микроорганизмы
О многих бактериях принято говорить как о проблемных, но есть и тихие помощники: они превращают молоко в йогурт, защищают кожу и могут снижать воспаление в дыхательных путях. Эти «полезные бактерии» продают как пробиотики или как более строго регулируемые живые биотерапевтические препараты, и сейчас их проверяют в клинических испытаниях при кожных заболеваниях, аллергиях, проблемах с желудочно‑кишечным трактом и в других областях. Тем не менее на удивление трудно ответить на базовый вопрос: если мы даем человеку конкретный бактериальный штамм, можно ли доказать, что именно этот штамм выжил и закрепился в организме, а не только его близкие родственники? В этой работе предложен новый подход для высокоточного отслеживания индивидуальных бактериальных штаммов с использованием растущих массивов геномных данных.
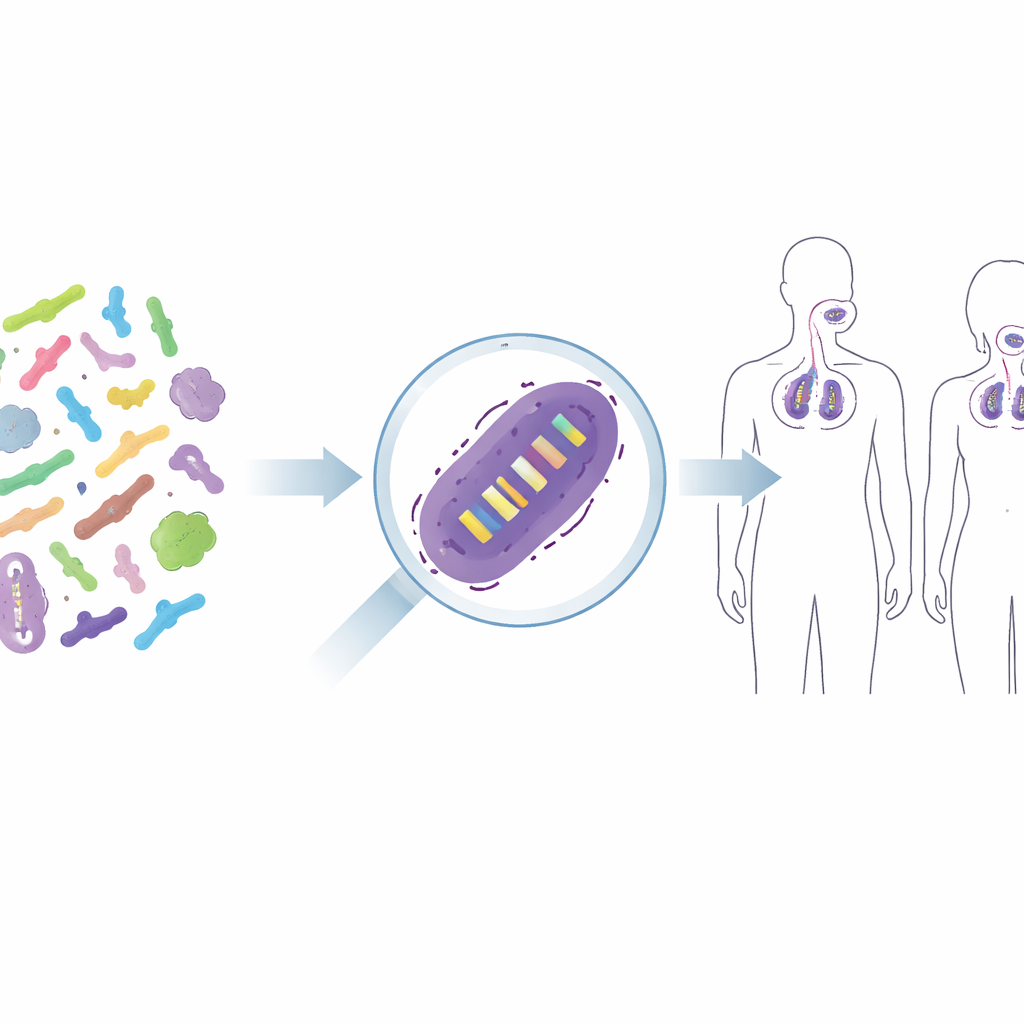
От смешанных сообществ к отдельным штаммам
Пробиотические продукты редко содержат абстрактных «бактерий»; они включают тщательно отобранные штаммы, например определенную версию Lacticaseibacillus rhamnosus GG или Lactiplantibacillus plantarum WCFS1. Близкородственные штаммы могут отличаться по взаимодействию с иммунной системой или по способности прикрепляться к коже или слизистой горла, поэтому исследователи и регуляторы хотят точно знать, какой именно штамм присутствует после лечения. Традиционные методы, такие как выращивание на селективных средах, дают сведения лишь о широких группах — например, о суммарных молочнокислых бактериях — и часто оказываются бесполезны, когда полезные штаммы сильно уступают числом другим. Более высокотехнологичные решения, например пометка штаммов флуоресцентными метками или ДНК‑штрихкодами, превращают их в генетически модифицированные организмы, что часто неприемлемо для пищевых продуктов или человеческих терапий. Задача — различать почти идентичные штаммы без их изменения.
Поиск уникальных генетических отпечатков в пангеноме
Авторы обратились к понятию «пангенома» — полного набора генов, встречающихся во множестве геномов одного вида. Одни гены присутствуют у всех представителей (ядро), другие — только у отдельных штаммов (доступная часть). Сравнив сотни геномов для нескольких видов молочнокислых бактерий и общего для полости рта вида, исследователи искали гены, которые встречаются лишь в одном штамме и не обнаруживаются у других известных родственных организмов. Такие редкие гены действуют как генетические отпечатки. Команда создала биоинформатический конвейер, который автоматически собирает пангеном, удаляет практически идентичные дубликаты геномов и выделяет штамм‑уникальные гены. Кандидаты затем проверяли на соответствие более широким базам геномов, чтобы убедиться, что схожие последовательности не скрыты в других видах.
Проектирование точных молекулярных «сканеров штрихкода»
После идентификации штамм‑уникальных генов следующим шагом было создание высокоспецифичных молекулярных тестов на их основе. Исследователи разработали короткие фрагменты ДНК — праймеры — которые связываются только с этими уникальными генами. В методе количественной ПЦР (qPCR) такие праймеры действуют как сканеры штрихкода, копируя и обнаруживая только ДНК целевого штамма. Команда создала и оптимизировала праймеры для шести штаммов разных видов, включая широко используемые пробиотики и новые кандидаты, выделенные из человеческого организма. В лаборатории они тестировали каждый набор праймеров не только на целевом штамме, но и на нескольких близкородственных штаммах того же вида. Тесты показали сильную амплификацию только для целевого штамма и минимальный сигнал от других, подтвердив, что выбранные генетические отпечатки действительно были отличительными.
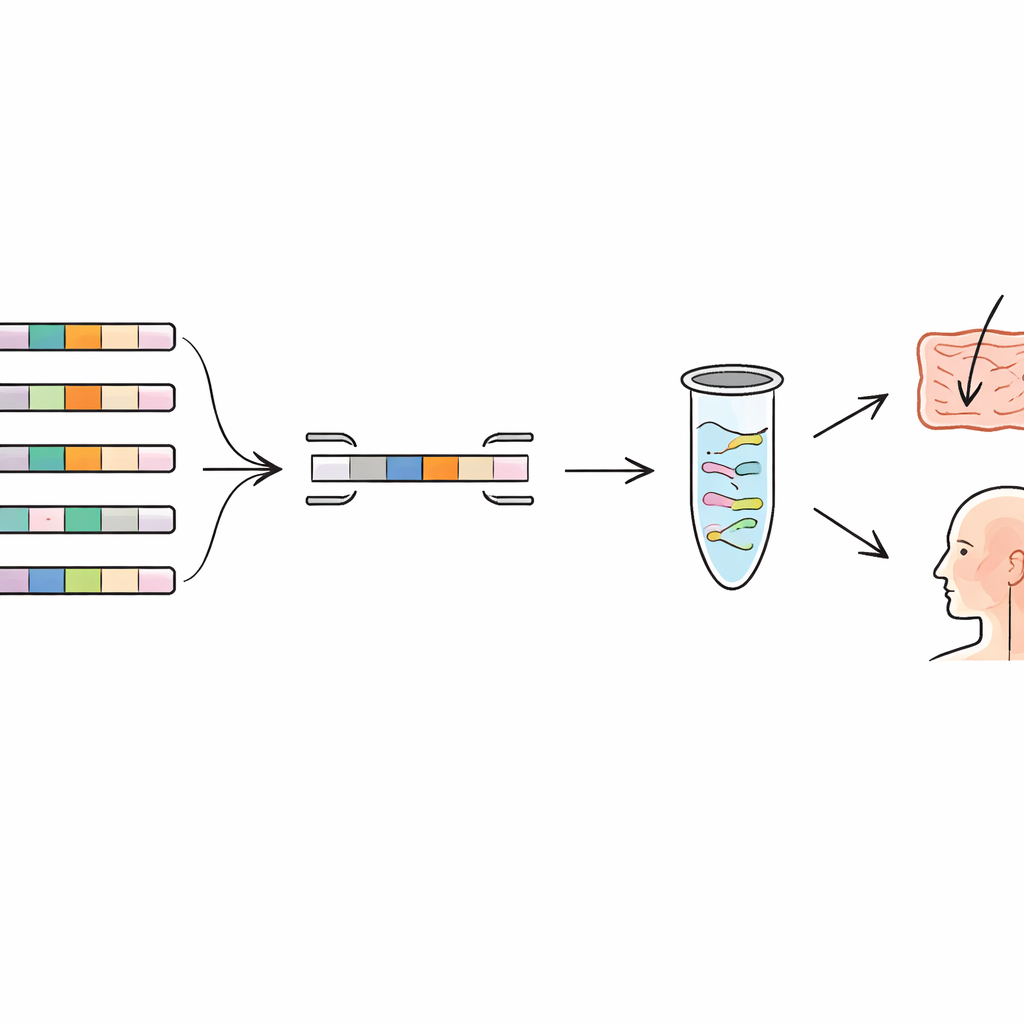
Отслеживание пробиотиков на коже и в дыхательных путях
Чтобы проверить подход на людях, авторы применили свои праймеры к образцам из трех плацебо‑контролируемых клинических испытаний. В одном исследовании добровольцы использовали крем для лица с двумя пробиотическими штаммами; в других люди получали пробиотический спрей для горла или разжевываемую таблетку. С помощью новых qPCR‑тестов ученые надежно обнаруживали добавленные штаммы на коже и в верхних дыхательных путях у участников, получавших лечение, тогда как почти никогда не видели их в группах плацебо. Они также наблюдали, как сигнал нарастал во время применения и снижался после прекращения лечения, получая четкое представление о временной колонизации. В нескольких случаях у контрольных образцов появлялись слабые сигналы, что напомнило исследователям о наличии естественного фонового микробиома и риске очень небольшой контаминации, особенно в участках тела с низким бактериальным обилием.
Что это значит для будущих микробиомных терапий
Проще говоря, эта работа показывает, как создать очень точный «радар штаммов», не вмешиваясь генетически в сами бактерии. Используя тонкие генетические различия, выявленные при масштабных сравнениях геномов, ученые могут разрабатывать qPCR‑тесты, которые выделяют один пробиотический штамм среди множества почти одинаковых. Это значительно упрощает практические вопросы: выдержал ли штамм срок годности продукта? Достиг ли он целевого участка организма? Как долго он сохранялся и в каких количествах? Поскольку метод прозрачен, недорог и применим к другим видам, он может стать стандартным инструментом при разработке и тестировании новых пробиотиков и живых биотерапевтических препаратов, повышая строгость и безопасность быстро развивающейся области вмешательств на основе микробиома.
Цитирование: Eilers, T., Delanghe, L., De Boeck, I. et al. Pangenome-based design of strain-specific primers enables precise monitoring of bacteria in human microbiome intervention trials. Sci Rep 16, 11274 (2026). https://doi.org/10.1038/s41598-026-41449-8
Ключевые слова: пробиотики, микробиом, трекинг штаммов, qPCR, анализ пангенома