Clear Sky Science · pl
Projektowanie starterów specyficznych dla szczepu oparte na pangenomie umożliwia precyzyjne monitorowanie bakterii w badaniach interwencyjnych na ludziach
Dlaczego warto śledzić pożyteczne mikroby
Wiele bakterii, o których słyszymy, to kłopotliwe organizmy, ale są też cisi sprzymierzeńcy, którzy przemieniają mleko w jogurt, chronią naszą skórę i mogą nawet łagodzić zapalenie dróg oddechowych. Te „dobre bakterie” sprzedawane są jako probiotyki lub — w przypadku ściśle regulowanych produktów leczniczych zawierających żywe mikroorganizmy — jako leki, i są obecnie testowane w badaniach na ludziach w kontekście problemów skórnych, alergii, schorzeń jelit i nie tylko. Jednak podstawowe pytanie okazuje się zaskakująco trudne do rozstrzygnięcia: gdy podajemy osobie konkretny szczep bakterii, czy potrafimy dowieść, że ten dokładny szczep przeżył i osiedlił się w organizmie, a nie tylko jego bliscy krewni? W niniejszym badaniu przedstawiono nową metodę śledzenia pojedynczych szczepów z dużą precyzją, wykorzystując rosnące zasoby danych genomowych.
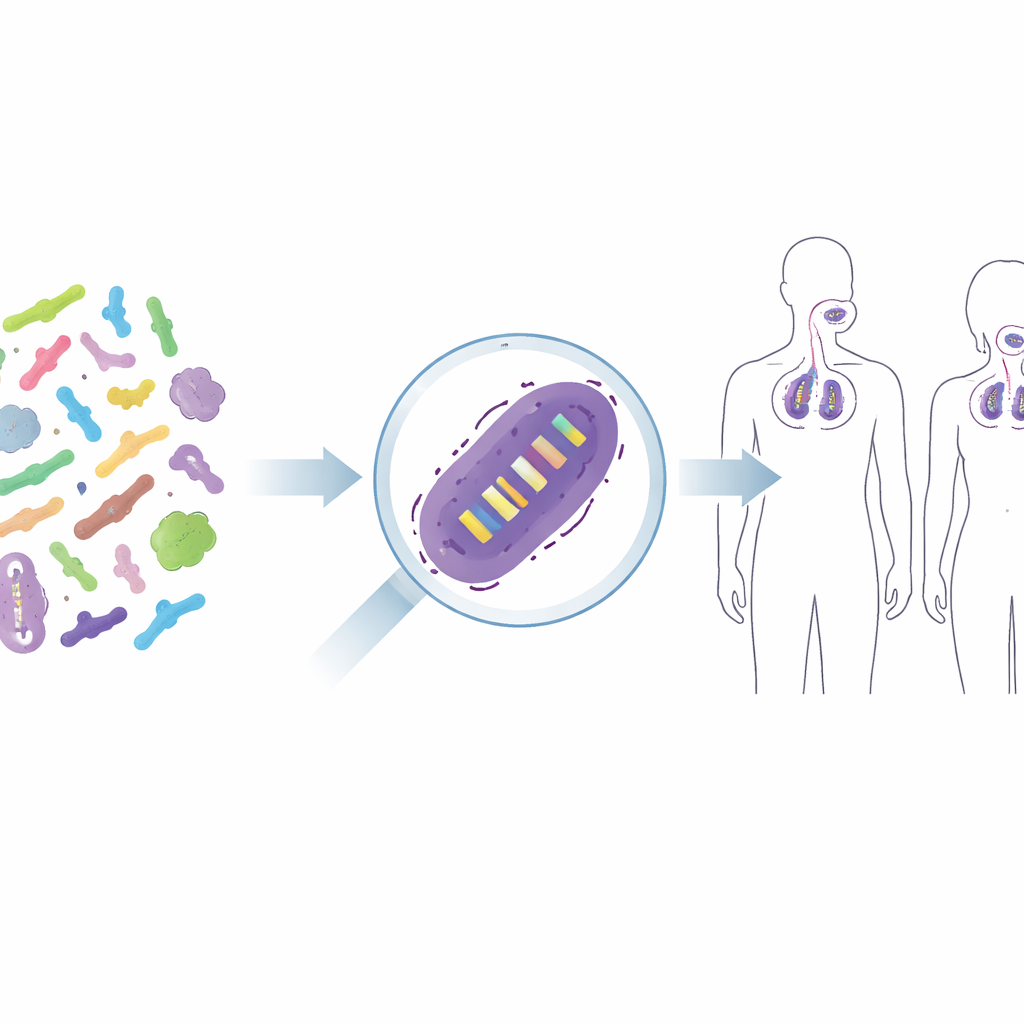
Z mieszanych mikrobiów do pojedynczych szczepów
Produkty probiotyczne rzadko zawierają „bakterie” w abstrakcyjnym znaczeniu; zawierają starannie wybrane szczepy, na przykład konkretną wersję Lacticaseibacillus rhamnosus GG albo Lactiplantibacillus plantarum WCFS1. Te blisko spokrewnione szczepy mogą różnić się sposobem interakcji z układem odpornościowym lub zdolnością przylegania do skóry czy błony śluzowej gardła, dlatego badacze i organy regulacyjne chcą wiedzieć dokładnie, który szczep występuje po terapii. Tradycyjne metody, takie jak hodowla na selektywnych pożywkach, informują jedynie o szerokich grupach — np. łącznej liczbie bakterii kwasu mlekowego — i często zawodzą, gdy korzystne szczepy są zdominowane przez inne. Bardziej zaawansowane rozwiązania, jak znakowanie szczepów markerami fluorescencyjnymi lub kodami DNA, przekształciłyby je w organizmy zmodyfikowane genetycznie, co często jest niedopuszczalne w przypadku żywności lub terapii dla ludzi. Wyzwanie polega na rozróżnieniu niemal identycznych szczepów bez ich modyfikowania.
Poszukiwanie unikalnych odcisków genetycznych w pangenomie
Autorzy sięgnęli po koncepcję „pangenomu”, czyli pełnego zbioru genów występujących w wielu genomach tego samego gatunku. Niektóre geny są wspólne dla wszystkich przedstawicieli (rdzeń), inne występują tylko w niektórych szczepach (część dodatkowa). Porównując setki genomów kilku gatunków bakterii kwasu mlekowego oraz powszechnego mikroba jamy ustnej, poszukiwali genów pojawiających się tylko w jednym szczepie i nieobecnych u żadnych znanych krewnych. Te rzadkie geny pełnią rolę odcisków genetycznych. Zespół zbudował pipeline bioinformatyczny, który automatycznie składa pangenom, usuwa niemal identyczne duplikaty genomów i wyłapuje geny unikalne dla szczepu. Następnie podwójnie weryfikowali te kandydatury względem szerszych baz genomowych, aby upewnić się, że podobne sekwencje nie ukrywają się w innych gatunkach.
Projektowanie precyzyjnych molekularnych „skanerów kodów kreskowych”
Gdy zidentyfikowano geny unikalne dla szczepu, kolejnym krokiem było zbudowanie wokół nich wysoce specyficznych testów molekularnych. Badacze zaprojektowali krótkie fragmenty DNA, zwane starterami (primers), które wiążą się wyłącznie z tymi unikalnymi genami. W technice zwanej ilościową PCR (qPCR) startery działają jak skanery kodów kreskowych, kopiując i wykrywając jedynie DNA docelowego szczepu. Zespół stworzył i zoptymalizował zestawy starterów dla sześciu szczepów należących do różnych gatunków, obejmujących powszechnie stosowane probiotyki oraz nowe kandydaty izolowane z ciała ludzkiego. W laboratorium testowali każdy zestaw starterów nie tylko na docelowym szczepie, ale też na kilku blisko spokrewnionych szczepach tego samego gatunku. Testy wykazały silną amplifikację jedynie dla szczepu docelowego, z minimalnym sygnałem z pozostałych, potwierdzając, że wybrane odciski genetyczne były rzeczywiście rozróżnialne.
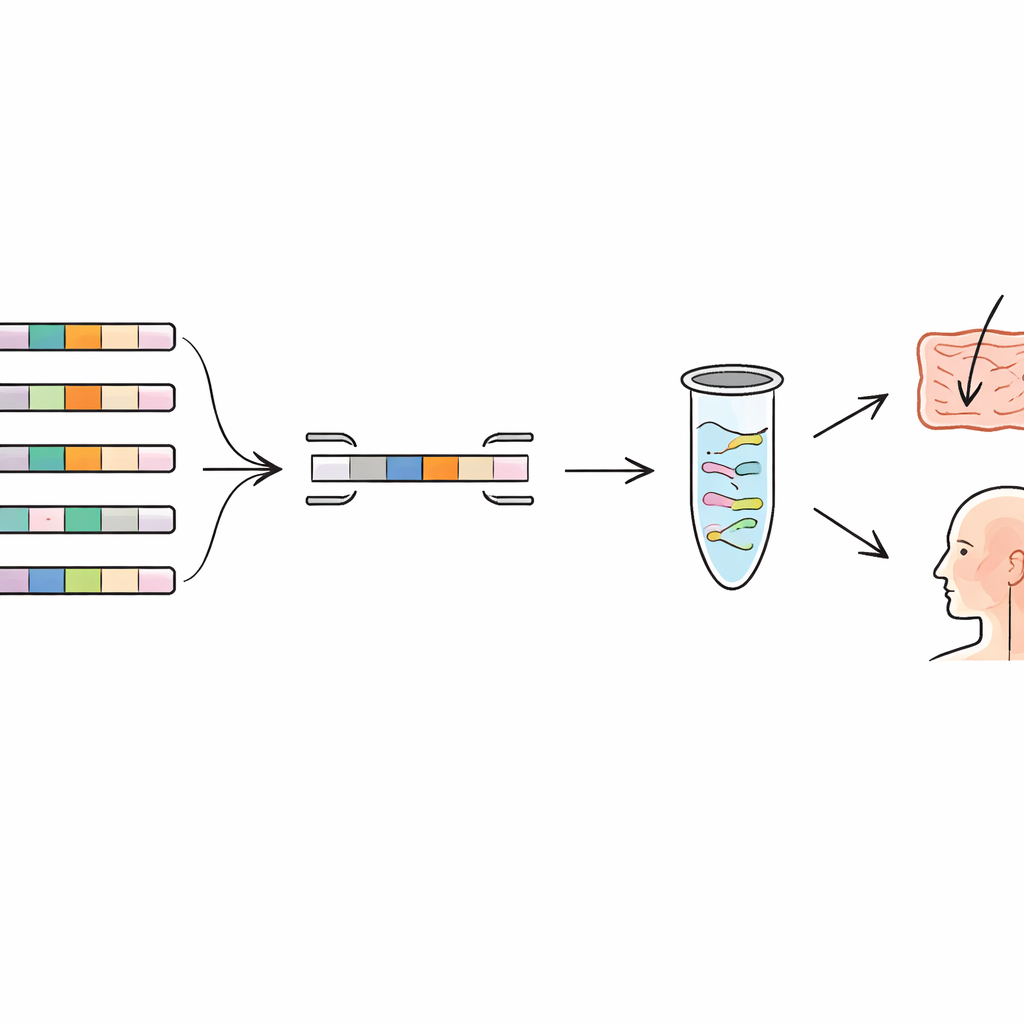
Śledzenie probiotyków na skórze i w drogach oddechowych
Aby sprawdzić, czy podejście działa u ludzi, autorzy zastosowali swoje startery do próbek pochodzących z trzech kontrolowanych placebo badań interwencyjnych. W jednym badaniu ochotnicy stosowali krem do twarzy zawierający dwa szczepy probiotyczne; w innych ludzie otrzymywali aerozol do gardła z probiotykiem lub tabletkę do żucia. Dzięki nowym testom qPCR naukowcy mogli wiarygodnie wykrywać dodane szczepy na skórze oraz w górnych drogach oddechowych uczestników leczenia, podczas gdy w grupach placebo prawie ich nie obserwowano. Zaobserwowano również, jak sygnał wzrastał podczas stosowania i zanikał po zaprzestaniu terapii, dając jasny obraz tymczasowej kolonizacji. W kilku przypadkach w kontrolach pojawiły się sygnały na niskim poziomie, co przypominało badaczom o konieczności uwzględnienia naturalnego tła bakteryjnego oraz ryzyka bardzo drobnego skażenia, szczególnie w miejscach ciała o niskiej liczbie bakterii.
Co to oznacza dla przyszłych terapii ukierunkowanych na mikrobiom
Mówiąc prościej, praca ta pokazuje, jak zbudować bardzo czuły „radar szczepu” bez genetycznego modyfikowania samych bakterii. Wykorzystując subtelne różnice genetyczne odkryte dzięki dużym porównaniom genomów, naukowcy mogą opracować testy qPCR, które wyłowią jeden szczep probiotyczny spośród tłumu niemal identycznych krewniaków. Ułatwia to odpowiedź na praktyczne pytania: czy szczep przetrwał okres przydatności produktu? Czy dotarł do docelowego miejsca w organizmie? Jak długo tam pozostał i w jakich ilościach? Ponieważ metoda jest przejrzysta, niedroga i można ją dostosować do innych gatunków, może stać się standardowym narzędziem do projektowania i testowania nowej generacji probiotyków oraz żywych produktów leczniczych, wnosząc więcej rygoru i bezpieczeństwa do dynamicznie rozwijającej się dziedziny interwencji opartych na mikrobiomie.
Cytowanie: Eilers, T., Delanghe, L., De Boeck, I. et al. Pangenome-based design of strain-specific primers enables precise monitoring of bacteria in human microbiome intervention trials. Sci Rep 16, 11274 (2026). https://doi.org/10.1038/s41598-026-41449-8
Słowa kluczowe: probiotyki, mikrobiom, śledzenie szczepów, qPCR, analiza pangenomu