Clear Sky Science · sv
En pipeline för maskininlärningsdrivna multimodala datafusionsmetoder för prognostisk riskanalys vid bevacizumab-behandlad metastaserande kolorektal cancer
Varför denna forskning är viktig
För personer som lever med avancerad tarmcancer är en av de största frågorna om ett kraftfullt men kostsamt läkemedel verkligen kommer att hjälpa dem. I denna studie undersöks hur mönster i en patients tumör-DNA, i kombination med klinisk information, kan användas tillsammans med modern maskininlärning för att förutsäga vem som sannolikt får nytta av en vanlig riktad behandling, bevacizumab, och vem som inte gör det. I framtiden skulle sådana verktyg kunna skona vissa patienter från biverkningar och ineffektiv behandling, samtidigt som andra styrs mot de mest lovande alternativen.
En närmare titt på behandling av tarmcancer
Metastaserande kolorektal cancer—tarmcancer som spridit sig till andra organ—är en huvudorsak till cancerdöd globalt. Många patienter vars tumörer bär specifika genförändringar (RAS-mutationer) får standardkemoterapi kombinerad med bevacizumab, ett läkemedel som blockerar blodkärlsbildning för att svälta tumörer. Även om denna kombination i genomsnitt förbättrar överlevnaden, är det bara en bråkdel av patienterna som ser en meningsfull nytta. Andra genomgår månader av behandling, biverkningar och ekonomiska kostnader med liten vinst. För närvarande har läkare inget pålitligt test för att i förväg säga vem som inte kommer att svara på bevacizumab, vilket skapar ett stort behov av bättre beslutsstöd.
Att föra samman många datatyper
Forskarlaget byggde en flerstegs analys-pipeline som använder maskininlärning för att foga samman flera typer av information från varje patient. De använde en väl karaktäriserad europeisk kohort kallad ANGIOPREDICT, som inkluderar 117 personer med metastaserande kolorektal cancer behandlade med bevacizumab plus kemoterapi. För varje patient hade de: regioner i genomet som antingen ökat eller förlorats (kopiantalvariationer), ett litet urval av viktiga genmutationer, och standard kliniska uppgifter såsom ålder, tumörstadium och tumörens läge. Ett specialiserat verktyg kallat PhenMap användes sedan för att upptäcka dolda mönster—så kallade meta-variabler—som sammanfattar hur dessa genetiska förändringar och kliniska drag varierar tillsammans över patienter.
Att hitta DNA-signaturen kopplad till utfall
Bland de tio mönster som identifierades av PhenMap var två starkt kopplade till hur länge patienterna levde utan att deras sjukdom försämrades, ett mått kallat progressionsfri överlevnad. Teamet fokuserade sedan på vilka specifika DNA-förändringar som drev dessa två nyckelmönster. Genom ytterligare statistiska och maskininlärningssteg minskade de ner hundratals genomiska regioner och mutationer till endast tre egenskaper: förluster i två kromosomala regioner (15q21.1 och 1p36.31) och mutation i en gen kallad BRAF. Dessa tre egenskaper tillsammans utgjorde en kompakt genetisk signatur som var starkt kopplad till sämre utfall hos patienter som fick bevacizumab.
Att omvandla en signatur till riskgrupper
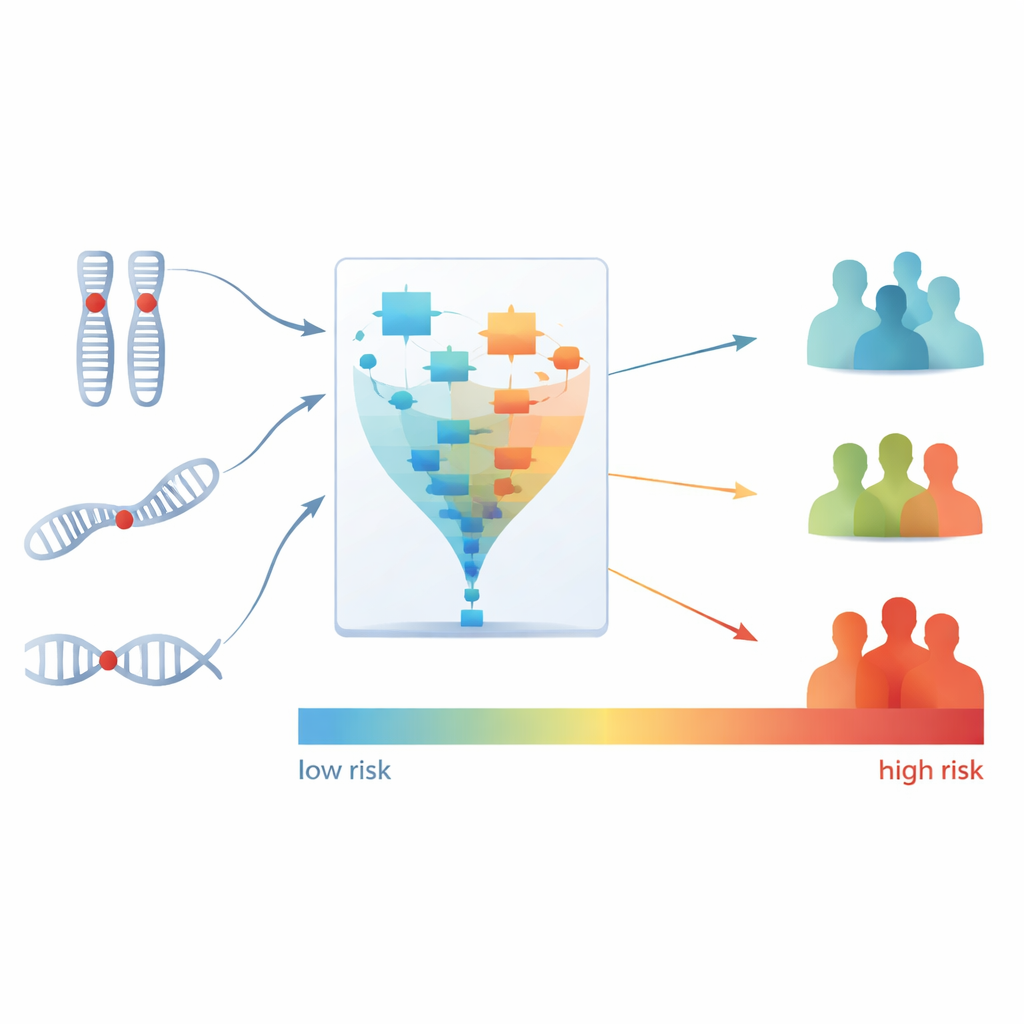
Nästa steg var att omvandla denna trefaldiga signatur till en enda riskscore för varje patient, som speglade deras uppskattade risk att avlida under bevacizumab-baserad behandling. De delade sedan in patienterna i tre grupper—låg, medel och hög risk—baserat på deras poäng. Skillnaderna var anmärkningsvärda: varje patient i hög-riskgruppen svarade inte på bevacizumab, medan de flesta patienter i låg-riskgruppen visade ett svar. Hög-riskgruppen hade också en mycket högre sannolikhet för tidig sjukdomsprogression jämfört med låg-riskgruppen. Viktigt är att denna riskscore gav prognostisk information utöver vad läkare redan kunde härleda från standard kliniska faktorer eller tidigare genomisk subtypning ensam.
Vad detta kan innebära för patienter
Även om detta arbete fortfarande behöver valideras i större och oberoende patientkohorter, pekar det mot en framtid där komplex tumör- och klinisk data kan integreras till en enda, handlingsbar riskscore. Om den bekräftas kan ett enkelt test som påvisar förekomsten av de två kromosomförlusterna och BRAF-mutation hjälpa till att identifiera patienter med metastaserande kolorektal cancer som troligen inte får nytta av bevacizumab-kombinationsterapi. Dessa patienter skulle då kunna hänvisas snabbare till alternativa strategier eller kliniska prövningar, medan andra fortsätter att få ett läkemedel som de med större sannolikhet gagnas av. Mer generellt skulle den maskininlärningspipeline som demonstreras här kunna anpassas till andra cancerformer och behandlingar, vilket främjar målet om verkligt personaliserad cancervård.
Citering: Thomas, V., Nyamundanda, G., Lärkeryd, A. et al. A pipeline of machine learning-driven multi-modal data fusion methods for prognostic risk analysis in bevacizumab-treated metastatic colorectal cancer. Sci Rep 16, 8843 (2026). https://doi.org/10.1038/s41598-026-39189-w
Nyckelord: metastaserande kolorektal cancer, bevacizumabresistens, maskininlärning, genomiska biomarkörer, precision-onkologi