Clear Sky Science · ar
خط أنابيب لطرق دمج بيانات متعددة النماذج مدفوعة بتعلم الآلة لتحليل مخاطر التنبؤ في سرطان القولون والمستقيم النقيلي المعالج ببيفاسيزوماب
لماذا تهم هذه الدراسة
بالنسبة للأشخاص الذين يعيشون مع سرطان الأمعاء المتقدم، فإن أحد أكبر الأسئلة هو ما إذا كان دواء قوي لكنه مكلف سيفيدهم بالفعل أم لا. تستكشف هذه الدراسة كيف يمكن أن تُستخدم أنماط الحمض النووي في ورم المريض، مجتمعة مع معلومات سريرية، مع تقنيات تعلم الآلة الحديثة للتنبؤ بمن من المرجح أن يستفيد من علاج مستهدف شائع، وهو بيفاسيزوماب، ومن لن يستفيد. في المستقبل، قد توفر مثل هذه الأدوات على بعض المرضى آثارًا جانبية وعلاجات غير فعالة، وفي الوقت نفسه توجه الآخرين نحو الخيارات الأكثر وعدًا.
نظرة أقرب على علاج سرطان الأمعاء
يعد سرطان القولون والمستقيم النقيلي — أي سرطان الأمعاء الذي انتشر إلى أعضاء أخرى — سببًا رئيسيًا للوفاة بسبب السرطان على مستوى العالم. يتلقى العديد من المرضى الذين تحمل أورامهم تغييرات جينية محددة (طفرات في جين RAS) العلاج الكيميائي القياسي مضافًا إليه بيفاسيزوماب، وهو دواء يعيق نمو الأوعية الدموية ليجوع الأورام. رغم أن هذا المزيج يحسن البقاء على قيد الحياة في المتوسط، فإن جزءًا صغيرًا فقط من المرضى يحقق فائدة معنوية. ويعاني الآخرون من شهور من العلاج والآثار الجانبية والتكلفة المالية مع القليل من المكاسب. في الوقت الحالي، لا يملك الأطباء اختبارًا موثوقًا ليخبرهم مسبقًا بمن لن يستجيب لبيفاسيزوماب، مما يخلق حاجة ملحة لأدوات قرار أفضل.
دمج أنواع بيانات متعددة
بنَت المجموعة البحثية خط تحليل متعدد المراحل يستخدم تعلم الآلة لدمج عدة أنواع من المعلومات لكل مريض. اعتمدوا على مجموعة أوروبية موثقة جيدًا تُدعى ANGIOPREDICT، والتي تشمل 117 شخصًا مصابًا بسرطان القولون والمستقيم النقيلي عولجوا بيفاسيزوماب مع العلاج الكيميائي. لكل مريض كانت لديهم: مناطق من الجينوم إما مُكسبة أو مفقودة (تغيّرات في عدد النسخ)، ومجموعة صغيرة من الطفرات الجينية المهمة، وتفاصيل سريرية قياسية مثل العمر ومرحلة الورم وموقع الورم. ثم استُخدمت أداة متخصصة تُسمى PhenMap للكشف عن أنماط خفية — تُدعى متغيرات فوقية — تلخص كيف تتغير هذه التغيرات الجينية والميزات السريرية معًا عبر المرضى.
اكتشاف التوقيع الجيني المرتبط بالنتيجة
من بين عشر أنماط حددها PhenMap، ارتبط اثنان منها بقوة لمدة بقاء المرضى دون تدهور، وهي مقياس يُسمى البقاء دون تقدم المرض. ثم ركز الفريق على أي التغيرات الجينية المحددة دفعت هذين النمطين الرئيسيين. باستخدام خطوات إحصائية وتعلم آلة إضافية، قلصوا مئات المناطق الجينومية والطفرات إلى ثلاث ميزات فقط: خسائر في منطقتين كروموسوميتين (15q21.1 و1p36.31) وطفرَة في جين يُدعى BRAF. شكلت هذه الميزات الثلاث معًا توقيعًا جينيًا مضغوطًا ارتبط ارتباطًا وثيقًا بنتائج أسوأ لدى المرضى الذين تلقوا بيفاسيزوماب.
تحويل التوقيع إلى مجموعات مخاطر
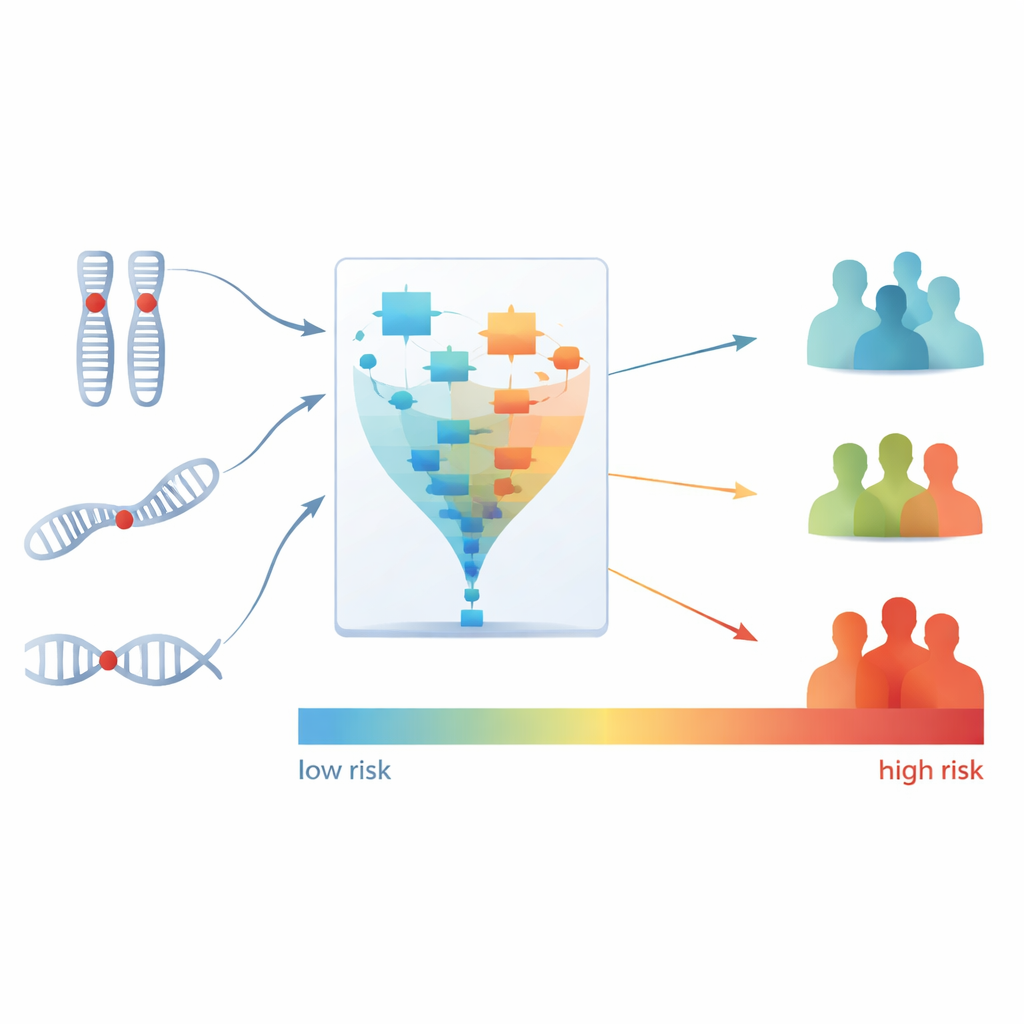
بعد ذلك، حول العلماء هذا التوقيع المكوّن من ثلاثة أجزاء إلى درجة خطر واحدة لكل مريض، تعكس مخاطر الوفاة المقدرة أثناء العلاج القائم على بيفاسيزوماب. ثم قسموا المرضى إلى ثلاث مجموعات — مخاطر منخفضة ومتوسطة وعالية — بناءً على درجاتهم. كانت الفروق مذهلة: فكل مريض في مجموعة المخاطر العالية لم يستجب لبيفاسيزوماب، بينما أظهر معظم المرضى في مجموعة المخاطر المنخفضة استجابة. كما أن مجموعة المخاطر العالية كان لديها فرصة أكبر بكثير للتقدم المبكر للمرض مقارنة بالمجموعة ذات المخاطر المنخفضة. والأهم من ذلك، أن درجة الخطر هذه قدمت معلومات تنبؤية تتجاوز ما يمكن للأطباء استنتاجه بالفعل من العوامل السريرية القياسية أو من التصنيف الجينومي السابق وحده.
ما الذي قد يعنيه هذا للمرضى
على الرغم من أن هذه الدراسة لا تزال بحاجة إلى التحقق منها في مجموعات مرضى أكبر ومستقلة، فإنها تشير إلى مستقبل يمكن فيه دمج بيانات الأورام والبيانات السريرية المعقدة في درجة خطر واحدة قابلة للاستخدام سريريًا. إذا تأكدت النتائج، فقد يساعد اختبار بسيط يقيس وجود خسارتي الكروموسومين وطفرَة BRAF في تحديد مرضى سرطان القولون والمستقيم النقيلي الذين من غير المرجح أن يستفيدوا من علاج تركيبي يشمل بيفاسيزوماب. ويمكن توجيه هؤلاء المرضى نحو استراتيجيات بديلة أو تجارب إكلينيكية في وقت أبكر، بينما يستمر الآخرون في تلقي دواء من المرجح أن يستفيدوا منه. وعلى نطاق أوسع، يمكن تكييف خط تعلم الآلة الموضح هنا مع سرطانات وعلاجات أخرى، مما يدفع نحو هدف رعاية سرطانية مخصصة حقًا.
الاستشهاد: Thomas, V., Nyamundanda, G., Lärkeryd, A. et al. A pipeline of machine learning-driven multi-modal data fusion methods for prognostic risk analysis in bevacizumab-treated metastatic colorectal cancer. Sci Rep 16, 8843 (2026). https://doi.org/10.1038/s41598-026-39189-w
الكلمات المفتاحية: سرطان القولون والمستقيم النقيلي, مقاومة بيفاسيزوماب, تعلّم الآلة, المؤشرات الحيوية الجينومية, الطب الدقيق في السرطان