Clear Sky Science · ru
Конвейер методов многомодальной фьюжн-аналитики на основе машинного обучения для прогностического анализа риска у больных метастатическим раком толстой кишки, леченных бевацизумабом
Почему это исследование важно
Для людей с распространенным раком кишечника одним из главных вопросов является, принесет ли им пользу мощный, но дорогой препарат. В этом исследовании изучают, как сочетание закономерностей в ДНК опухоли пациента и клинических данных можно использовать с помощью современных методов машинного обучения, чтобы предсказать, кто, вероятно, извлечет пользу из широко применяемого таргетного лечения бевацизумабом, а кто — нет. В будущем такие инструменты могли бы оградить некоторых пациентов от побочных эффектов и неэффективной терапии и направить других к наиболее перспективным вариантам лечения.
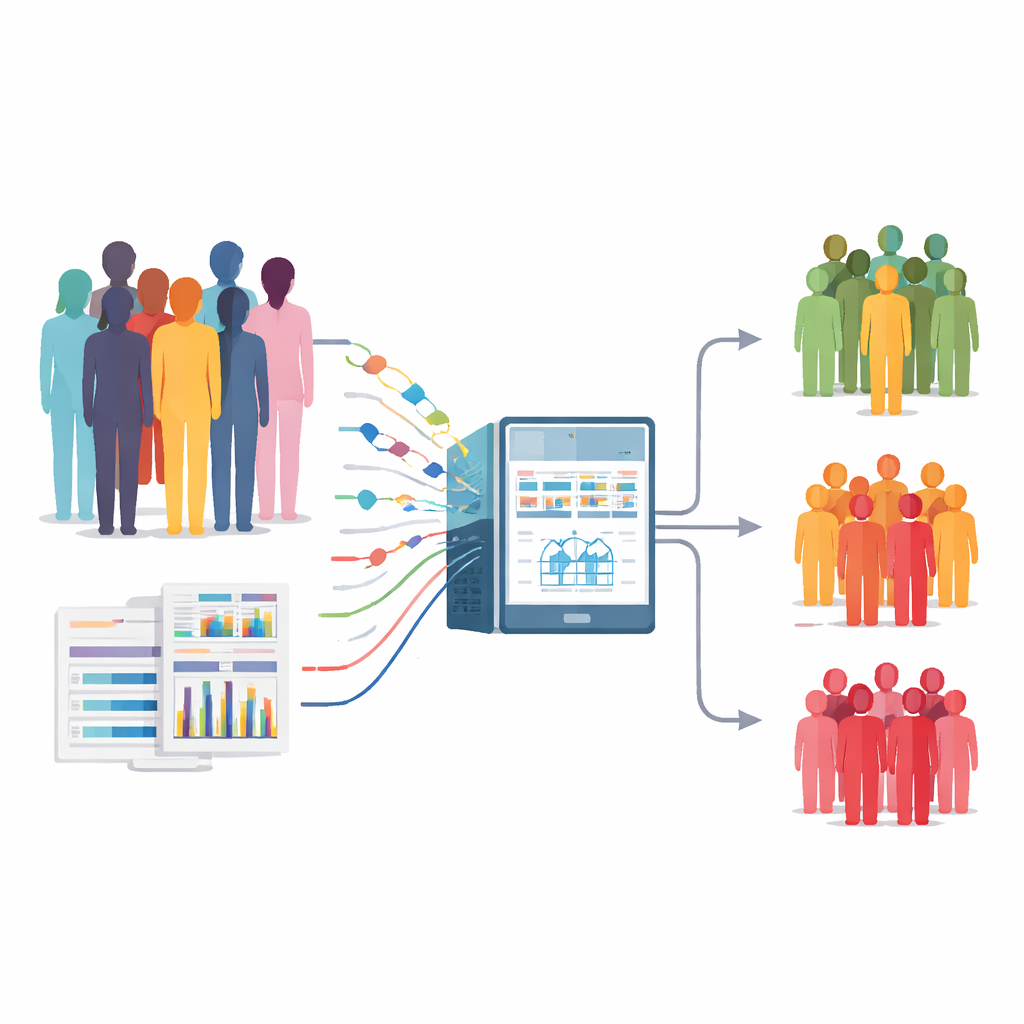
Более близкий взгляд на лечение рака кишечника
Метастатический рак толстой кишки — то есть опухоль, распространившаяся в другие органы — является одной из ведущих причин смертности от рака в мире. Многим пациентам с опухолями, несущими специфические генетические изменения (мутации RAS), назначают стандартную химиотерапию в сочетании с бевацизумабом — препаратом, блокирующим рост сосудов и тем самым лишающим опухоль кровоснабжения. Хотя в среднем такая комбинация улучшает выживаемость, лишь у части пациентов наблюдается значимый эффект. Другие проходят месяцы лечения, переносят побочные эффекты и несут финансовые затраты без заметной пользы. В настоящее время врачи не располагают надежным тестом, который заранее бы показал, кто не ответит на бевацизумаб, что создает острую потребность в лучших инструментах для принятия решений.
Объединение множества типов данных
Исследователи разработали многоэтапный аналитический конвейер, использующий машинное обучение для слияния нескольких видов информации по каждому пациенту. Они опирались на хорошо охарактеризованную европейскую когорту ANGIOPREDICT, включающую 117 человек с метастатическим раком толстой кишки, лечившихся бевацизумабом в комбинации с химиотерапией. Для каждого пациента были доступны: участки генома с утратами или приращениями копий (копийные изменения числа), небольшой набор значимых генетических мутаций и стандартные клинические данные, такие как возраст, стадия опухоли и ее локализация. Специализированный инструмент под названием PhenMap затем использовали для выявления скрытых закономерностей — так называемых мета-переменных, которые суммируют совместное изменение этих генетических и клинических характеристик у разных пациентов.
Нахождение ДНК-подписи, связанной с исходом
Среди десяти закономерностей, выделенных PhenMap, две были тесно связаны с тем, как долго пациенты жили без прогрессирования заболевания, показателем, называемым безрецидивной выживаемостью. Команда сосредоточилась на том, какие конкретные изменения в ДНК определяли эти две ключевые закономерности. С применением дополнительных статистических и машинно-обучающих шагов они сузили сотни геномных регионов и мутаций до всего трех признаков: утраты в двух хромосомных областях (15q21.1 и 1p36.31) и мутации в гене BRAF. Эти три признака вместе образовали компактную генетическую подпись, тесно связанную с более плохими исходами у пациентов, получавших бевацизумаб.
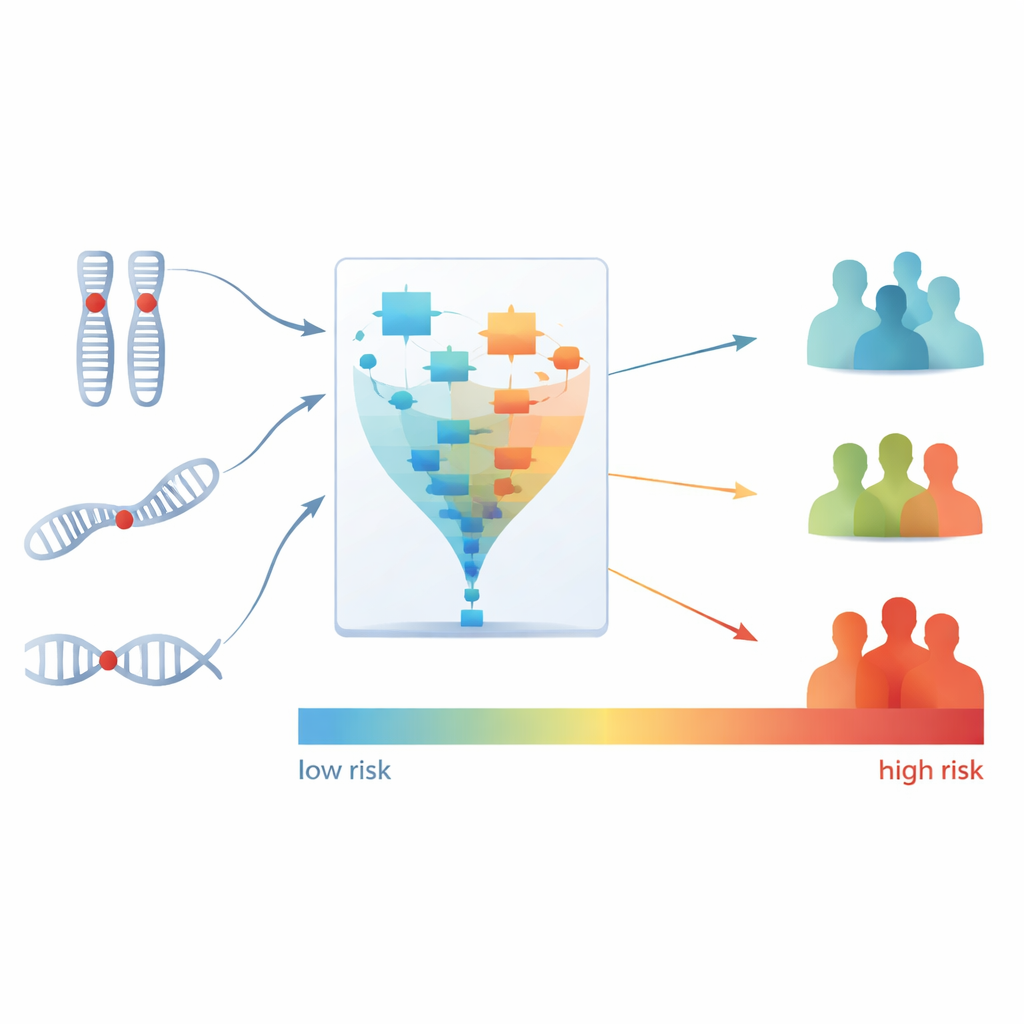
Преобразование подписи в группы риска
Далее ученые преобразовали эту трехкомпонентную подпись в единый риск‑скор для каждого пациента, отражающий оценочный риск смерти при терапии на основе бевацизумаба. Затем пациентов разделили на три группы — низкого, среднего и высокого риска — по их баллам. Различия оказались поразительными: все пациенты в группе высокого риска не ответили на бевацизумаб, тогда как большинство пациентов в группе низкого риска показали ответ. Группа высокого риска также имела значительно более высокую вероятность раннего прогрессирования по сравнению с группой низкого риска. Что важно, этот скор предоставлял прогностическую информацию, выходящую за рамки того, что врачи могли уже сделать выводить на основе стандартных клинических факторов или ранее выполненной геномной типизации.
Что это может означать для пациентов
Хотя эта работа требует подтверждения в больших и независимых когортах пациентов, она указывает на будущее, в котором сложные данные об опухоли и клинические показатели можно интегрировать в единый, практически применимый скор риска. Если результаты подтвердятся, простой тест, определяющий наличие двух хромосомных утрат и мутации BRAF, мог бы помочь выявить пациентов с метастатическим раком толстой кишки, маловероятно получающих пользу от комбинированной терапии с бевацизумабом. Таких пациентов можно будет раньше направить на альтернативные стратегии или клинические исследования, а другие продолжат получать препарат, от которого они с большей вероятностью получат пользу. В более широком смысле продемонстрированный здесь конвейер машинного обучения может быть адаптирован к другим видам рака и методам лечения, продвигая цель по-настоящему персонализированной онкологической помощи.
Цитирование: Thomas, V., Nyamundanda, G., Lärkeryd, A. et al. A pipeline of machine learning-driven multi-modal data fusion methods for prognostic risk analysis in bevacizumab-treated metastatic colorectal cancer. Sci Rep 16, 8843 (2026). https://doi.org/10.1038/s41598-026-39189-w
Ключевые слова: метастатический рак толстой кишки, резистентность к бевацизумабу, машинное обучение, геномные биомаркеры, персонализированная онкология