Clear Sky Science · it
Una pipeline di metodi di fusione di dati multimodali guidati da machine learning per l’analisi prognostica del rischio nel carcinoma colorettale metastatico trattato con bevacizumab
Perché questa ricerca è importante
Per le persone che convivono con un tumore intestinale avanzato, una delle domande principali è se un farmaco potente ma costoso avrà realmente benefici per loro. Questo studio esplora come i modelli nel DNA del tumore di un paziente, combinati con informazioni cliniche, possano essere utilizzati con il machine learning moderno per prevedere chi è probabile che tragga vantaggio da un trattamento mirato comune, il bevacizumab, e chi no. In futuro, strumenti di questo tipo potrebbero risparmiare ad alcuni pazienti effetti collaterali e terapie inefficaci, indirizzando altri verso le opzioni più promettenti.
Uno sguardo più attento al trattamento del tumore intestinale
Il carcinoma colorettale metastatico — il tumore dell’intestino che si è diffuso in altri organi — è una causa importante di morte per cancro a livello mondiale. Molti pazienti i cui tumori presentano specifiche alterazioni geniche (mutazioni RAS) ricevono chemioterapia standard combinata con bevacizumab, un farmaco che blocca la formazione di nuovi vasi sanguigni per “affamare” il tumore. Sebbene questa combinazione migliori la sopravvivenza in media, solo una frazione dei pazienti ottiene un beneficio significativo. Altri affrontano mesi di trattamento, effetti collaterali e costi finanziari con pochi vantaggi. Attualmente i medici non dispongono di un test affidabile per dire in anticipo chi non risponderà al bevacizumab, creando un bisogno urgente di strumenti decisionali migliori.
Integrare molti tipi di dati
I ricercatori hanno costruito una pipeline di analisi in più fasi che usa il machine learning per fondere diversi tipi di informazioni di ciascun paziente. Hanno fatto riferimento a una coorte europea ben caratterizzata chiamata ANGIOPREDICT, che include 117 persone con carcinoma colorettale metastatico trattate con bevacizumab più chemioterapia. Per ogni paziente disponevano di: regioni del genoma che risultavano guadagnate o perse (alterazioni del numero di copie), un piccolo insieme di mutazioni geniche rilevanti e dettagli clinici standard come età, stadio del tumore e sede del tumore. Uno strumento specializzato chiamato PhenMap è stato poi utilizzato per scoprire schemi nascosti — chiamati meta-variabili — che riassumono come questi cambiamenti genetici e le caratteristiche cliniche variano insieme tra i pazienti.
Individuare la firma del DNA collegata all’esito
Tra i dieci schemi identificati da PhenMap, due risultarono fortemente correlati alla durata della sopravvivenza libera da progressione, una misura chiamata progression-free survival. Il team si è quindi concentrato su quali specifici cambiamenti del DNA guidassero questi due schemi chiave. Usando ulteriori passaggi statistici e di machine learning, hanno ridotto centinaia di regioni genomiche e mutazioni a sole tre caratteristiche: perdite in due regioni cromosomiche (15q21.1 e 1p36.31) e la mutazione in un gene chiamato BRAF. Queste tre caratteristiche, prese insieme, hanno formato una firma genetica compatta strettamente associata a esiti peggiori nei pazienti trattati con bevacizumab.
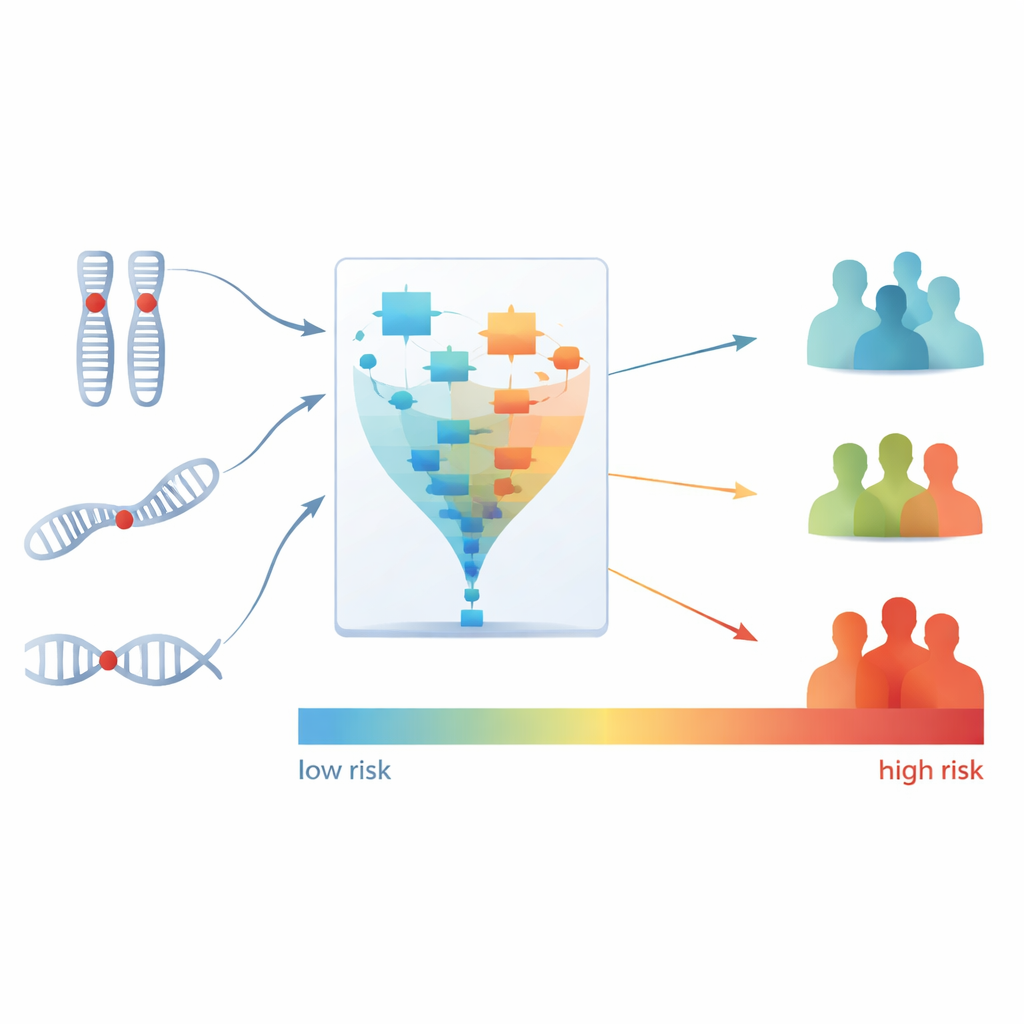
Trasformare una firma in gruppi di rischio
Successivamente, gli scienziati hanno convertito questa firma in tre elementi in un singolo punteggio di rischio per ciascun paziente, riflettendo il rischio stimato di morte durante la terapia a base di bevacizumab. Hanno poi diviso i pazienti in tre gruppi — basso, medio e alto rischio — in base ai loro punteggi. Le differenze sono state sorprendenti: ogni paziente nel gruppo ad alto rischio non ha risposto al bevacizumab, mentre la maggior parte dei pazienti nel gruppo a basso rischio ha mostrato una risposta. Il gruppo ad alto rischio ha anche avuto una probabilità molto maggiore di progressione precoce della malattia rispetto al gruppo a basso rischio. È importante sottolineare che questo punteggio di rischio ha fornito informazioni prognostiche oltre a quelle che i medici potevano già dedurre dai fattori clinici standard o dalla sola sottotipizzazione genomica precedente.
Cosa potrebbe significare per i pazienti
Sebbene questo lavoro debba ancora essere convalidato in coorti di pazienti più ampie e indipendenti, indica un futuro in cui dati tumorali e clinici complessi possono essere integrati in un unico punteggio di rischio azionabile. Se confermato, un test semplice che rileva la presenza delle due perdite cromosomiche e della mutazione BRAF potrebbe aiutare a identificare i pazienti con carcinoma colorettale metastatico che probabilmente non trarranno beneficio dalla terapia combinata con bevacizumab. Questi pazienti potrebbero così essere indirizzati più rapidamente verso strategie alternative o trial clinici, mentre altri continuerebbero a ricevere un farmaco dal quale è più probabile che traggano beneficio. Più in generale, la pipeline di machine learning presentata qui potrebbe essere adattata ad altri tumori e trattamenti, promuovendo l’obiettivo di una cura oncologica veramente personalizzata.
Citazione: Thomas, V., Nyamundanda, G., Lärkeryd, A. et al. A pipeline of machine learning-driven multi-modal data fusion methods for prognostic risk analysis in bevacizumab-treated metastatic colorectal cancer. Sci Rep 16, 8843 (2026). https://doi.org/10.1038/s41598-026-39189-w
Parole chiave: carcinoma colorettale metastatico, resistenza al bevacizumab, machine learning, biomarcatori genomici, oncologia di precisione