Clear Sky Science · pt
Uma linha de métodos de fusão de dados multimodais orientada por aprendizado de máquina para análise prognóstica de risco em câncer colorretal metastático tratado com bevacizumabe
Por que esta pesquisa importa
Para pessoas com câncer intestinal avançado, uma das maiores questões é se um medicamento potente, porém caro, realmente as beneficiará. Este estudo explora como padrões no DNA tumoral de um paciente, combinados com informações clínicas, podem ser usados com técnicas modernas de aprendizado de máquina para prever quem tem probabilidade de se beneficiar de um tratamento alvo comum, o bevacizumabe, e quem não. No futuro, tais ferramentas poderiam poupar alguns pacientes de efeitos colaterais e terapias ineficazes, ao mesmo tempo em que orientariam outros às opções mais promissoras.
Um olhar mais atento ao tratamento do câncer intestinal
O câncer colorretal metastático — câncer intestinal que se espalhou para outros órgãos — é uma causa importante de mortes por câncer no mundo. Muitos pacientes cujos tumores apresentam alterações genéticas específicas (mutações em RAS) recebem quimioterapia padrão combinada com bevacizumabe, uma droga que bloqueia o crescimento de vasos sanguíneos para “sufocar” os tumores. Embora essa combinação melhore a sobrevida em média, apenas uma parcela dos pacientes obtém benefício significativo. Outros enfrentam meses de tratamento, efeitos colaterais e custo financeiro com pouco ganho. Atualmente, os médicos não dispõem de um teste confiável para prever antecipadamente quem não responderá ao bevacizumabe, o que cria uma necessidade urgente por melhores ferramentas de decisão.
Integrando muitos tipos de dados
Os pesquisadores construíram um pipeline de análise em várias etapas que usa aprendizado de máquina para fundir vários tipos de informação de cada paciente. Eles recorreram a uma coorte europeia bem caracterizada chamada ANGIOPREDICT, que inclui 117 pessoas com câncer colorretal metastático tratadas com bevacizumabe mais quimioterapia. Para cada paciente tinham: regiões do genoma que foram ganhas ou perdidas (alterações no número de cópias), um pequeno conjunto de mutações gênicas importantes e detalhes clínicos padrão, como idade, estágio do tumor e localização do tumor. Uma ferramenta especializada chamada PhenMap foi então usada para descobrir padrões ocultos — chamados metavariáveis — que resumem como essas mudanças genéticas e características clínicas variam em conjunto entre os pacientes.
Encontrando a assinatura de DNA ligada ao desfecho
Entre os dez padrões identificados pelo PhenMap, dois estavam fortemente ligados ao tempo que os pacientes viveram sem piora da doença, uma medida chamada sobrevida livre de progressão. A equipe então concentrou-se em quais mudanças específicas de DNA impulsionavam esses dois padrões-chave. Usando etapas adicionais de estatística e aprendizado de máquina, reduziram centenas de regiões genômicas e mutações a apenas três características: perdas em duas regiões cromossômicas (15q21.1 e 1p36.31) e mutação em um gene chamado BRAF. Essas três características juntas formaram uma assinatura genética compacta que se correlacionou fortemente com desfechos piores em pacientes que receberam bevacizumabe.
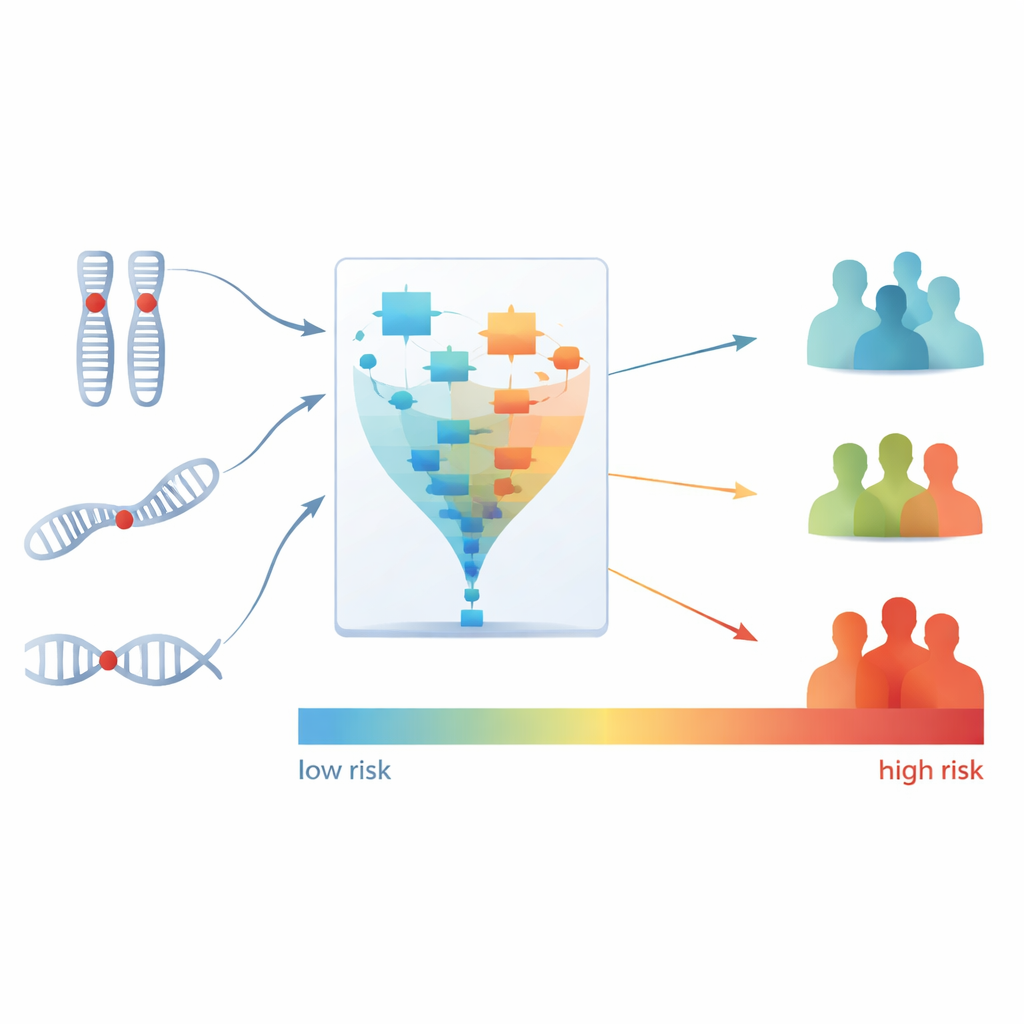
Transformando uma assinatura em grupos de risco
Em seguida, os cientistas converteram essa assinatura de três partes em um único escore de risco para cada paciente, refletindo o risco estimado de morte durante a terapia baseada em bevacizumabe. Eles então dividiram os pacientes em três grupos — baixo, médio e alto risco — com base em seus escores. As diferenças foram marcantes: todos os pacientes do grupo de alto risco não responderam ao bevacizumabe, enquanto a maioria dos pacientes do grupo de baixo risco apresentou resposta. O grupo de alto risco também teve uma chance muito maior de progressão precoce da doença em comparação com o grupo de baixo risco. Importante, esse escore de risco ofereceu informação prognóstica além do que os médicos já podiam inferir a partir de fatores clínicos padrão ou da subtipagem genômica prévia isoladamente.
O que isso pode significar para os pacientes
Embora este trabalho ainda precise ser validado em coortes de pacientes maiores e independentes, ele aponta para um futuro em que dados tumorais e clínicos complexos possam ser integrados em um único escore de risco acionável. Se confirmado, um teste simples que detecte a presença das duas perdas cromossômicas e da mutação em BRAF poderia ajudar a identificar pacientes com câncer colorretal metastático que provavelmente não se beneficiariam da terapia combinada com bevacizumabe. Esses pacientes poderiam então ser direcionados mais cedo para estratégias alternativas ou para ensaios clínicos, enquanto outros continuam a receber um medicamento do qual têm maior probabilidade de se beneficiar. Mais amplamente, o pipeline de aprendizado de máquina demonstrado aqui poderia ser adaptado a outros cânceres e tratamentos, avançando o objetivo de um cuidado oncológico verdadeiramente personalizado.
Citação: Thomas, V., Nyamundanda, G., Lärkeryd, A. et al. A pipeline of machine learning-driven multi-modal data fusion methods for prognostic risk analysis in bevacizumab-treated metastatic colorectal cancer. Sci Rep 16, 8843 (2026). https://doi.org/10.1038/s41598-026-39189-w
Palavras-chave: câncer colorretal metastático, resistência ao bevacizumabe, aprendizado de máquina, biomarcadores genômicos, oncologia de precisão