Clear Sky Science · es
Una canalización de métodos de fusión de datos multimodales impulsados por aprendizaje automático para el análisis pronóstico de riesgo en cáncer colorrectal metastásico tratado con bevacizumab
Por qué importa esta investigación
Para las personas con cáncer de colon avanzado, una de las mayores incógnitas es si un fármaco potente pero costoso realmente les ayudará. Este estudio explora cómo los patrones en el ADN tumoral de un paciente, combinados con información clínica, pueden emplearse con técnicas modernas de aprendizaje automático para predecir quién es probable que se beneficie de un tratamiento dirigido común, bevacizumab, y quién no. En el futuro, estas herramientas podrían evitar que algunos pacientes sufran efectos secundarios y tratamientos ineficaces, al tiempo que orientan a otros hacia las opciones más prometedoras.
Una mirada más cercana al tratamiento del cáncer de colon
El cáncer colorrectal metastásico —cáncer de colon que se ha diseminado a otros órganos— es una de las principales causas de muerte por cáncer en todo el mundo. Muchos pacientes cuyos tumores presentan cambios genéticos específicos (mutaciones en RAS) reciben quimioterapia estándar combinada con bevacizumab, un fármaco que bloquea el crecimiento de vasos sanguíneos para “ahogar” a los tumores. Aunque esta combinación mejora la supervivencia en promedio, solo una fracción de los pacientes obtiene un beneficio significativo. Otros soportan meses de tratamiento, efectos secundarios y costes económicos con escasas ganancias. En la actualidad, los médicos no disponen de una prueba fiable para predecir de antemano quién no responderá a bevacizumab, lo que crea una necesidad urgente de mejores herramientas de decisión.
Integrando muchos tipos de datos
Los investigadores construyeron una canalización de análisis en varios pasos que utiliza aprendizaje automático para fusionar distintos tipos de información de cada paciente. Se basaron en una cohorte europea bien caracterizada llamada ANGIOPREDICT, que incluye a 117 personas con cáncer colorrectal metastásico tratadas con bevacizumab más quimioterapia. Para cada paciente contaban con: regiones del genoma que mostraban ganancias o pérdidas (alteraciones del número de copias), un pequeño conjunto de mutaciones génicas relevantes y datos clínicos estándar como edad, estadio tumoral y localización del tumor. A continuación, se empleó una herramienta especializada llamada PhenMap para descubrir patrones ocultos —llamados metavaribles— que resumen cómo varían conjuntamente estos cambios genéticos y las características clínicas entre los pacientes.
Encontrando la firma del ADN ligada al resultado
Entre los diez patrones identificados por PhenMap, dos se asociaron fuertemente con el tiempo que los pacientes vivieron sin empeoramiento de la enfermedad, una medida denominada supervivencia libre de progresión. El equipo se centró entonces en qué cambios genéticos específicos impulsaban estos dos patrones clave. Mediante pasos adicionales estadísticos y de aprendizaje automático, redujeron cientos de regiones genómicas y mutaciones a solo tres características: pérdidas en dos regiones cromosómicas (15q21.1 y 1p36.31) y la mutación en un gen llamado BRAF. Estas tres características formaron en conjunto una firma genética compacta que se asoció de forma estrecha con peores resultados en pacientes tratados con bevacizumab.
Convertir una firma en grupos de riesgo
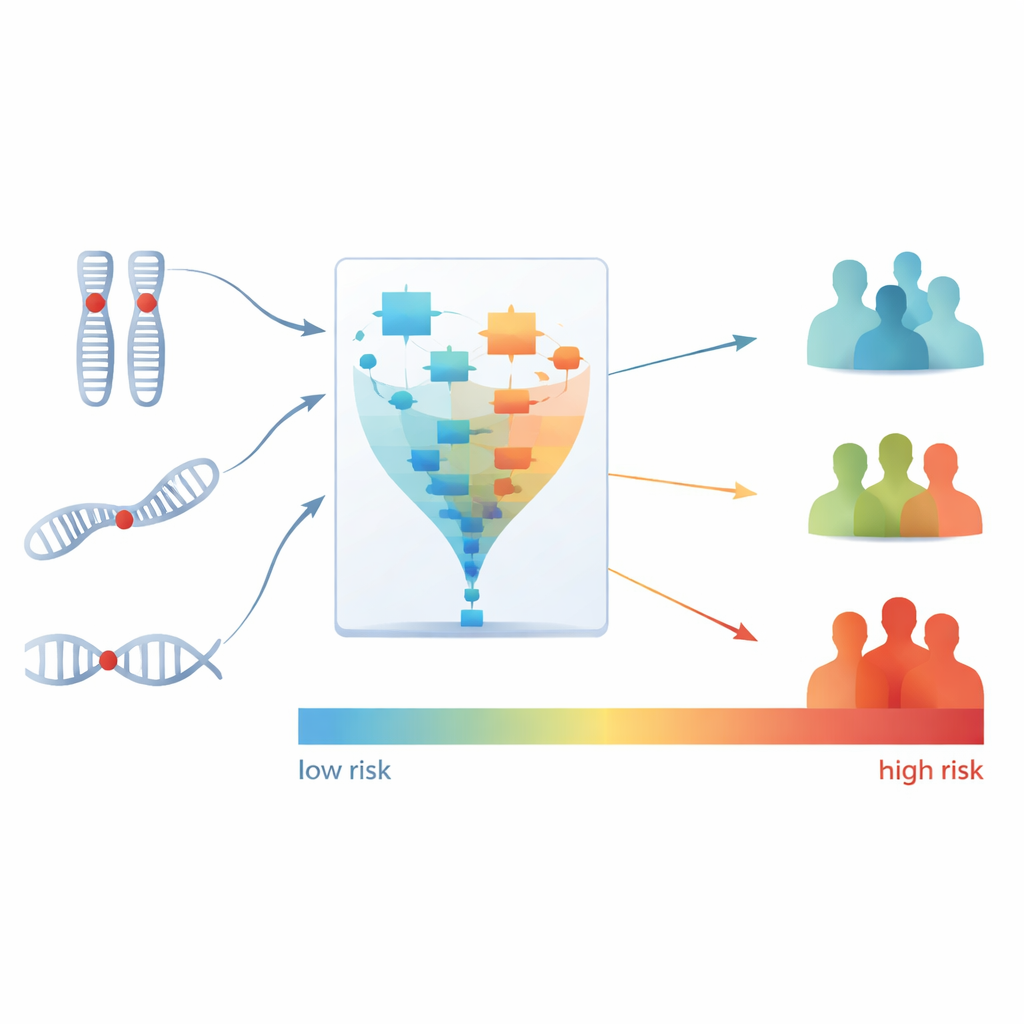
A continuación, los científicos convirtieron esta firma de tres elementos en una única puntuación de riesgo por paciente, que refleja el riesgo estimado de fallecimiento durante la terapia basada en bevacizumab. Luego dividieron a los pacientes en tres grupos —riesgo bajo, medio y alto— según sus puntuaciones. Las diferencias fueron llamativas: todos los pacientes del grupo de alto riesgo no respondieron a bevacizumab, mientras que la mayoría de los del grupo de bajo riesgo sí presentaron respuesta. El grupo de alto riesgo también mostró una probabilidad mucho mayor de progresión temprana de la enfermedad en comparación con el grupo de bajo riesgo. Es importante destacar que esta puntuación de riesgo ofreció información pronóstica más allá de lo que los médicos podían inferir ya a partir de factores clínicos estándar o de la subtipificación genómica previa.
Qué podría significar esto para los pacientes
Aunque este trabajo aún debe validarse en cohortes de pacientes más grandes e independientes, apunta hacia un futuro en el que datos tumorales y clínicos complejos puedan integrarse en una única puntuación de riesgo accionable. Si se confirma, una prueba sencilla que detecte la presencia de las dos pérdidas cromosómicas y la mutación BRAF podría ayudar a identificar a los pacientes con cáncer colorrectal metastásico que probablemente no se beneficien de la terapia combinada con bevacizumab. Esos pacientes podrían entonces dirigirse más pronto a estrategias alternativas o ensayos clínicos, mientras que otros seguirían recibiendo un fármaco del que tienen más probabilidades de beneficiarse. En términos más amplios, la canalización de aprendizaje automático demostrada aquí podría adaptarse a otros cánceres y tratamientos, avanzando hacia el objetivo de una atención oncológica verdaderamente personalizada.
Cita: Thomas, V., Nyamundanda, G., Lärkeryd, A. et al. A pipeline of machine learning-driven multi-modal data fusion methods for prognostic risk analysis in bevacizumab-treated metastatic colorectal cancer. Sci Rep 16, 8843 (2026). https://doi.org/10.1038/s41598-026-39189-w
Palabras clave: cáncer colorrectal metastásico, resistencia a bevacizumab, aprendizaje automático, biomarcadores genómicos, oncología de precisión