Clear Sky Science · sv
Fibroblaster kopplade till cancer reglerar utvecklingen av kolangiokarcinom via IL-6/STAT3/AKR1C3-signalaxeln
Varför tumörens omgivning spelar roll
Kolangiokarcinom, en cancer i gallgångarna i och runt levern, är ökänd för att vara svår att upptäcka tidigt och svårbehandlad när den väl upptäcks. Denna studie ställer en till synes enkel fråga med stora konsekvenser: hur hjälper den omkringliggande vävnaden tumörerna att växa, motstå cellgift och omprogrammera sin energianvändning? Genom att avslöja en nyckelkommunikationsväg mellan stödceller och cancerceller pekar forskarna ut en möjlig svag punkt som framtida terapier kan rikta in sig på.
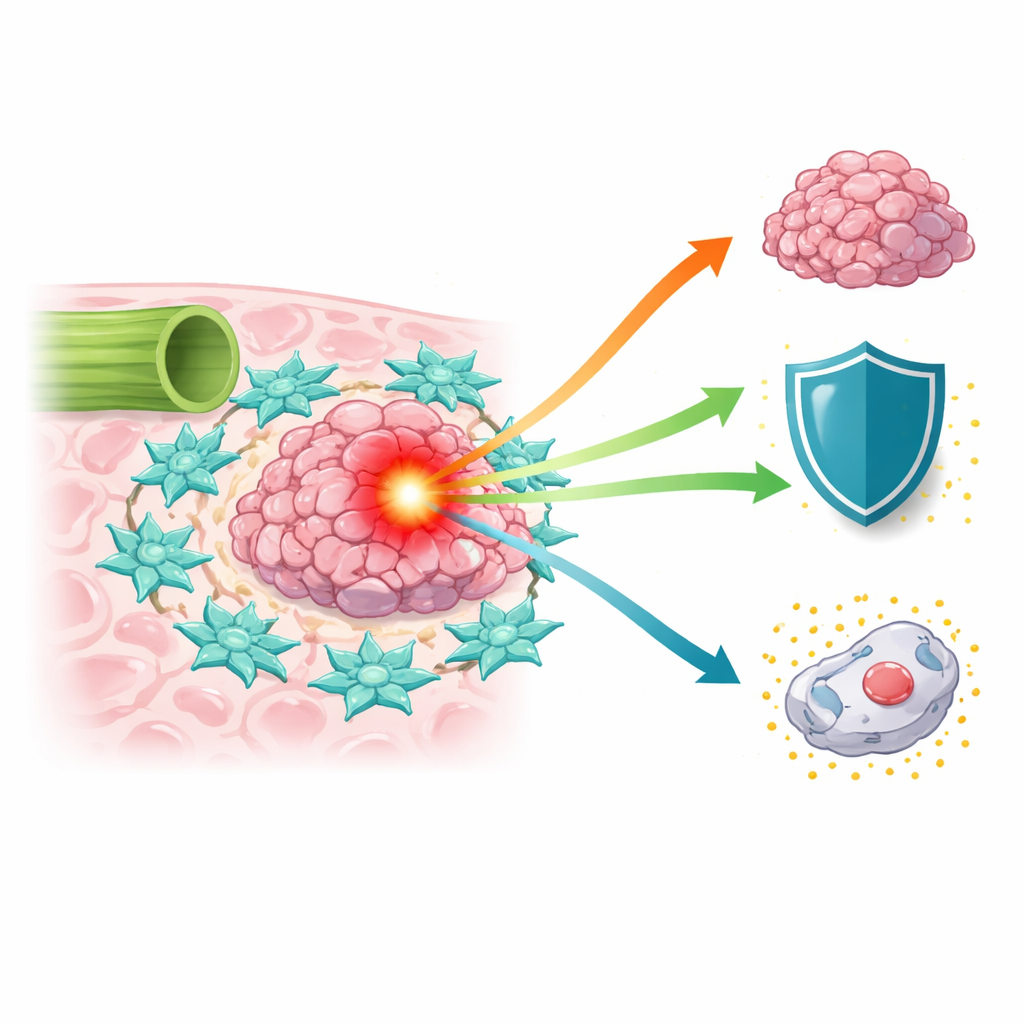
En svårbehandlad cancer som ökar
Gallgångscancer har ökat i världen under de senaste två decennierna, men patienterna får ofta dålig överlevnad eftersom tumörer upptäcks sent och full kirurgisk borttagning är utmanande. Standardkemoterapier, som 5-fluorouracil och platinumbaserade läkemedel, ger begränsad nytta. Forskare har insett att tumören inte bara är en klump maligna celler; den sitter i ett komplext mikroklimat av blodkärl, immunceller och bindvävsceller som antingen kan hämma eller stödja cancern. Bland dessa hjälpande celler framträder cancerassocierade fibroblaster—celler som normalt bygger upp och omformar vävnad—som kraftfulla medhjälpare som kan mata tumörer och dämpa behandlingseffekter.
En problematisk enzymaktivitet inne i tumörcellerna
Forskargruppen fokuserade på ett metaboliskt enzym kallat AKR1C3, tidigare kopplat till flera andra cancerformer men dåligt studerat i gallgångstumörer. Genom att analysera patientprover fann de att AKR1C3-nivåerna var mycket högre i kolangiokarcinomvävnad än i närliggande normala gallgångar. Patienter vars tumörer uttryckte detta protein starkt hade större tumörer, mer spridning till lymfkörtlar, mer avancerad sjukdomsstadium och kortare total överlevnad. I laboratoriedyrkade cancerceller gjorde ökad AKR1C3 att cellerna delade sig snabbare, bildade fler kolonier och stod emot kemoterapi bättre, medan minskad nivå bromsade tillväxten och gjorde läkemedlen mer effektiva. Dessa resultat tyder på att AKR1C3 inte bara är en passagerare utan en aktiv drivkraft för aggressivt beteende.
Driver tumörens aptit på socker
Cancerceller föredrar ofta en sockerhungrig strategi kallad aerob glykolys, där glukos förbränns snabbt även när syre finns tillgängligt. Denna metabola genväg stödjer snabb tillväxt och omformar den omgivande vävnaden. När forskarna minskade AKR1C3 i gallgångscancerceller upptog cellerna mindre glukos, släppte ut mindre laktat (en biprodukt av glykolys) och visade lägre mått på syrabildning och energiproduktion. Med andra ord hjälper AKR1C3 till att ställa om tumörmetabolismen mot detta högfrekventa, högkrävande läge. Utan det blev cancercellerna metabolt mindre aggressiva, vilket antyder att blockering av AKR1C3 både kan svälta tumörer och sakta deras tillväxt.
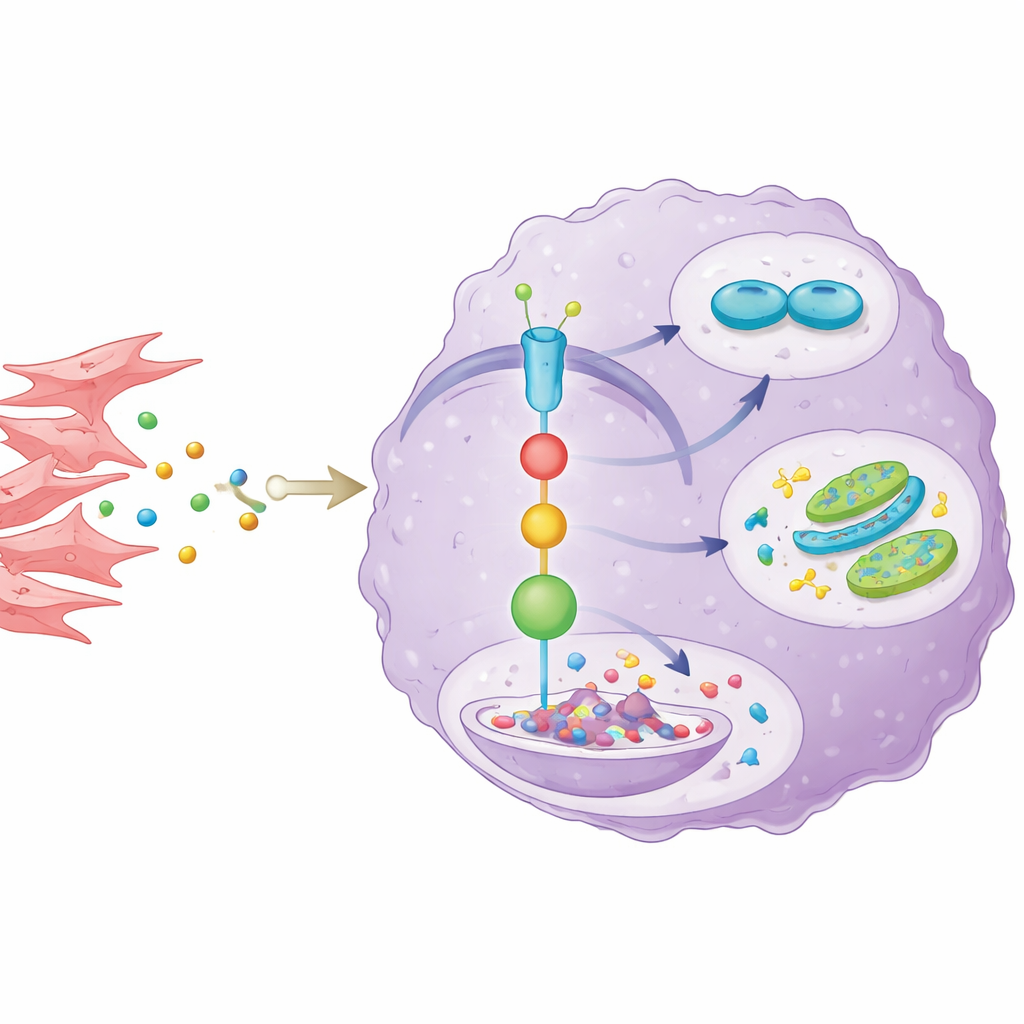
En signalkedja från stödceller till cancerceller
För att förstå hur tumörens grannar påverkar AKR1C3 isolerade forskarna cancerassocierade fibroblaster från patienttumörer och odlade dem tillsammans med kolangiokarcinomceller. Fibroblaster utsöndrade den inflammatoriska budbäraren IL-6, som aktiverade en välkänd kommunikationsväg inne i cancerceller kallad STAT3. Detta ökade i sin tur AKR1C3-nivåerna. När teamet blockerade IL-6 eller ett nyckelsteg i STAT3-signaleringen sjönk AKR1C3 och cancercellerna förlorade en del av sin tillväxtförmåga, läkemedelsresistens och sockerförbränningsfördelar. De upptäckte också en ytterligare twist: AKR1C3 störde SOCS1, en naturlig broms på STAT3, genom att främja dess nedbrytning. Detta bildade en självförstärkande loop där fibroblast-utsöndrat IL-6 slår på STAT3, STAT3 ökar AKR1C3 och AKR1C3 håller STAT3 aktiv genom att försvaga dess hämmare.
Från musemodeller till möjliga behandlingar
Berättelsen höll även i djurmodeller. När mänskliga gallgångscancerceller med minskat AKR1C3 implanterades i möss växte tumörerna långsammare. Att blanda dessa cancerceller med fibroblaster snabbade normalt på tumörtillväxten och gjorde dem svårare att behandla med kemoterapi. Men om AKR1C3 var nedreglerat i cancercellerna kunde inte fibroblasternas närvaro fullt ut återställa deras styrka, och tumörerna förblev mer känsliga för 5-fluorouracil. Tumörprover från dessa möss bekräftade lägre AKR1C3, svagare STAT3-aktivitet, färre tecken på celldelning och dämpade metabola markörer, vilket förstärker den centrala rollen för denna signalaxel i levande vävnad.
Vad detta betyder för patienter
Enkelt uttryckt visar denna forskning att vissa stödceller i gallgångstumörer skickar ett kemiskt budskap som slår på ett protein inne i cancercellerna, vilket gör att de växer snabbare, motstår kemoterapi och förbränner socker mer intensivt. Proteinet AKR1C3 hjälper också till att hålla budskapet igång genom att inaktivera en inbyggd säkerhetsbroms. På grund av dess starka koppling till dåliga utfall och dess centrala position i denna loop kan AKR1C3 bli både en markör för att identifiera högriskpatienter och ett mål för nya läkemedel. Medan kliniska tillämpningar kräver vidare prövningar, erbjuder störning av IL-6/STAT3/AKR1C3-vägen en lovande strategi för att försvaga gallgångscancer genom att angripa samspelet mellan tumörceller och deras omvårdande omgivning.
Citering: Huang, Tc., Feng, Wd., Fang, Gx. et al. Cancer-Associated fibroblasts regulate the development of cholangiocarcinoma through IL-6/STAT3/AKR1C3 signaling axis. Sci Rep 16, 10467 (2026). https://doi.org/10.1038/s41598-026-37583-y
Nyckelord: kolangiokarcinom, cancerassocierade fibroblaster, AKR1C3, IL-6 STAT3-signalering, tumörmetabolism