Clear Sky Science · nl
Kankergeliciteerde fibroblasten reguleren de ontwikkeling van cholangiocarcinoom via de IL-6/STAT3/AKR1C3-signaleringsas
Waarom de buurt rond een tumor ertoe doet
Cholangiocarcinoom, een kanker van de galwegen in en rond de lever, is berucht omdat het vroeg moeilijk te detecteren is en eenmaal vastgesteld lastig te behandelen is. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote gevolgen: hoe helpt het weefsel rond deze tumoren hen groeien, chemotherapie te weerstaan en hun energiegebruik te herprogrammeren? Door een belangrijke communicatieroute tussen ondersteunende cellen en kankercellen te ontrafelen, wijzen de onderzoekers op een nieuw zwak punt dat toekomstige therapieën kunnen benutten.
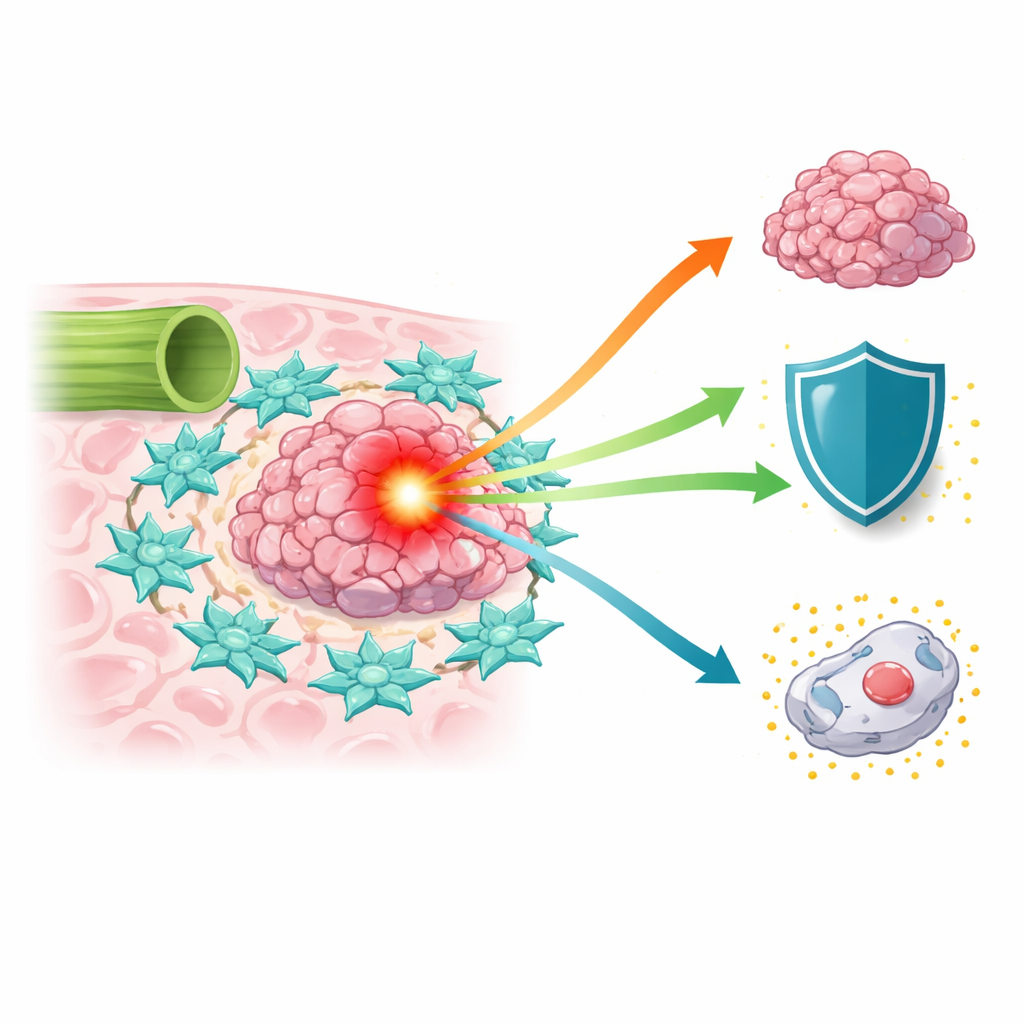
Een moeilijk te behandelen kanker die toeneemt
Galwegkanker neemt wereldwijd toe in de afgelopen twee decennia, maar patiënten hebben vaak een slechte overleving omdat tumoren laat worden ontdekt en volledige chirurgische verwijdering lastig is. Standaardchemotherapieën, zoals 5-fluorouracil en platina-gebaseerde middelen, bieden beperkte voordelen. Wetenschappers beseffen dat de tumor niet slechts een hoop kwaadaardige cellen is; ze zetelt in een complex “micro-omgeving” van bloedvaten, immuuncellen en bindweefselcellen die kanker kunnen remmen of juist ondersteunen. Onder deze helpers komen kankergeliciteerde fibroblasten—cellen die normaal weefsel opbouwen en herstructureren—naar voren als krachtige medeplichtigen die tumoren kunnen voeden en de effecten van behandeling kunnen verzachten.
Een lastige enzym in tumorcellen
Het team richtte zich op een metabolisch enzym genaamd AKR1C3, dat eerder aan verschillende andere kankers is gekoppeld maar weinig bestudeerd is in galwegtumoren. Bij analyse van patiëntmonsters vonden ze dat AKR1C3-niveaus veel hoger waren in cholangiocarcinoomweefsel dan in nabijgelegen normale galwegen. Patiënten waarvan de tumor sterk dit eiwit tot expressie bracht, hadden grotere tumoren, meer uitzaaiingen naar lymfeklieren, een gevorderdere ziekte en een kortere totale overleving. In in vitro gekweekte kankercellen zorgde het verhogen van AKR1C3 ervoor dat cellen sneller deelden, meer kolonies vormden en beter bestand waren tegen chemotherapie, terwijl het verlagen ervan de groei vertraagde en de medicijnen effectiever maakte. Deze resultaten suggereren dat AKR1C3 niet slechts een voorbijganger is, maar een actieve drijfveer van agressief gedrag.
Het voeden van de suikervretende neiging van kanker
Kankercellen geven vaak de voorkeur aan een suikhongerige strategie die aerobe glycolyse wordt genoemd, waarbij glucose snel wordt verbrand zelfs wanneer er voldoende zuurstof is. Deze metabole snelkoppeling ondersteunt snelle groei en herstructureert het omliggende weefsel. Toen de onderzoekers AKR1C3 in galwegkankercellen verminderden, namen de cellen minder glucose op, scheidden ze minder lactaat (een bijproduct van glycolyse) en lieten ze lagere waarden zien voor zuurproductie en energieopwekking. Met andere woorden: AKR1C3 helpt het tumormetabolisme af te stemmen op deze hogesnelheids-, hoge-vraagmodus. Zonder het werden de kankercellen metabolisch minder agressief, wat suggereert dat het blokkeren van AKR1C3 tumoren zowel zou kunnen uithongeren als hun groei zou vertragen.
Een signaalrelay van ondersteunende cellen naar kankercellen
Om te begrijpen hoe de buurttumorcellen AKR1C3 beïnvloeden, isoleerden de wetenschappers kankergeliciteerde fibroblasten uit patiënttumoren en kweekten ze samen met cholangiocarcinoomcellen. Fibroblasten scheidden de inflammatoire boodschapper IL-6 uit, die een bekende communicatieweg binnen kankercellen activeerde, de STAT3-route. Dit verhoogde op zijn beurt AKR1C3-niveaus. Toen het team IL-6 of een cruciale stap in de STAT3-signalisatie blokkeerde, daalde AKR1C3 en verloren de kankercellen een deel van hun groei-, medicijnresistentie- en suikerverbrandingsvoordelen. Ze ontdekten ook een verdere wending: AKR1C3 verstoorde SOCS1, een natuurlijke rem op STAT3, door de afbraak ervan te bevorderen. Dit vormde een zichzelf versterkende lus, waarin fibroblast-afgeleide IL-6 STAT3 inschakelt, STAT3 AKR1C3 verhoogt, en AKR1C3 STAT3 actief houdt door zijn remmer te verzwakken.
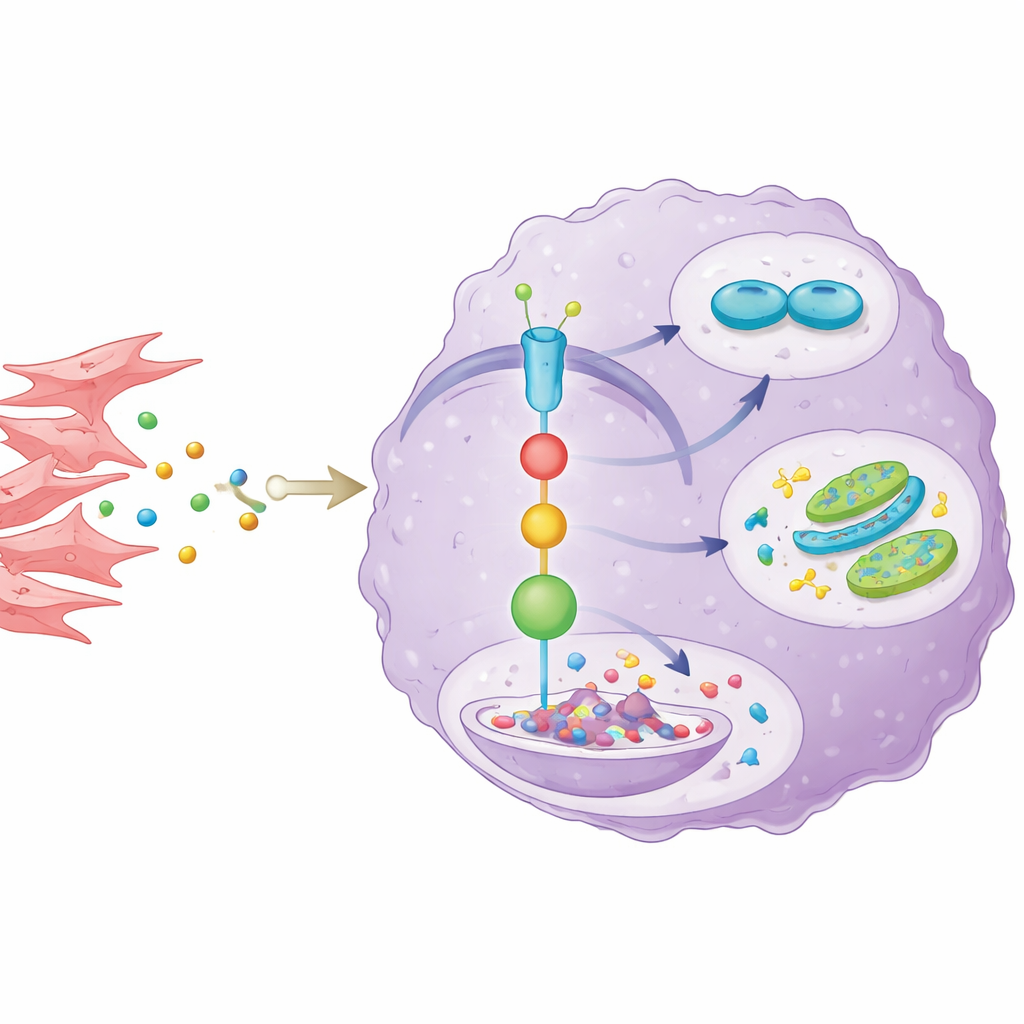
Van muismodellen naar mogelijke therapieën
Het verhaal hield ook stand in diermodellen. Wanneer menselijke galwegkankercellen met verminderd AKR1C3 in muizen werden geïmplanteerd, groeiden tumoren langzamer. Het mengen van deze kankercellen met fibroblasten versnelde normaal gesproken de tumorgroei en maakte ze moeilijker te behandelen met chemotherapie. Maar als AKR1C3 in de kankercellen was onderdrukt, kon zelfs de aanwezigheid van fibroblasten hun vitaliteit niet volledig herstellen, en bleven de tumoren gevoeliger voor 5-fluorouracil. Tumormonsters van deze muizen bevestigden lagere AKR1C3-waarden, zwakkere STAT3-activiteit, minder tekenen van celdeling en gedempte metabolische markers, waarmee de centrale rol van deze signaleringsas in levend weefsel werd versterkt.
Wat dit betekent voor patiënten
In eenvoudige woorden toont dit onderzoek aan dat bepaalde ondersteunende cellen in galwegtumoren een chemische boodschap uitzenden die een eiwit in kankercellen activeert, waardoor ze sneller groeien, chemotherapie weerstaan en suikers intensiever verbranden. Dat eiwit, AKR1C3, helpt ook om de boodschap gaande te houden door een ingebouwd veiligheidsmechanisme uit te schakelen. Vanwege de sterke koppeling met slechte uitkomsten en de centrale positie in deze lus, zou AKR1C3 zowel een merker kunnen worden om hoogrisicopatiënten te identificeren als een doelwit voor nieuwe geneesmiddelen. Hoewel klinische toepassing verdere tests vereist, biedt het verstoren van deze IL-6/STAT3/AKR1C3-route een veelbelovende strategie om galwegkankers te verzwakken door de communicatie tussen tumorcellen en hun verzorgende omgeving aan te vallen.
Bronvermelding: Huang, Tc., Feng, Wd., Fang, Gx. et al. Cancer-Associated fibroblasts regulate the development of cholangiocarcinoma through IL-6/STAT3/AKR1C3 signaling axis. Sci Rep 16, 10467 (2026). https://doi.org/10.1038/s41598-026-37583-y
Trefwoorden: cholangiocarcinoom, kankergeliciteerde fibroblasten, AKR1C3, IL-6 STAT3 signalering, tumormetabolisme