Clear Sky Science · it
I fibroblasti associati al cancro regolano lo sviluppo del colangiocarcinoma attraverso l’asse di segnalazione IL-6/STAT3/AKR1C3
Perché il vicinato del tumore conta
Il colangiocarcinoma, un cancro delle vie biliari nel fegato e nelle aree circostanti, è notoriamente difficile da rilevare precocemente e complesso da trattare una volta diagnosticato. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: in che modo il tessuto che circonda questi tumori ne favorisce la crescita, la resistenza alla chemioterapia e la riorganizzazione del metabolismo energetico? Svelando una via di comunicazione chiave tra le cellule di supporto e le cellule tumorali, i ricercatori indicano un nuovo punto debole che terapie future potrebbero sfruttare.
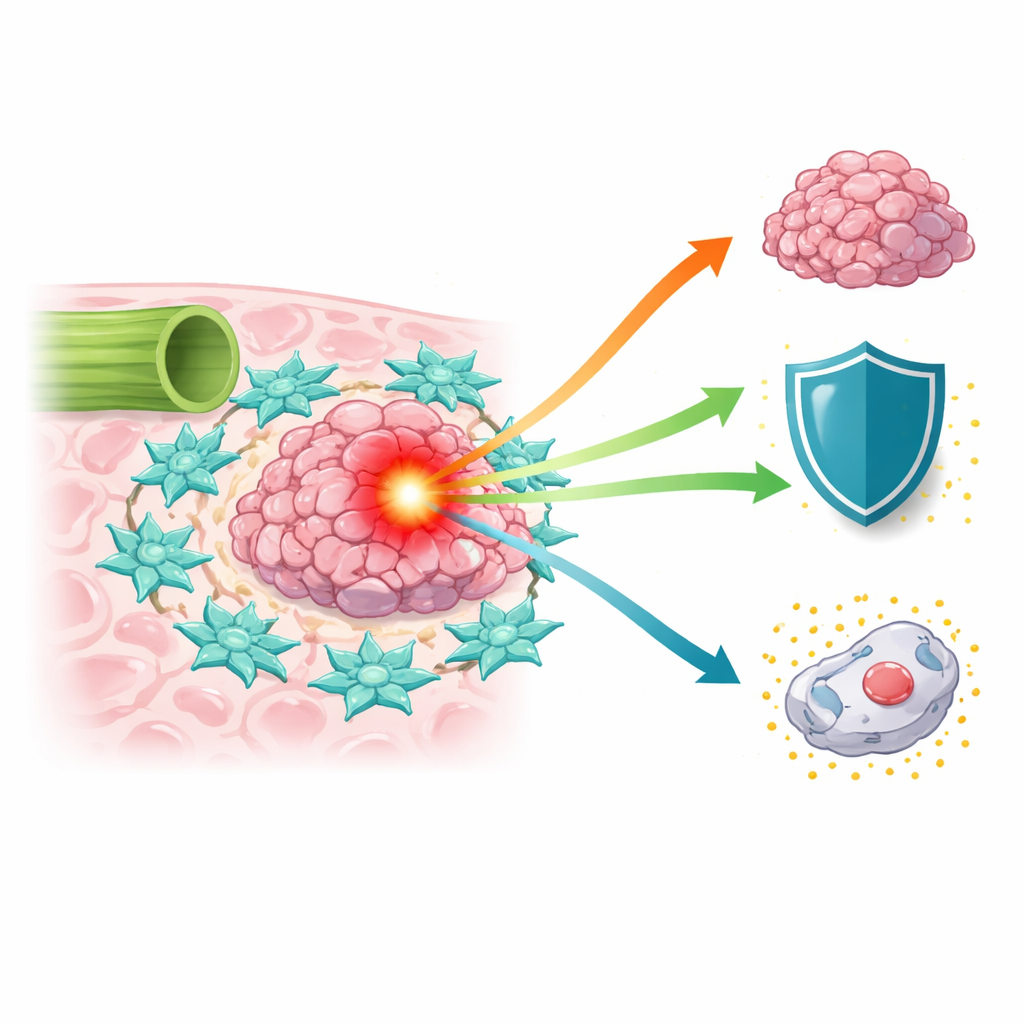
Un cancro difficile da trattare in aumento
Il cancro delle vie biliari è in aumento in tutto il mondo negli ultimi due decenni, eppure i pazienti spesso affrontano una prognosi sfavorevole perché i tumori vengono scoperti tardi e la rimozione chirurgica completa è complicata. I farmaci chemioterapici standard, come 5-fluorouracile e agenti a base di platino, offrono benefici limitati. Gli scienziati hanno compreso che il tumore non è solo un ammasso di cellule maligne; si trova all’interno di un complesso "microambiente" di vasi sanguigni, cellule immunitarie e cellule del tessuto connettivo che possono sia limitare sia sostenere il cancro. Tra questi alleati, i fibroblasti associati al cancro — cellule che normalmente costruiscono e rimodellano il tessuto — emergono come potenti complici in grado di nutrire i tumori e attenuare gli effetti del trattamento.
Un enzima problematico all’interno delle cellule tumorali
Il gruppo si è concentrato su un enzima metabolico chiamato AKR1C3, precedentemente collegato a diversi altri tumori ma poco studiato nei tumori delle vie biliari. Analizzando campioni di pazienti, hanno riscontrato livelli di AKR1C3 molto più elevati nel tessuto di colangiocarcinoma rispetto ai dotti biliari normali adiacenti. I pazienti i cui tumori esprimevano fortemente questa proteina avevano neoplasie più grandi, maggiore diffusione ai linfonodi, malattia più avanzata e sopravvivenza globale più breve. In cellule tumorali coltivate in laboratorio, l’aumento di AKR1C3 ha reso le cellule più rapide a dividersi, a formare colonie e più resistenti alla chemioterapia, mentre la sua riduzione ha rallentato la crescita e reso i farmaci più efficaci. Questi risultati suggeriscono che AKR1C3 non è un semplice spettatore ma un motore attivo del comportamento aggressivo.
Alimentare l’appetito di zucchero del cancro
Le cellule tumorali spesso preferiscono una strategia a base di zucchero chiamata glicolisi aerobica, consumando glucosio rapidamente anche quando l’ossigeno è abbondante. Questa scorciatoia metabolica sostiene la crescita rapida e rimodella il tessuto circostante. Quando i ricercatori hanno ridotto AKR1C3 nelle cellule di colangiocarcinoma, queste hanno assorbito meno glucosio, rilasciato meno lattato (un prodotto della glicolisi) e mostrato misure inferiori di produzione di acidi ed energia. In altre parole, AKR1C3 contribuisce a rimodulare il metabolismo tumorale verso questa modalità ad alta velocità e alta richiesta. Senza di esso, le cellule cancerose diventano meno aggressive dal punto di vista metabolico, suggerendo che bloccare AKR1C3 potrebbe sia "affamare" i tumori sia rallentarne la crescita.
Una catena di segnali dalle cellule di supporto alle cellule tumorali
Per capire come i vicini del tumore influenzino AKR1C3, gli scienziati hanno isolato fibroblasti associati al cancro da tumori di pazienti e li hanno coltivati insieme a cellule di colangiocarcinoma. I fibroblasti secretono il messaggero infiammatorio IL-6, che attiva una nota via di comunicazione all’interno delle cellule tumorali chiamata via STAT3. Ciò, a sua volta, aumenta i livelli di AKR1C3. Quando il gruppo ha bloccato l’IL-6 o un passaggio chiave della segnalazione STAT3, AKR1C3 è diminuito e le cellule tumorali hanno perso parte della loro crescita, resistenza ai farmaci e vantaggi nella combustione degli zuccheri. Hanno anche scoperto un ulteriore elemento: AKR1C3 interferisce con SOCS1, un freno naturale su STAT3, promuovendone la degradazione. Questo forma un circuito di rinforzo, in cui l’IL-6 derivato dai fibroblasti attiva STAT3, STAT3 aumenta AKR1C3 e AKR1C3 mantiene STAT3 attivo indebolendo il suo inibitore.
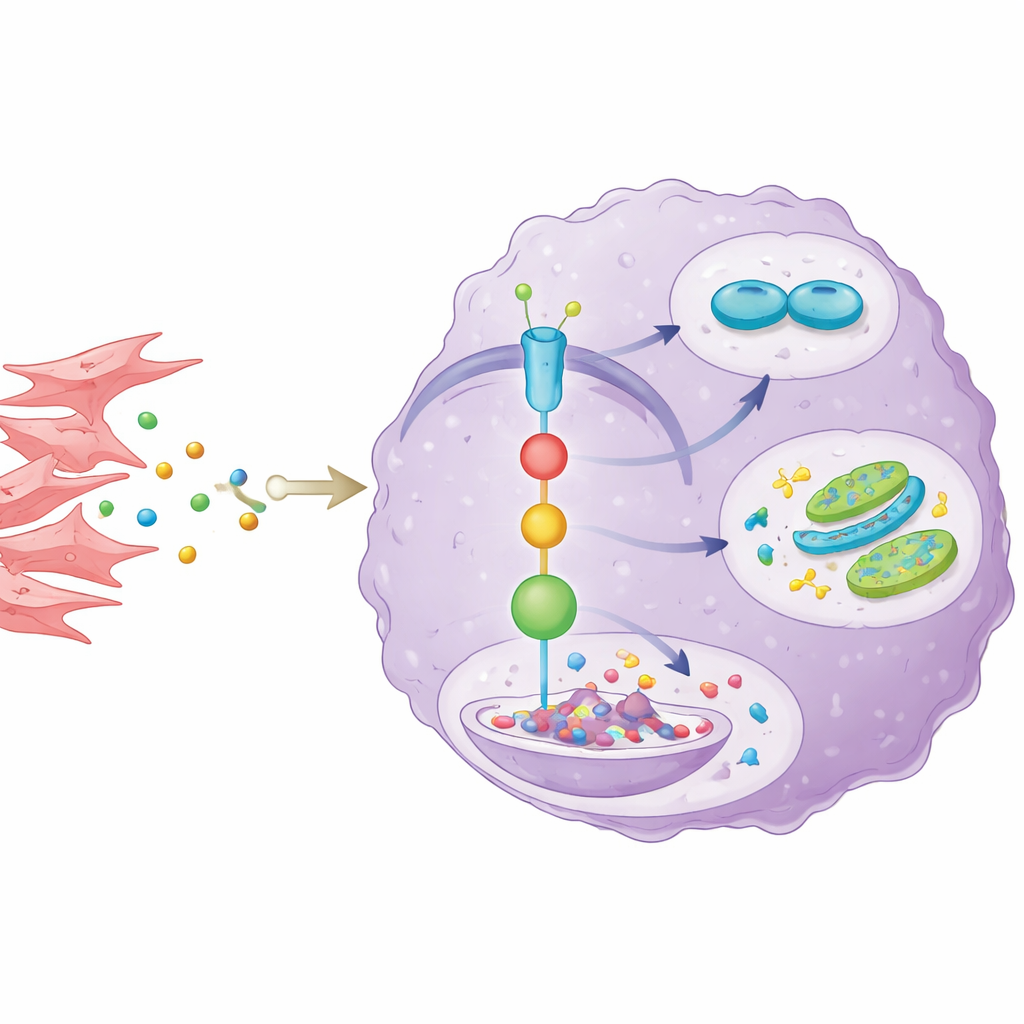
Da modelli murini a possibili terapie
La storia è stata confermata anche in modelli animali. Quando cellule umane di colangiocarcinoma con AKR1C3 ridotto sono state impiantate in topi, i tumori sono cresciuti più lentamente. Mescolare queste cellule tumorali con fibroblasti normalmente accelerava la crescita tumorale e le rendeva più difficili da trattare con la chemioterapia. Tuttavia, se AKR1C3 era silenziato nelle cellule tumorali, anche la presenza dei fibroblasti non riusciva a ripristinarne completamente la vitalità, e i tumori rimanevano più sensibili al 5-fluorouracile. I campioni tumorali di questi topi hanno confermato livelli più bassi di AKR1C3, una minore attività di STAT3, segnali ridotti di divisione cellulare e marcatori metabolici attenuati, rafforzando il ruolo centrale di questo asse di segnalazione nei tessuti viventi.
Cosa significa per i pazienti
In termini semplici, questa ricerca mostra che alcune cellule di supporto nei tumori delle vie biliari inviano un messaggio chimico che attiva una proteina nelle cellule tumorali, rendendole più rapide a crescere, più resistenti alla chemioterapia e più intense nel consumo di zucchero. Quella proteina, AKR1C3, aiuta anche a mantenere attivo il messaggio disabilitando un interruttore di sicurezza interno. Per il suo forte legame con esiti sfavorevoli e la sua posizione centrale in questo circuito, AKR1C3 potrebbe diventare sia un marcatore per identificare pazienti ad alto rischio sia un bersaglio per nuovi farmaci. Sebbene le applicazioni cliniche richiedano ulteriori verifiche, interrompere questa via IL-6/STAT3/AKR1C3 offre una strategia promettente per indebolire i tumori delle vie biliari attaccando la comunicazione tra le cellule tumorali e il loro ambiente di sostegno.
Citazione: Huang, Tc., Feng, Wd., Fang, Gx. et al. Cancer-Associated fibroblasts regulate the development of cholangiocarcinoma through IL-6/STAT3/AKR1C3 signaling axis. Sci Rep 16, 10467 (2026). https://doi.org/10.1038/s41598-026-37583-y
Parole chiave: colangiocarcinoma, fibroblasti associati al cancro, AKR1C3, segnalazione IL-6 STAT3, metabolismo tumorale