Clear Sky Science · pl
Fibroblasty związane z rakiem regulują rozwój chłoniaka dróg żółciowych poprzez oś sygnalizacyjną IL-6/STAT3/AKR1C3
Dlaczego sąsiedztwo guza ma znaczenie
Chłoniak dróg żółciowych, nowotwór przewodów żółciowych w obrębie i wokół wątroby, jest wyjątkowo trudny do wykrycia we wczesnym stadium i trudny do leczenia po rozpoznaniu. To badanie stawia pozornie proste pytanie o duże konsekwencje: w jaki sposób tkanka otaczająca te guzy pomaga im rosnąć, opierać się chemioterapii i przebudowywać wykorzystanie energii? Odkrycie kluczowej drogi komunikacji między komórkami podporowymi a komórkami nowotworowymi wskazuje nowe słabe ogniwo, które mogą wykorzystać przyszłe terapie.
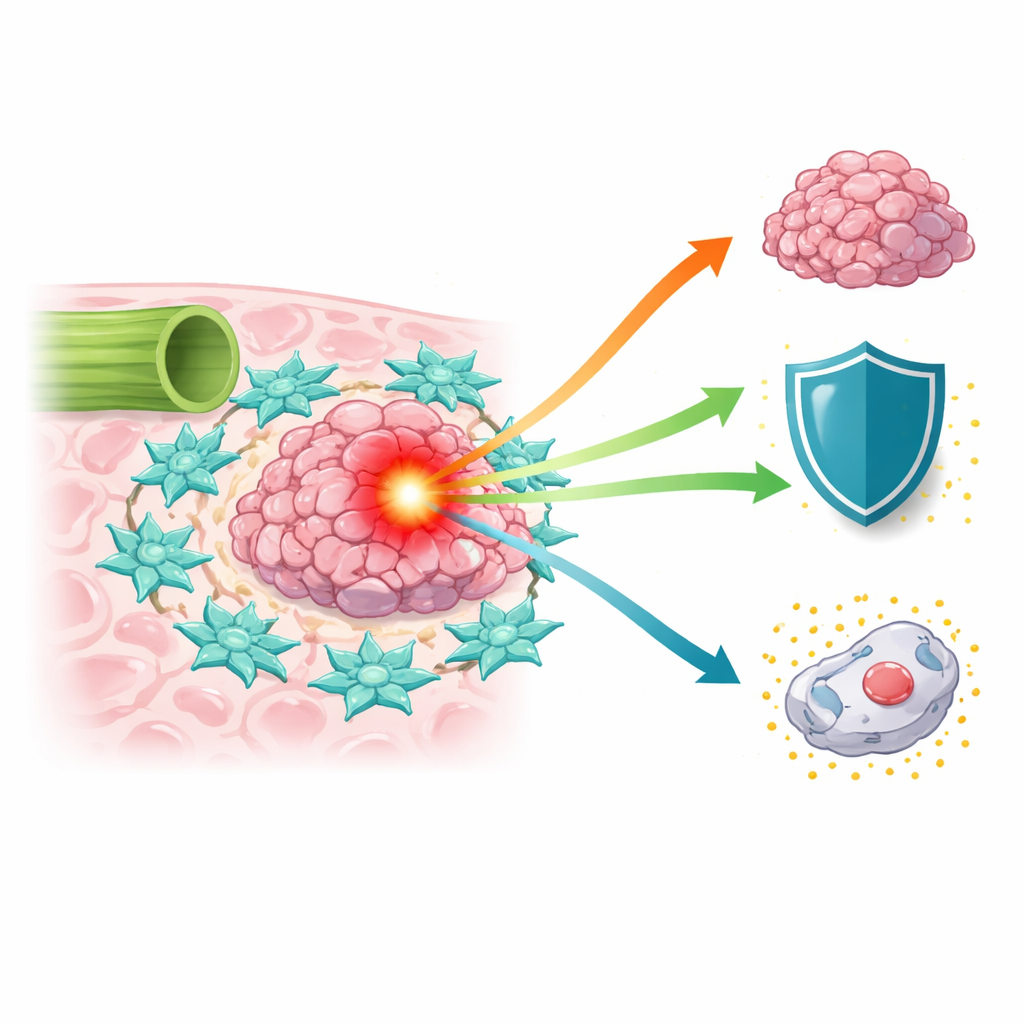
Trudny w leczeniu nowotwór w natarciu
Rak przewodów żółciowych narasta na całym świecie w ciągu ostatnich dwóch dekad, a pacjenci często mają złe rokowania, ponieważ guzy wykrywane są późno, a ich całkowite usunięcie chirurgiczne jest trudne. Standardowe leki chemioterapeutyczne, takie jak 5-fluorouracyl i środki oparte na platynie, przynoszą ograniczone korzyści. Naukowcy zrozumieli, że guz to nie tylko skupisko komórek złośliwych; znajduje się on w złożonym „mikrośrodowisku” naczyń krwionośnych, komórek układu odpornościowego i komórek tkanki łącznej, które mogą hamować lub wspierać raka. Wśród tych wspomagaczy fibroblasty związane z rakiem — komórki, które normalnie budują i przebudowują tkankę — wyłaniają się jako potężni współsprawcy, mogący odżywiać guzy i osłabiać skutki leczenia.
Sprawczy enzym w komórkach guza
Zespół skupił się na enzymie metabolicznym o nazwie AKR1C3, wcześniej powiązanym z kilkoma innymi nowotworami, ale słabo zbadanym w rakach przewodów żółciowych. Analiza próbek od pacjentów wykazała, że poziomy AKR1C3 były znacznie wyższe w tkance chłoniaka niż w sąsiednich prawidłowych przewodach żółciowych. Pacjenci, których guzy silnie eksprymowały ten białko, mieli większe nowotwory, więcej przerzutów do węzłów chłonnych, bardziej zaawansowane stadia choroby i krótsze całkowite przeżycie. W hodowlach komórkowych zwiększenie AKR1C3 powodowało szybszy podział komórek, tworzenie większej liczby kolonii i lepszą odporność na chemioterapię, podczas gdy jego zmniejszenie spowalniało wzrost i zwiększało skuteczność leków. Wyniki te sugerują, że AKR1C3 nie jest jedynie pasażerem, lecz aktywnym sprawcą agresywnego zachowania.
Nawożenie apetytu raka na glukozę
Komórki nowotworowe często preferują strategię głodną cukru zwaną glikolizą tlenową, spalając glukozę szybko, nawet gdy dostępny jest tlen. Ten metaboliczny skrót wspiera szybki wzrost i przekształca otaczającą tkankę. Gdy badacze zmniejszyli poziom AKR1C3 w komórkach raka przewodów żółciowych, komórki pobierały mniej glukozy, wydzielały mniej mleczanu (produkty uboczny glikolizy) i wykazywały niższe wskaźniki produkcji kwaśności i generowania energii. Innymi słowy, AKR1C3 pomaga przestroić metabolizm guza w kierunku tego szybkiego, wysoce wymagającego trybu. Bez niego komórki nowotworowe stały się metabolicznie mniej agresywne, co sugeruje, że blokada AKR1C3 mogłaby głodzić guzy, a także spowalniać ich wzrost.
Przekaźnik sygnału od komórek podporowych do nowotworowych
Aby zrozumieć, jak sąsiedztwo guza wpływa na AKR1C3, naukowcy wyizolowali fibroblasty związane z rakiem z próbek pacjentów i hodowali je razem z komórkami chłoniaka przewodów żółciowych. Fibroblasty wydzielały zapalny mediator IL-6, który aktywował dobrze poznaną drogę komunikacji wewnątrz komórek nowotworowych zwaną szlakiem STAT3. To z kolei podnosiło poziomy AKR1C3. Gdy zespół zablokował IL-6 lub kluczowy etap w sygnalizacji STAT3, AKR1C3 spadł, a komórki nowotworowe straciły część swojej zdolności do wzrostu, oporności na leki i przewagi w spalaniu cukru. Odkryli też kolejny zwrot akcji: AKR1C3 zakłócał działanie SOCS1, naturalnego hamulca STAT3, promując jego rozkład. Powstała pętla samowzmacniająca — IL-6 pochodzące z fibroblastów włącza STAT3, STAT3 zwiększa AKR1C3, a AKR1C3 utrzymuje STAT3 aktywny przez osłabianie jego inhibitorów.
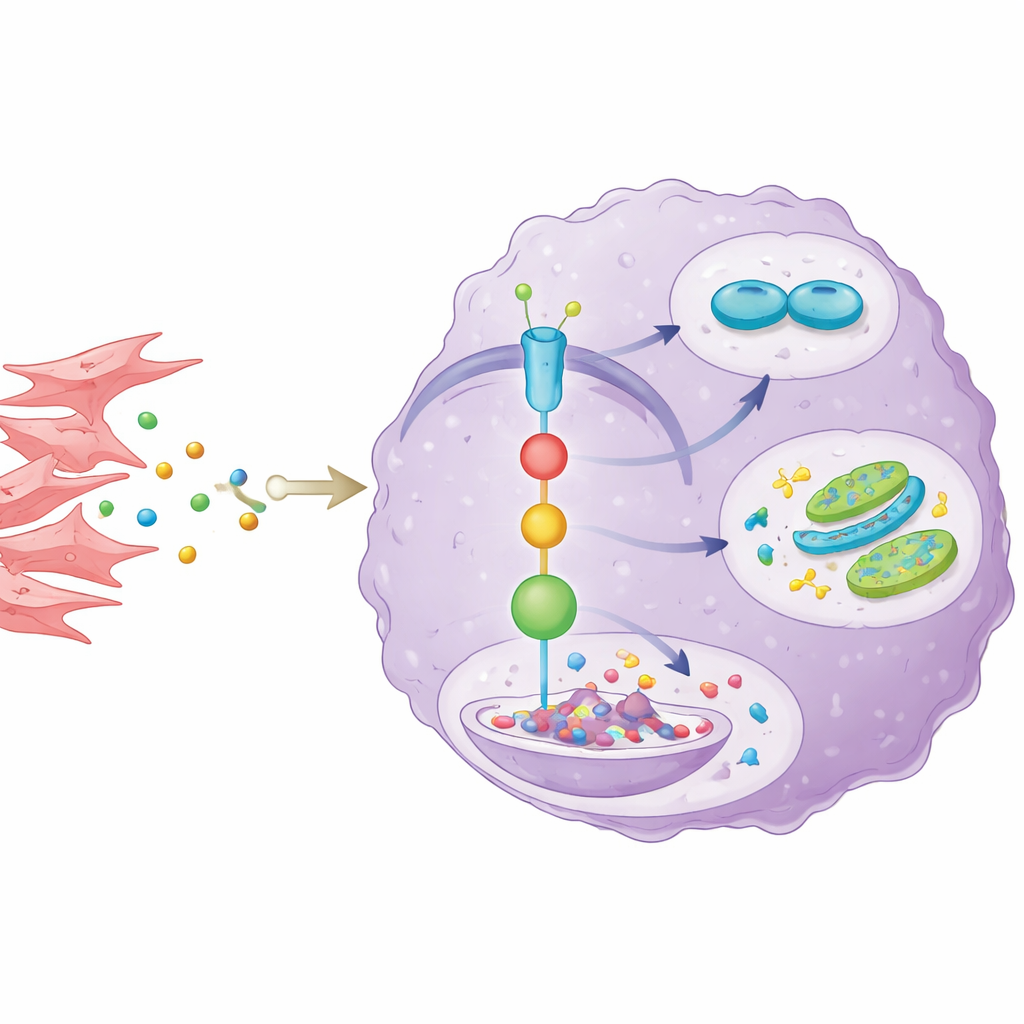
Od modeli mysich do potencjalnych terapii
Opowieść potwierdziła się w modelach zwierzęcych. Gdy ludzkie komórki raka przewodów żółciowych z obniżonym AKR1C3 wszczepiano myszom, guzy rosły wolniej. Mieszanie tych komórek nowotworowych z fibroblastami zwykle przyspieszało wzrost guza i utrudniało leczenie chemioterapią. Jednak jeśli AKR1C3 został wyciszony w komórkach nowotworowych, nawet obecność fibroblastów nie była w stanie w pełni przywrócić ich witalności, a guzy pozostały bardziej wrażliwe na 5-fluorouracyl. Próbki guzów od tych myszy potwierdziły niższe poziomy AKR1C3, słabszą aktywność STAT3, mniej oznak podziału komórek i osłabione markery metaboliczne, wzmacniając centralną rolę tej osi sygnalizacyjnej w tkance żywej.
Co to znaczy dla pacjentów
Mówiąc prosto, te badania pokazują, że pewne komórki podporowe w guzach przewodów żółciowych wysyłają chemiczny sygnał, który włącza białko w komórkach nowotworowych, powodując, że rosną szybciej, opierają się chemioterapii i intensywniej spalają cukier. To białko, AKR1C3, pomaga też utrzymać przepływ sygnału, dezaktywując wbudowany wyłącznik bezpieczeństwa. Ze względu na silne powiązanie ze złymi wynikami i centralne miejsce w tej pętli, AKR1C3 może stać się zarówno markerem pomagającym identyfikować pacjentów wysokiego ryzyka, jak i celem nowych leków. Choć zastosowania kliniczne będą wymagać dalszych badań, przerwanie tej ścieżki IL-6/STAT3/AKR1C3 oferuje obiecującą strategię osłabienia raków przewodów żółciowych przez atak na dialog między komórkami guza a ich opiekuńczym sąsiedztwem.
Cytowanie: Huang, Tc., Feng, Wd., Fang, Gx. et al. Cancer-Associated fibroblasts regulate the development of cholangiocarcinoma through IL-6/STAT3/AKR1C3 signaling axis. Sci Rep 16, 10467 (2026). https://doi.org/10.1038/s41598-026-37583-y
Słowa kluczowe: chłoniak dróg żółciowych, fibroblasty związane z rakiem, AKR1C3, sygnalizacja IL-6 STAT3, metabolizm guza