Clear Sky Science · pt
Fibroblastos associados ao câncer regulam o desenvolvimento do colangiocarcinoma por meio do eixo de sinalização IL-6/STAT3/AKR1C3
Por que o entorno do tumor importa
O colangiocarcinoma, um câncer dos ductos biliares dentro e ao redor do fígado, é notoriamente difícil de detectar precocemente e complicado de tratar uma vez diagnosticado. Este estudo faz uma pergunta aparentemente simples, mas de grande impacto: como o tecido que envolve esses tumores os ajuda a crescer, resistir à quimioterapia e reprogramar seu uso de energia? Ao descobrir uma via de comunicação chave entre as células de suporte e as células tumorais, os pesquisadores apontam para uma nova vulnerabilidade que terapias futuras poderiam explorar.
Um câncer de difícil tratamento em ascensão
O câncer dos ductos biliares tem aumentado em todo o mundo nas últimas duas décadas, e ainda assim os pacientes frequentemente enfrentam desfechos ruins porque os tumores são descobertos tardiamente e a remoção cirúrgica completa é desafiadora. Drogas quimioterápicas padrão, como 5-fluorouracil e agentes à base de platina, oferecem benefício limitado. Cientistas perceberam que o tumor não é apenas um amontoado de células malignas; ele está inserido em um complexo “microambiente” de vasos sanguíneos, células imunes e células do tecido conjuntivo que podem tanto conter quanto apoiar o câncer. Entre esses colaboradores, os fibroblastos associados ao câncer — células que normalmente constroem e remodelam o tecido — emergem como cúmplices poderosos que podem nutrir os tumores e atenuar os efeitos do tratamento.
Uma enzima problemática dentro das células tumorais
A equipe concentrou-se em uma enzima metabólica chamada AKR1C3, previamente ligada a vários outros cânceres, mas pouco estudada em tumores dos ductos biliares. Ao analisar amostras de pacientes, eles encontraram níveis muito mais altos de AKR1C3 no tecido de colangiocarcinoma do que nos ductos biliares normais adjacentes. Pacientes cujos tumores expressavam fortemente essa proteína apresentaram cânceres maiores, maior acometimento dos linfonodos, doença em estágio mais avançado e sobrevivência global mais curta. Em células cancerosas cultivadas em laboratório, aumentar a expressão de AKR1C3 fez as células dividiram-se mais rápido, formar mais colônias e resistir melhor à quimioterapia, enquanto reduzi-la desacelerou o crescimento e tornou os medicamentos mais eficazes. Esses resultados sugerem que a AKR1C3 não é apenas uma acompanhante, mas um motor ativo do comportamento agressivo.
Alimentando o apetite do câncer por glicose
As células cancerosas frequentemente favorecem uma estratégia gulosa por açúcar chamada glicólise aeróbica, queimando glicose rapidamente mesmo quando há oxigênio disponível. Esse atalho metabólico sustenta o crescimento rápido e remodela o tecido ao redor. Quando os pesquisadores reduziram AKR1C3 em células de câncer de ducto biliar, as células captaram menos glicose, liberaram menos lactato (um subproduto da glicólise) e mostraram menores indicadores de produção de ácido e geração de energia. Em outras palavras, a AKR1C3 ajuda a reorientar o metabolismo tumoral para esse modo de alta velocidade e alta demanda. Sem ela, as células cancerosas tornaram-se metabolicamente menos agressivas, sugerindo que bloquear a AKR1C3 poderia tanto “desnutrir” os tumores quanto frear seu crescimento.
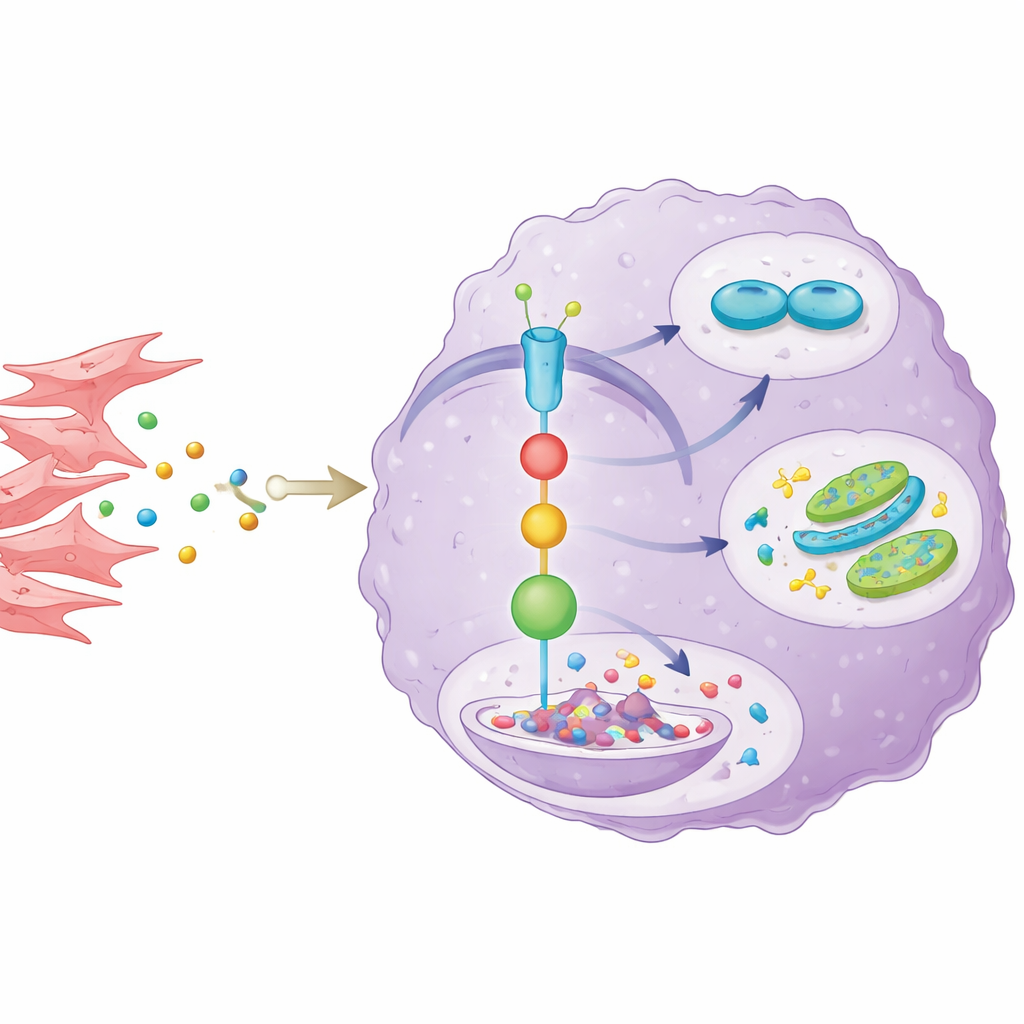
Um repasse de sinal das células de suporte para as células tumorais
Para entender como os vizinhos do tumor influenciam a AKR1C3, os cientistas isolaram fibroblastos associados ao câncer de tumores de pacientes e os cultivaram com células de colangiocarcinoma. Os fibroblastos secretaram o mensageiro inflamatório IL-6, que ativou uma via de comunicação bem conhecida dentro das células cancerosas chamada via STAT3. Isso, por sua vez, elevou os níveis de AKR1C3. Quando a equipe bloqueou o IL-6 ou um passo chave na sinalização do STAT3, a AKR1C3 caiu e as células tumorais perderam parte de seu crescimento, resistência aos medicamentos e vantagens na queima de glicose. Eles também descobriram uma reviravolta adicional: a AKR1C3 interferia com a SOCS1, um freio natural do STAT3, promovendo sua degradação. Isso formou um ciclo auto-reforçador, em que o IL-6 derivado de fibroblastos ativa o STAT3, o STAT3 aumenta a AKR1C3, e a AKR1C3 mantém o STAT3 ativo enfraquecendo seu inibidor.
De modelos em camundongos a possíveis terapias
A história se confirmou em modelos animais. Quando células humanas de câncer dos ductos biliares com AKR1C3 reduzida foram implantadas em camundongos, os tumores cresceram mais lentamente. Misturar essas células cancerosas com fibroblastos normalmente acelerava o crescimento tumoral e tornava-os mais difíceis de tratar com quimioterapia. Ainda assim, se a AKR1C3 fosse suprimida nas células tumorais, mesmo a presença dos fibroblastos não conseguia restaurar totalmente seu vigor, e os tumores permaneceram mais sensíveis ao 5-fluorouracil. Amostras tumorais desses camundongos confirmaram níveis menores de AKR1C3, atividade mais fraca do STAT3, menos sinais de divisão celular e marcadores metabólicos atenuados, reforçando o papel central desse eixo de sinalização em tecido vivo.
O que isso significa para os pacientes
Em termos simples, esta pesquisa mostra que certas células de suporte em tumores dos ductos biliares enviam uma mensagem química que liga uma proteína dentro das células tumorais, fazendo-as crescer mais rápido, resistir à quimioterapia e queimar açúcar com mais intensidade. Essa proteína, AKR1C3, também ajuda a manter a mensagem ativa ao desativar um interruptor de segurança interno. Por causa de sua forte ligação com desfechos ruins e de sua posição central nesse circuito, a AKR1C3 pode se tornar tanto um marcador para identificar pacientes de alto risco quanto um alvo para novas drogas. Embora aplicações clínicas exijam testes adicionais, interromper essa via IL-6/STAT3/AKR1C3 oferece uma estratégia promissora para enfraquecer os cânceres dos ductos biliares atacando a conversa entre as células tumorais e seu entorno nutridor.
Citação: Huang, Tc., Feng, Wd., Fang, Gx. et al. Cancer-Associated fibroblasts regulate the development of cholangiocarcinoma through IL-6/STAT3/AKR1C3 signaling axis. Sci Rep 16, 10467 (2026). https://doi.org/10.1038/s41598-026-37583-y
Palavras-chave: colangiocarcinoma, fibroblastos associados ao câncer, AKR1C3, sinalização IL-6 STAT3, metabolismo tumoral