Clear Sky Science · es
Los fibroblastos asociados al cáncer regulan el desarrollo del colangiocarcinoma a través del eje de señalización IL-6/STAT3/AKR1C3
Por qué importa el vecindario del tumor
El colangiocarcinoma, un cáncer de los conductos biliares dentro y alrededor del hígado, es notoriamente difícil de detectar en fases tempranas y complejo de tratar una vez diagnosticado. Este estudio plantea una pregunta aparentemente sencilla pero de grandes implicaciones: ¿cómo el tejido que rodea a estos tumores les ayuda a crecer, a resistir la quimioterapia y a reconfigurar su uso de la energía? Al desvelar una vía clave de comunicación entre las células de sostén y las células cancerosas, los investigadores señalan una nueva vulnerabilidad que futuras terapias podrían aprovechar.
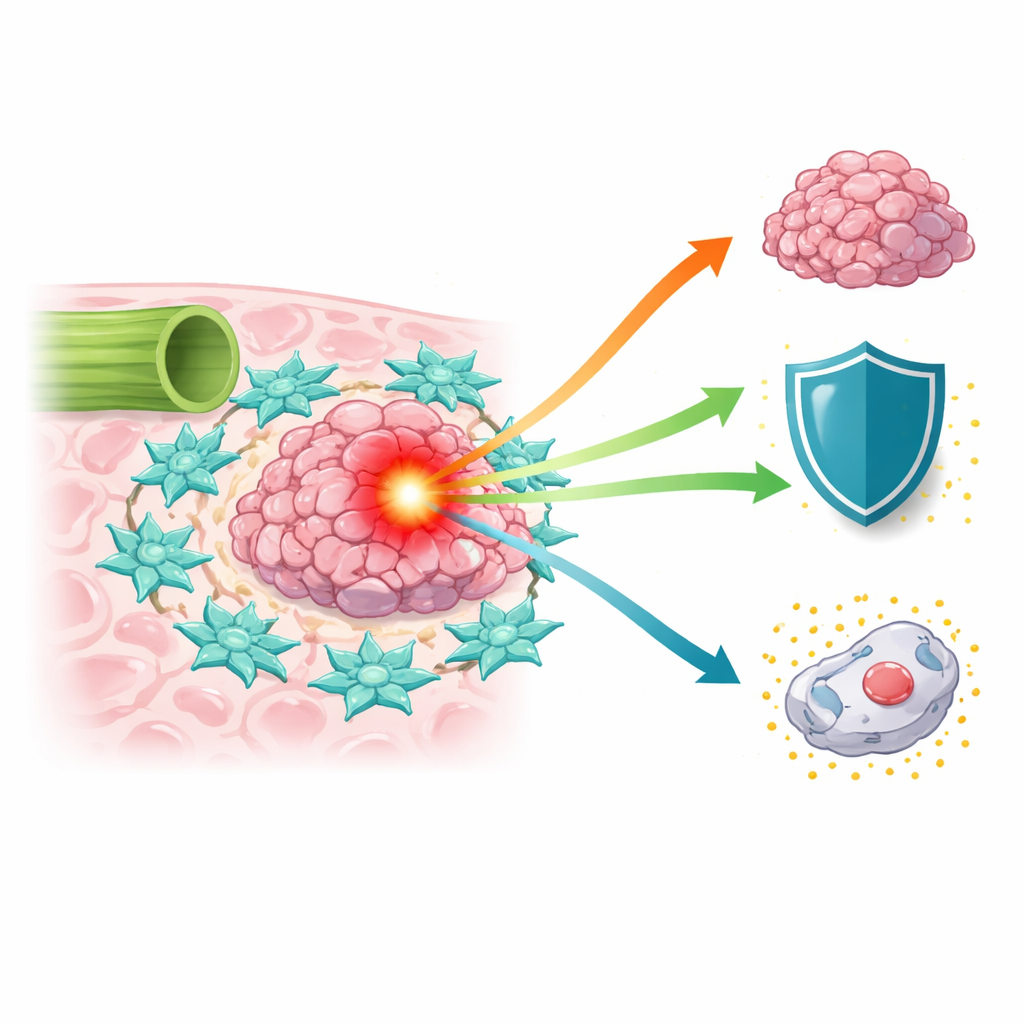
Un cáncer difícil de tratar en aumento
El cáncer de conductos biliares ha ido en aumento en todo el mundo durante las últimas dos décadas; aun así, los pacientes suelen enfrentarse a una supervivencia baja porque los tumores se detectan tarde y la extirpación quirúrgica completa es complicada. Los fármacos de quimioterapia estándar, como el 5-fluorouracilo y los agentes basados en platino, ofrecen un beneficio limitado. Los científicos han comprendido que el tumor no es solo un grupo de células malignas; se halla en un “microambiente” complejo de vasos sanguíneos, células inmunitarias y células del tejido conectivo que pueden frenar o apoyar al cáncer. Entre estos colaboradores, los fibroblastos asociados al cáncer —células que normalmente construyen y remodelan el tejido— emergen como cómplices poderosos que pueden alimentar a los tumores y atenuar los efectos del tratamiento.
Una enzima problemática dentro de las células tumorales
El equipo se centró en una enzima metabólica llamada AKR1C3, ligada previamente a varios otros cánceres pero poco estudiada en tumores de los conductos biliares. Al analizar muestras de pacientes, hallaron que los niveles de AKR1C3 eran mucho más altos en tejido de colangiocarcinoma que en conductos biliares normales cercanos. Los pacientes cuyos tumores expresaban fuertemente esta proteína tenían cánceres más grandes, mayor afectación de ganglios linfáticos, enfermedad en estadio más avanzado y una supervivencia global más corta. En células cancerosas cultivadas en laboratorio, aumentar AKR1C3 hizo que las células se dividieran más rápido, formaran más colonias y resistieran mejor la quimioterapia, mientras que reducirla ralentizaba el crecimiento y hacía los fármacos más efectivos. Estos resultados sugieren que AKR1C3 no es solo un pasajero, sino un impulsor activo del comportamiento agresivo.
Alimentando el apetito de azúcar del cáncer
Las células cancerosas con frecuencia favorecen una estrategia glucosa-dependiente llamada glucólisis aeróbica, quemando glucosa rápidamente incluso cuando el oxígeno es abundante. Este atajo metabólico sostiene un crecimiento rápido y remodela el tejido circundante. Cuando los investigadores redujeron AKR1C3 en células de cáncer de conductos biliares, las células absorbieron menos glucosa, liberaron menos lactato (un subproducto de la glucólisis) y mostraron menores indicadores de producción de ácido y generación de energía. En otras palabras, AKR1C3 ayuda a reorientar el metabolismo tumoral hacia este modo de alta velocidad y alta demanda. Sin él, las células cancerosas se volvieron metabólicamente menos agresivas, lo que sugiere que bloquear AKR1C3 podría tanto privar de combustible a los tumores como frenar su crecimiento.
Un relevo de señal desde las células de sostén a las células cancerosas
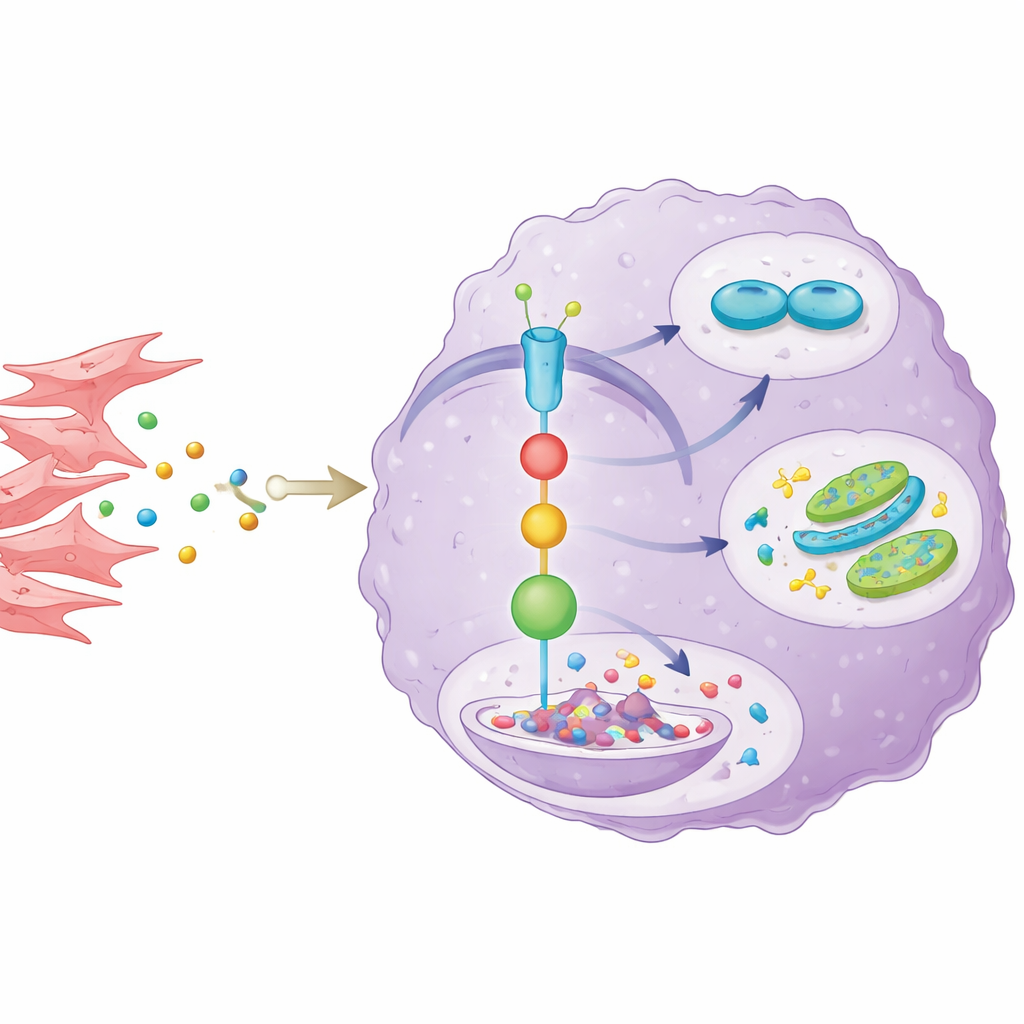
Para entender cómo los vecinos del tumor influyen en AKR1C3, los científicos aislaron fibroblastos asociados al cáncer de tumores de pacientes y los cultivaron junto con células de colangiocarcinoma. Los fibroblastos secretaron el mensajero inflamatorio IL-6, que activó una conocida vía de comunicación dentro de las células cancerosas llamada vía STAT3. Esto, a su vez, elevó los niveles de AKR1C3. Cuando el equipo bloqueó IL-6 o un paso clave en la señalización de STAT3, AKR1C3 disminuyó y las células cancerosas perdieron parte de su crecimiento, resistencia a fármacos y ventajas en la quema de azúcar. También desvelaron un giro adicional: AKR1C3 interfería con SOCS1, un freno natural sobre STAT3, promoviendo su degradación. Esto formó un bucle autorreforzante, en el que la IL-6 derivada de fibroblastos activa STAT3, STAT3 aumenta AKR1C3, y AKR1C3 mantiene a STAT3 activo debilitando a su inhibidor.
De modelos en ratones a posibles terapias
La historia se confirmó en modelos animales. Cuando células humanas de cáncer de conductos biliares con AKR1C3 reducido se implantaron en ratones, los tumores crecieron más despacio. Mezclar estas células cancerosas con fibroblastos aceleraba normalmente el crecimiento tumoral y los hacía más difíciles de tratar con quimioterapia. Sin embargo, si AKR1C3 estaba silenciado en las células cancerosas, incluso la presencia de fibroblastos no pudo restaurar por completo su vigor, y los tumores siguieron siendo más sensibles al 5-fluorouracilo. Las muestras tumorales de estos ratones confirmaron niveles más bajos de AKR1C3, una actividad de STAT3 más débil, menos señales de división celular y marcadores metabólicos atenuados, reforzando el papel central de este eje de señalización en tejido vivo.
Qué significa esto para los pacientes
En términos sencillos, esta investigación muestra que ciertas células de apoyo en los tumores de conductos biliares envían un mensaje químico que activa una proteína dentro de las células cancerosas, haciéndolas crecer más rápido, resistir la quimioterapia y quemar azúcar con mayor intensidad. Esa proteína, AKR1C3, también ayuda a mantener el mensaje activo al desactivar un interruptor de seguridad interno. Debido a su fuerte vínculo con peores resultados y su posición central en este bucle, AKR1C3 podría convertirse tanto en un marcador para identificar a pacientes de alto riesgo como en un objetivo para nuevos fármacos. Aunque las aplicaciones clínicas requerirán más ensayos, interrumpir esta vía IL-6/STAT3/AKR1C3 ofrece una estrategia prometedora para debilitar los cánceres de conductos biliares atacando la comunicación entre las células tumorales y su vecindario nutridor.
Cita: Huang, Tc., Feng, Wd., Fang, Gx. et al. Cancer-Associated fibroblasts regulate the development of cholangiocarcinoma through IL-6/STAT3/AKR1C3 signaling axis. Sci Rep 16, 10467 (2026). https://doi.org/10.1038/s41598-026-37583-y
Palabras clave: colangiocarcinoma, fibroblastos asociados al cáncer, AKR1C3, señalización IL-6 STAT3, metabolismo tumoral