Clear Sky Science · ar
الخلايا الليفية المرتبطة بالسرطان تنظم تطور سرطان القنوات الصفراوية عبر محور إشاري IL-6/STAT3/AKR1C3
لماذا يهم جوار الورم
سرطان القنوات الصفراوية، وهو سرطان يصيب القنوات الصفراوية داخل الكبد وحوله، يصعب اكتشافه مبكراً ويصعب علاجه بمجرد اكتشافه. تطرح هذه الدراسة سؤالاً يبدو بسيطاً لكنه ذو تداعيات كبيرة: كيف يساعد النسيج المحيط بهذه الأورام على نموها، ومقاومتها للعلاج الكيميائي، وإعادة برمجة استخدام الطاقة؟ من خلال كشف مسار تواصل رئيسي بين خلايا الدعم وخلايا السرطان، يشير الباحثون إلى نقطة ضعف جديدة يمكن أن تستهدفها العلاجات المستقبلية.
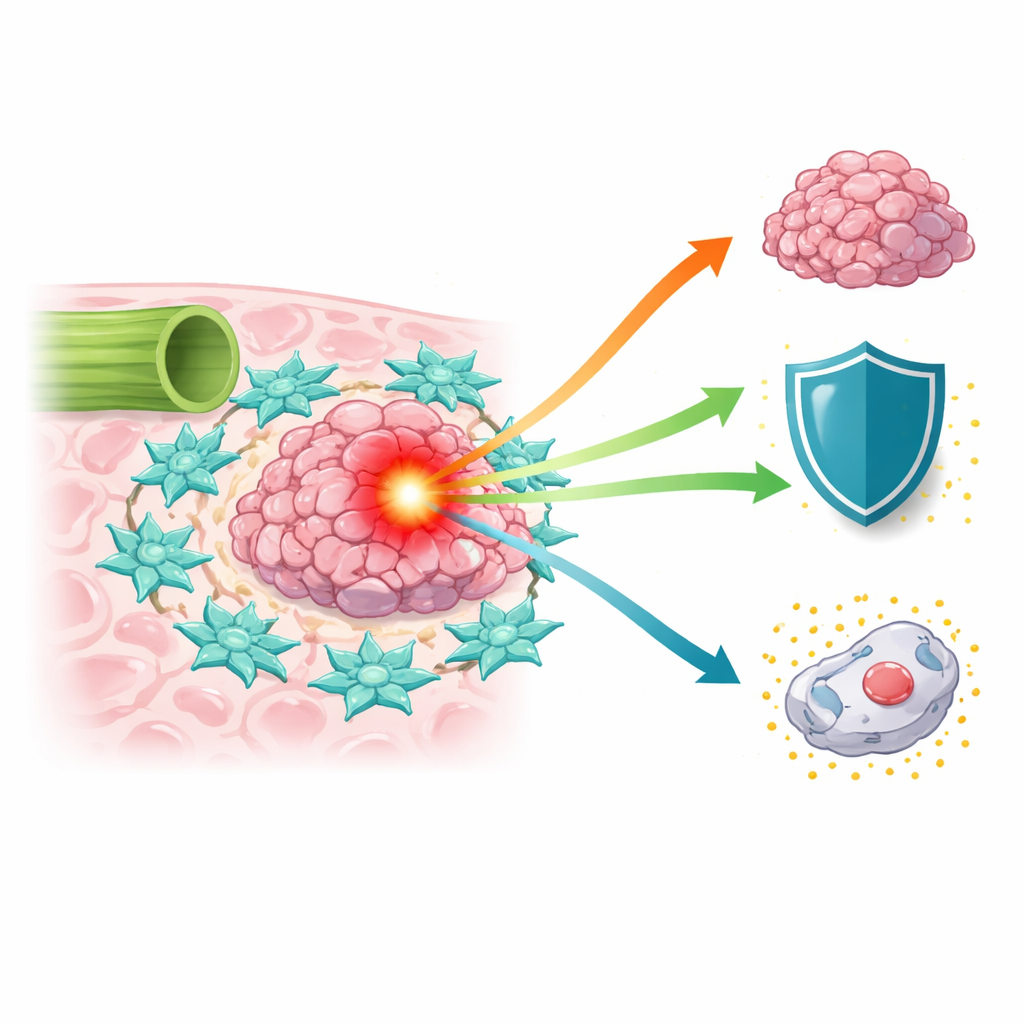
سرطان يصعب علاجه يتزايد انتشاره
زاد انتشار سرطان القنوات الصفراوية عالمياً خلال العقدين الماضيين، ومع ذلك يواجه المرضى غالباً نتائج بقاء ضعيفة لأن الأورام تكتشف في مراحل متأخرة ويصعب إزالتها جراحياً بالكامل. توفر أدوية العلاج الكيميائي القياسية، مثل 5-فلورويوراسيل والعوامل المحتوية على البلاتين، فوائد محدودة. أدرك العلماء أن الورم ليس مجرد كتلة من الخلايا الخبيثة؛ بل يوجد داخل «البيئة الميكروية» المعقدة من الأوعية الدموية والخلايا المناعية وخلايا النسيج الضام التي يمكن أن تكبح السرطان أو تدعمه. من بين هؤلاء المساعدين، تظهر الخلايا الليفية المرتبطة بالسرطان—وهي خلايا تبني النسيج وتعيد تشكيله عادة—كمتواطئين أقوياء يمكنهم تغذية الأورام وتقليل تأثيرات العلاج.
إنزيم يسبب المشاكل داخل خلايا الورم
ركز الفريق على إنزيم أيضي يُدعى AKR1C3، المرتبط سابقاً بعدة سرطانات أخرى لكنه لم يُدرس جيداً في أورام القنوات الصفراوية. من خلال تحليل عينات المرضى، وجدوا أن مستويات AKR1C3 كانت أعلى بكثير في نسيج سرطان القنوات الصفراوية مقارنة بالقنوات الصفراوية السليمة المجاورة. كان المرضى الذين أعربت أورامهم عن هذا البروتين بقوة يعانون من أورام أكبر، وانتشار أكبر في العقد اللمفاوية، ومرحلة متقدمة من المرض، وبقاء عام أقصر. في خلايا سرطانية نمت مختبرياً، جعل زيادة AKR1C3 الخلايا تنقسم أسرع، وتكوّن مستعمرات أكثر، وتتحمل العلاج الكيميائي بشكل أفضل، بينما أدى تخفيضه إلى إبطاء النمو وجعل الأدوية أكثر فعالية. توحي هذه النتائج أن AKR1C3 ليس مجرد راكب بل دافع نشط للسلوك العدواني.
تغذية شهية السرطان للسكر
غالباً ما تفضل خلايا السرطان استراتيجية جائعة للسكر تُسمى التحلل السكري الهوائي، تحرق فيها الجلوكوز بسرعة حتى عندما يتوفر الأكسجين. هذا الاختصار الأيضي يدعم النمو السريع ويعيد تشكيل النسيج المحيط. عندما خفّض الباحثون مستوى AKR1C3 في خلايا سرطان القنوات الصفراوية، قلّت كمية الجلوكوز الممتصة، وانخفض إفراز اللاكتات (ناتج جانبي للتحلل السكري)، وظهرت مقاييس أقل لإنتاج الحمض وتوليد الطاقة. بعبارة أخرى، يساعد AKR1C3 في إعادة ضبط أيض الورم باتجاه هذا النمط عالي السرعة والطلب. من دونه أصبحت خلايا السرطان أقل عدوانية من الناحية الأيضية، مما يوحي بأن حجب AKR1C3 قد يجوع الأورام بالإضافة إلى إبطاء نموها.
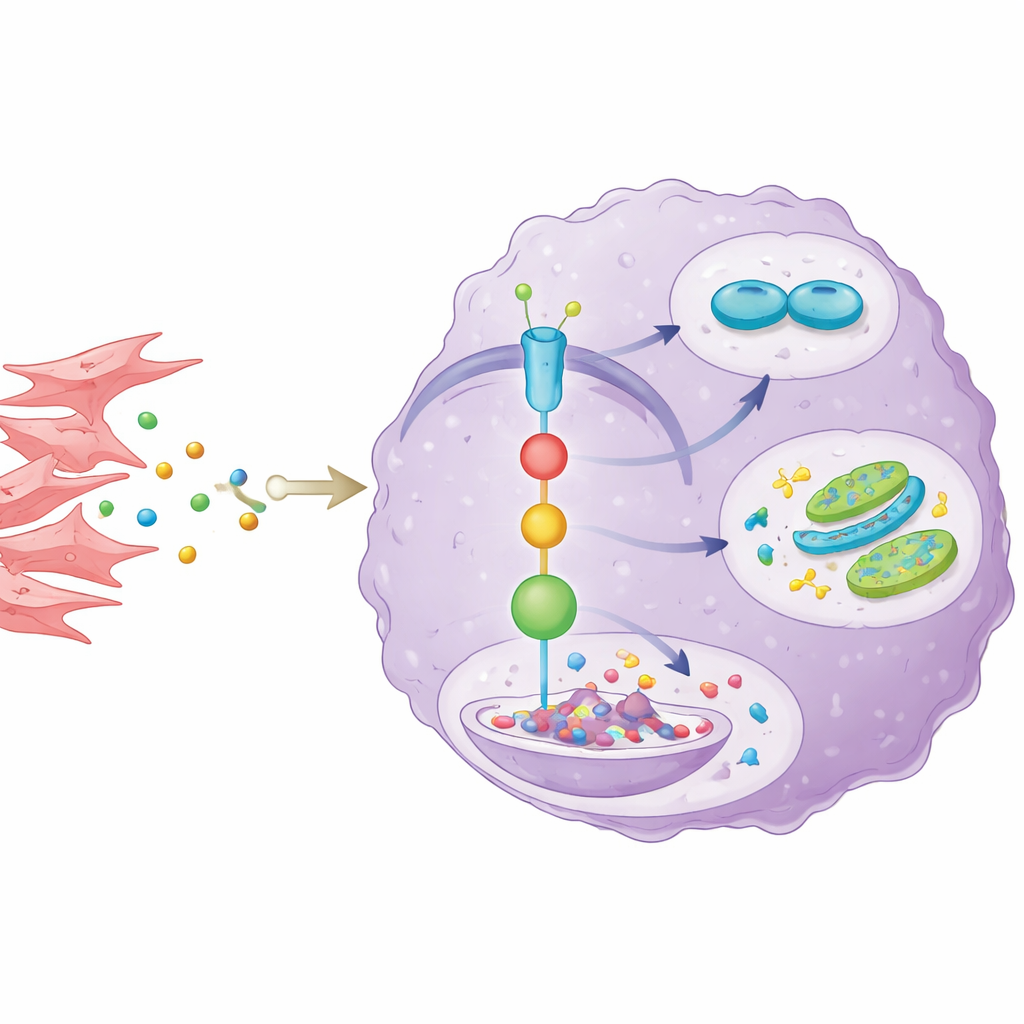
تتابع إشاراتي من خلايا الدعم إلى خلايا السرطان
لفهم كيف يؤثر جيران الورم على AKR1C3، عزّل العلماء الخلايا الليفية المرتبطة بالسرطان من أورام المرضى ونموّوها مع خلايا سرطان القنوات الصفراوية. أفرزت الخلايا الليفية المرسِل الالتهابي IL-6، الذي فعّل مسار تواصل معروف داخل خلايا السرطان يُدعى STAT3. هذا بدوره رفع مستويات AKR1C3. عندما حجب الفريق IL-6 أو خطوة رئيسية في إشارات STAT3، انخفض AKR1C3 وخسرت خلايا السرطان بعضاً من مزاياها في النمو، ومقاومة الدواء، واحتراق السكر. كما اكتشفوا لفة إضافية: تعارض AKR1C3 مع SOCS1، الفرامل الطبيعية على STAT3، عن طريق تعزيز تحللها. شكّل ذلك حلقة معززة ذاتياً، حيث يشغّل IL-6 القادم من الخلايا الليفية STAT3، ويعزز STAT3 AKR1C3، ويحافظ AKR1C3 على نشاط STAT3 من خلال إضعاف مثبطه.
من نماذج الفئران إلى علاجات محتملة
ثبتت صحة القصة في نماذج حيوانية. عندما زُرع في الفئران خلايا بشرية لسرطان القنوات الصفراوية مع انخفاض AKR1C3، نمت الأورام ببطء أكبر. كان خلط هذه الخلايا السرطانية مع خلايا ليفية يسرّع نمو الأورام عادة ويجعلها أصعب في العلاج بالعلاج الكيميائي. ومع ذلك، إذا تم خفض AKR1C3 في خلايا السرطان، حتى وجود الخلايا الليفية لم يستعد حيويتها بالكامل، وبقيت الأورام أكثر حساسية للـ5-فلورويوراسيل. أكدت عينات الأورام من هذه الفئران انخفاض AKR1C3، وضعف نشاط STAT3، وقلة علامات انقسام الخلايا، وتراجع العلامات الأيضية، مما يعزّز الدور المركزي لهذا المحور الإشاري في الأنسجة الحية.
ماذا يعني هذا للمرضى
بعبارة بسيطة، تُظهر هذه الأبحاث أن خلايا دعم معينة في أورام القنوات الصفراوية ترسل رسالة كيميائية تُشغّل بروتيناً داخل خلايا السرطان، مما يجعلها تنمو أسرع، وتقاوم العلاج الكيميائي، وتحرق السكر بشدة أكبر. يساعد هذا البروتين، AKR1C3، أيضاً في الحفاظ على استمرار الرسالة من خلال تعطيل مفتاح أمان داخلي. وبسبب ارتباطه القوي بالنتائج السيئة وموقعه المركزي في هذه الحلقة، قد يصبح AKR1C3 علامة لتحديد المرضى ذوي المخاطر العالية وهدفاً لأدوية جديدة. رغم أن التطبيقات السريرية ستتطلب مزيداً من الاختبارات، فإن تعطيل مسار IL-6/STAT3/AKR1C3 يقدم استراتيجية واعدة لإضعاف سرطانات القنوات الصفراوية بمهاجمة التواصُل بين خلايا الورم وجوارها الراعي.
الاستشهاد: Huang, Tc., Feng, Wd., Fang, Gx. et al. Cancer-Associated fibroblasts regulate the development of cholangiocarcinoma through IL-6/STAT3/AKR1C3 signaling axis. Sci Rep 16, 10467 (2026). https://doi.org/10.1038/s41598-026-37583-y
الكلمات المفتاحية: سرطان القنوات الصفراوية, الخلايا الليفية المرتبطة بالسرطان, AKR1C3, إشارة IL-6 STAT3, أيض الورم