Clear Sky Science · de
Durch Krebs-assoziierte Fibroblasten reguliert: Entwicklung des Gallengangskarzinoms über die IL-6/STAT3/AKR1C3-Signalkaskade
Warum die Nachbarschaft des Tumors wichtig ist
Das Cholangiokarzinom, ein Krebs der Gallengänge in und um die Leber, ist berüchtigt dafür, früh nur schwer zu entdecken und nach Auftreten schwer zu behandeln zu sein. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Wie hilft das umliegende Gewebe diesen Tumoren beim Wachsen, beim Widerstehen gegen Chemotherapie und beim Umstellen ihres Energieverbrauchs? Indem die Forscher eine zentrale Kommunikationsachse zwischen Stütz- und Krebszellen aufdecken, weisen sie auf eine neue Verwundbarkeit hin, die künftige Therapien ansprechen könnten.
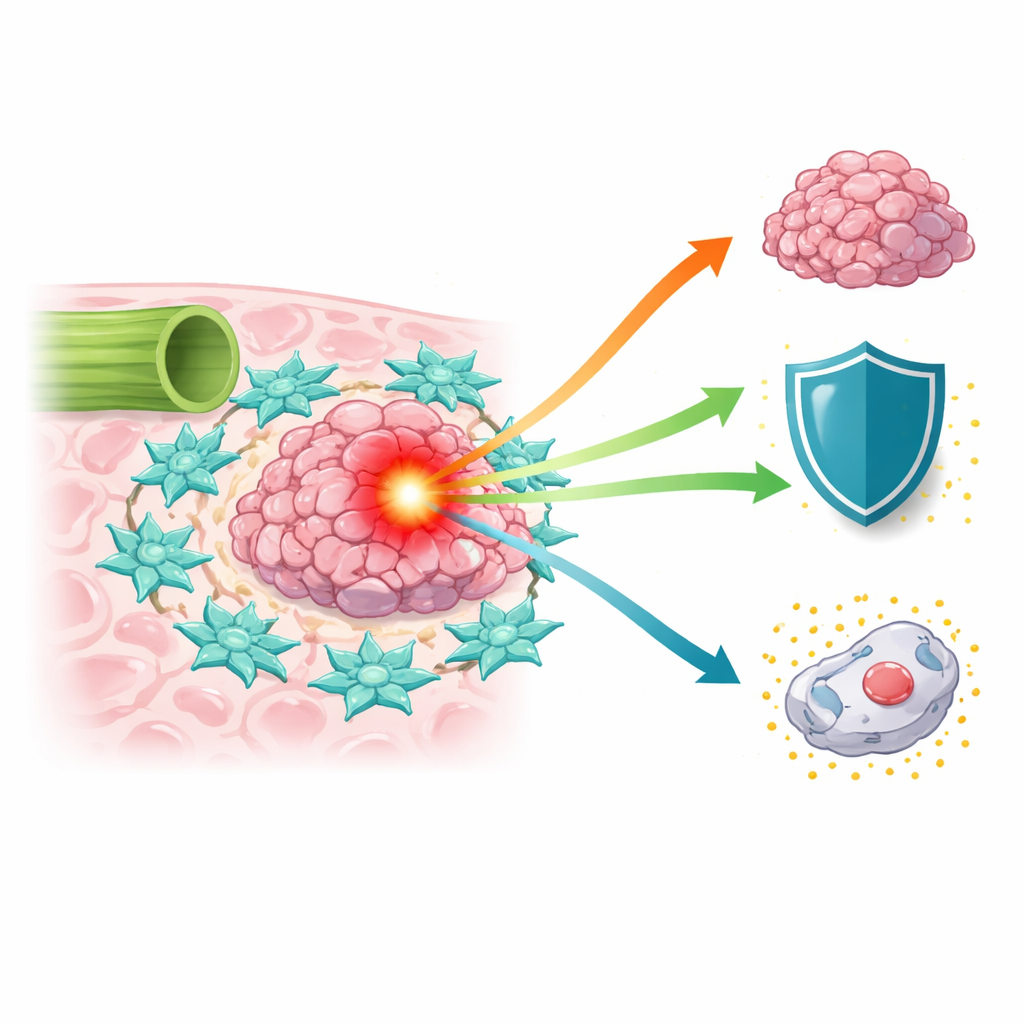
Ein schwer zu behandelnder Krebs mit steigender Häufigkeit
Die Inzidenz von Gallengangskarzinomen ist in den letzten zwei Jahrzehnten weltweit gestiegen; dennoch haben Patientinnen und Patienten häufig eine schlechte Prognose, weil Tumoren spät entdeckt werden und eine vollständige chirurgische Entfernung schwierig ist. Standard-Chemotherapeutika wie 5-Fluorouracil und platinhaltige Wirkstoffe bringen nur begrenzten Nutzen. Wissenschaftler haben erkannt, dass der Tumor nicht nur aus einer Ansammlung maligner Zellen besteht; er sitzt in einer komplexen Mikroumgebung aus Blutgefäßen, Immunzellen und Bindegewebszellen, die Krebs hemmen oder fördern können. Unter diesen Helfern treten krebsassoziierte Fibroblasten — Zellen, die normalerweise Gewebe aufbauen und umbauen — als mächtige Komplizen hervor, die Tumoren nähren und die Wirkung von Therapien abschwächen können.
Ein störendes Enzym in Tumorzellen
Das Team konzentrierte sich auf ein Stoffwechselenzym namens AKR1C3, das zuvor mit mehreren anderen Krebsarten in Verbindung gebracht wurde, in Gallengangstumoren aber kaum untersucht war. Die Analyse von Patientenproben zeigte, dass die AKR1C3-Spiegel im Cholangiokarzinomgewebe deutlich höher waren als in angrenzenden normalen Gallengängen. Patienten, deren Tumoren dieses Protein stark exprimierten, hatten größere Tumoren, häufiger Lymphknotenbefall, fortgeschrittenere Stadien und eine kürzere Gesamtüberlebenszeit. In im Labor kultivierten Krebszellen führte eine Erhöhung von AKR1C3 zu schnellerer Zellteilung, mehr Koloniebildung und größerer Chemotherapie-Resistenz, während eine Verringerung das Wachstum verlangsamte und die Medikamente wirksamer machte. Diese Ergebnisse deuten darauf hin, dass AKR1C3 nicht nur ein Begleiter, sondern ein aktiver Treiber aggressiven Verhaltens ist.
Wie Krebs seinen Zuckerhunger antreibt
Krebszellen bevorzugen oft eine zuckerhungrige Strategie, die als aerobe Glykolyse bekannt ist: Sie verbrennen Glukose schnell, selbst wenn ausreichend Sauerstoff vorhanden ist. Dieser stoffwechselbedingte Kurzschluss unterstützt rasches Wachstum und verändert das umliegende Gewebe. Wenn die Forscher AKR1C3 in Gallengangstumorzellen reduzierten, nahmen die Zellen weniger Glukose auf, setzten weniger Laktat frei (ein Nebenprodukt der Glykolyse) und zeigten geringere Messwerte für Säurebildung und Energieerzeugung. Anders gesagt: AKR1C3 trägt dazu bei, den Tumorstoffwechsel auf diesen schnellen, energieintensiven Modus umzustellen. Ohne das Enzym wurden die Krebszellen stoffwechselmäßig weniger aggressiv, was nahelegt, dass eine Hemmung von AKR1C3 Tumoren nicht nur verlangsamen, sondern sie auch „aushungern“ könnte.
Eine Signalübertragung von Stütz- zu Krebszellen
Um zu verstehen, wie die Nachbarzellen AKR1C3 beeinflussen, isolierten die Wissenschaftler krebsassoziierte Fibroblasten aus Patientenproben und kultivierten sie gemeinsam mit Cholangiokarzinomzellen. Die Fibroblasten schütteten den entzündlichen Botenstoff IL-6 aus, der einen bekannten Signalweg in den Krebszellen, den STAT3-Weg, aktivierte. Dieser erhöhte wiederum die AKR1C3-Spiegel. Wenn das Team IL-6 oder einen wichtigen Schritt der STAT3-Signalübertragung blockierte, sank AKR1C3 und die Krebszellen verloren einen Teil ihres Wachstums-, Arzneimittelresistenz- und Zuckerverbrauchsvorteils. Sie entdeckten außerdem eine zusätzliche Wendung: AKR1C3 beeinträchtigte SOCS1, eine natürliche Bremse von STAT3, indem es dessen Abbau förderte. So entstand eine sich selbst verstärkende Schleife, in der von Fibroblasten stammendes IL-6 STAT3 einschaltet, STAT3 AKR1C3 hochreguliert und AKR1C3 STAT3 aktiv hält, indem es dessen Inhibitor schwächt.
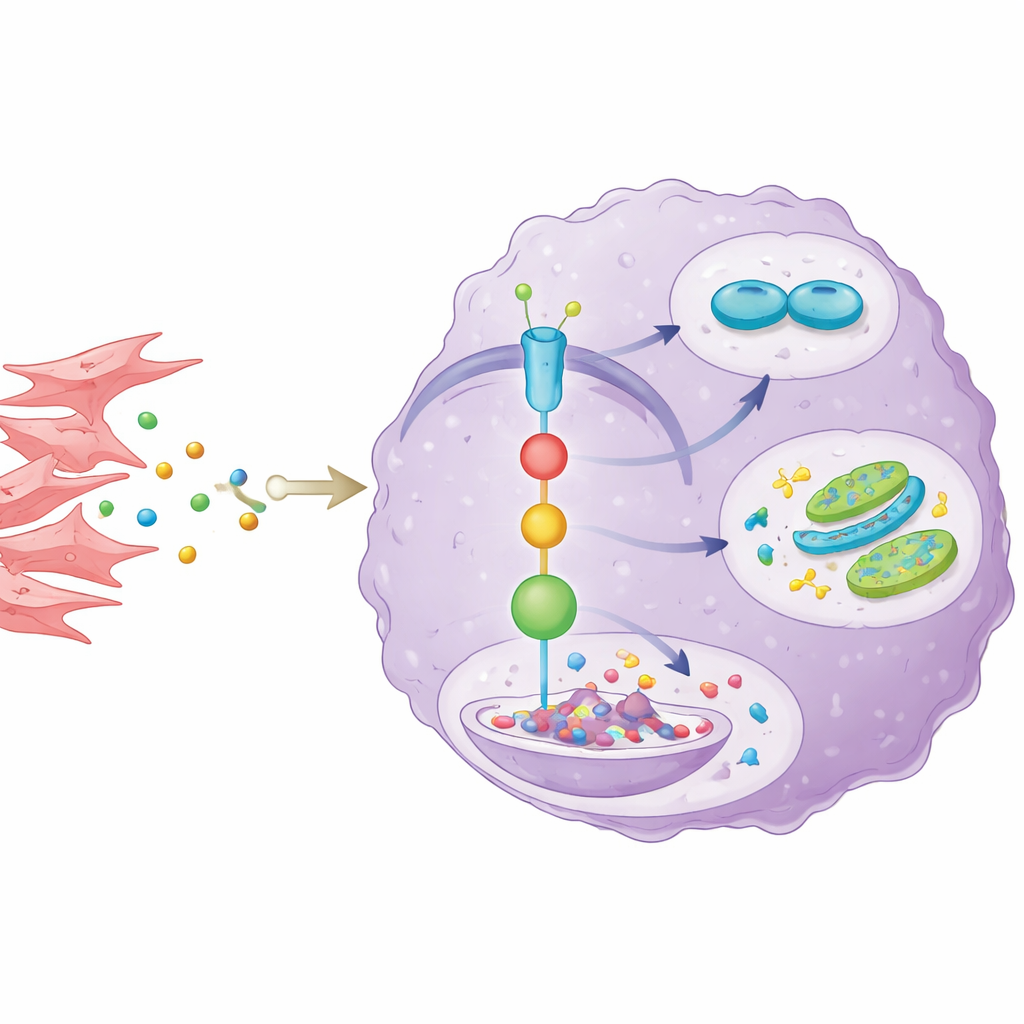
Von Mausmodellen zu möglichen Therapien
Die Befunde bestätigten sich in Tiermodellen. Wurden humane Gallengangstumorzellen mit reduziertem AKR1C3 in Mäuse implantiert, wuchsen die Tumoren langsamer. Die Vermischung dieser Tumorzellen mit Fibroblasten beschleunigte normalerweise das Tumorwachstum und machte die Tumoren schwerer behandelbar mit Chemotherapie. War AKR1C3 in den Tumorzellen jedoch herunterreguliert, konnte selbst die Anwesenheit von Fibroblasten ihre Vitalität nicht vollständig wiederherstellen, und die Tumoren blieben gegenüber 5-Fluorouracil empfindlicher. Tumorproben aus diesen Mäusen zeigten niedrigere AKR1C3-Werte, schwächere STAT3-Aktivität, weniger Anzeichen von Zellteilung und gedämpfte Stoffwechselmarker — was die zentrale Rolle dieser Signalachse im lebenden Gewebe stützt.
Was das für Patientinnen und Patienten bedeutet
Vereinfacht gesagt zeigt diese Forschung, dass bestimmte Stütz-Zellen in Gallengangstumoren eine chemische Botschaft aussenden, die ein Protein in Krebszellen einschaltet und sie dadurch schneller wachsen, der Chemotherapie widerstehen und Zucker intensiver verbrennen lässt. Dieses Protein, AKR1C3, trägt außerdem dazu bei, die Botschaft aufrechtzuerhalten, indem es einen eingebauten Sicherheitsmechanismus außer Kraft setzt. Aufgrund seines starken Zusammenhangs mit schlechter Prognose und seiner zentralen Stellung in dieser Schleife könnte AKR1C3 sowohl als Marker zur Identifizierung von Hochrisikopatienten als auch als Ziel für neue Medikamente dienen. Klinische Anwendungen erfordern zwar weitere Tests, doch die Störung der IL-6/STAT3/AKR1C3-Achse bietet eine vielversprechende Strategie, Gallengangstumoren zu schwächen, indem man die Kommunikation zwischen Tumorzellen und ihrer nährenden Umgebung angreift.
Zitation: Huang, Tc., Feng, Wd., Fang, Gx. et al. Cancer-Associated fibroblasts regulate the development of cholangiocarcinoma through IL-6/STAT3/AKR1C3 signaling axis. Sci Rep 16, 10467 (2026). https://doi.org/10.1038/s41598-026-37583-y
Schlüsselwörter: Cholangiokarzinom, Krebs-assoziierte Fibroblasten, AKR1C3, IL-6 STAT3 Signalübertragung, Tumorstoffwechsel