Clear Sky Science · fr
Les fibroblastes associés au cancer régulent le développement du cholangiocarcinome via l’axe de signalisation IL-6/STAT3/AKR1C3
Pourquoi le voisinage de la tumeur compte
Le cholangiocarcinome, un cancer des voies biliaires à l’intérieur et autour du foie, est notoirement difficile à détecter précocement et complexe à traiter une fois diagnostiqué. Cette étude pose une question apparemment simple mais aux grandes répercussions : comment le tissu entourant ces tumeurs aide-t-il leur croissance, leur résistance à la chimiothérapie et la réorganisation de leur métabolisme énergétique ? En découvrant une voie de communication clé entre les cellules de soutien et les cellules cancéreuses, les chercheurs identifient une nouvelle faiblesse potentielle que de futures thérapies pourraient cibler.
Un cancer difficile à traiter en augmentation
Le cancer des voies biliaires a augmenté dans le monde au cours des deux dernières décennies, et les patients font souvent face à un pronostic sombre parce que les tumeurs sont découvertes tard et l’exérèse chirurgicale complète est difficile. Les chimiothérapies standards, comme le 5-fluorouracile et les agents à base de platine, offrent des bénéfices limités. Les scientifiques ont compris que la tumeur n’est pas simplement un amas de cellules malignes ; elle évolue dans un microenvironnement complexe de vaisseaux sanguins, de cellules immunitaires et de cellules du tissu conjonctif qui peuvent soit freiner soit soutenir le cancer. Parmi ces auxiliaires, les fibroblastes associés au cancer — des cellules qui, normalement, construisent et réorganisent le tissu — apparaissent comme des complices puissants capables d’alimenter les tumeurs et d’atténuer les effets du traitement.
Une enzyme problématique à l’intérieur des cellules tumorales
L’équipe s’est concentrée sur une enzyme métabolique appelée AKR1C3, déjà liée à plusieurs autres cancers mais peu étudiée dans les tumeurs des voies biliaires. L’analyse d’échantillons de patients a montré que les niveaux d’AKR1C3 étaient bien plus élevés dans les tissus de cholangiocarcinome que dans les voies biliaires normales adjacentes. Les patients dont les tumeurs exprimaient fortement cette protéine présentaient des cancers plus volumineux, une dissémination ganglionnaire plus importante, des stades plus avancés et une survie globale plus courte. En culture, l’augmentation d’AKR1C3 rendait les cellules cancéreuses plus prolifératives, formant davantage de colonies et résistantes à la chimiothérapie, tandis que sa diminution ralentissait la croissance et rendait les médicaments plus efficaces. Ces résultats suggèrent qu’AKR1C3 n’est pas un simple témoin, mais un moteur actif du comportement agressif.
Alimenter l’appétit du cancer pour le glucose
Les cellules cancéreuses privilégient souvent une stratégie avide en glucose appelée glycolyse aérobie, brûlant rapidement le glucose même en présence d’oxygène. Ce raccourci métabolique soutient une croissance rapide et modifie le tissu environnant. Lorsque les chercheurs ont réduit AKR1C3 dans des cellules de cancer des voies biliaires, celles-ci prenaient moins de glucose, libéraient moins de lactate (un sous-produit de la glycolyse) et montraient des mesures plus faibles de production d’acide et de génération d’énergie. Autrement dit, AKR1C3 contribue à réorienter le métabolisme tumoral vers ce mode à haute vitesse et forte demande. En son absence, les cellules cancéreuses devenaient métaboliquement moins agressives, suggérant que bloquer AKR1C3 pourrait affamer les tumeurs autant que ralentir leur croissance.
Un relais de signal des cellules de soutien vers les cellules cancéreuses
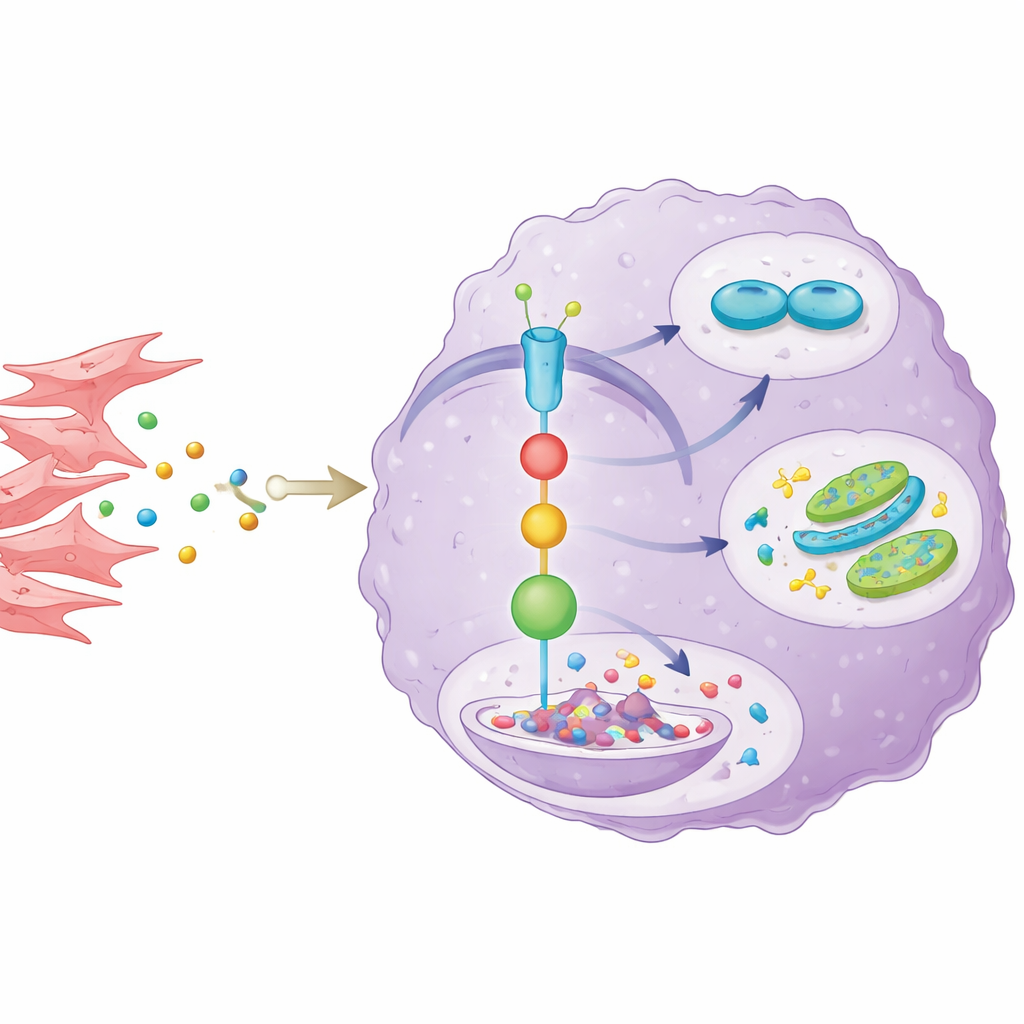
Pour comprendre comment les voisins tumoraux influencent AKR1C3, les scientifiques ont isolé des fibroblastes associés au cancer à partir de tumeurs de patients et les ont cultivés avec des cellules de cholangiocarcinome. Les fibroblastes sécrétaient le messager inflammatoire IL-6, qui activait une voie de communication bien connue à l’intérieur des cellules cancéreuses appelée voie STAT3. Cela augmentait à son tour les niveaux d’AKR1C3. Lorsque l’équipe bloquait l’IL-6 ou une étape clé de la signalisation STAT3, AKR1C3 diminuait et les cellules cancéreuses perdaient une partie de leur croissance, de leur résistance aux médicaments et de leurs avantages glycolytiques. Ils ont aussi mis au jour une autre subtilité : AKR1C3 interférait avec SOCS1, un frein naturel sur STAT3, en favorisant sa dégradation. Cela formait une boucle auto-renforçante où l’IL-6 d’origine fibroblastique active STAT3, STAT3 augmente AKR1C3, et AKR1C3 maintient STAT3 actif en affaiblissant son inhibiteur.
Des modèles murins aux pistes thérapeutiques possibles
Le mécanisme se confirmait dans des modèles animaux. Lorsque des cellules humaines de cancer des voies biliaires avec une expression réduite d’AKR1C3 étaient implantées chez des souris, les tumeurs croissaient plus lentement. Le mélange de ces cellules cancéreuses avec des fibroblastes accélérait normalement la croissance tumorale et rendait les tumeurs plus difficiles à traiter par chimiothérapie. Pourtant, si AKR1C3 était réduit dans les cellules cancéreuses, même la présence des fibroblastes ne pouvait pas entièrement restaurer leur vigueur, et les tumeurs restaient plus sensibles au 5-fluorouracile. Les prélèvements tumoraux de ces souris confirmaient une baisse d’AKR1C3, une activité STAT3 affaiblie, moins de signes de division cellulaire et des marqueurs métaboliques atténués, renforçant le rôle central de cet axe de signalisation dans le tissu vivant.
Ce que cela signifie pour les patients
En termes simples, ce travail montre que certaines cellules de soutien dans les tumeurs des voies biliaires envoient un signal chimique qui active une protéine à l’intérieur des cellules cancéreuses, les rendant plus prolifératives, résistantes à la chimiothérapie et plus intensément consommatrices de glucose. Cette protéine, AKR1C3, aide aussi à maintenir le signal en désactivant un dispositif de sécurité interne. En raison de son lien fort avec un mauvais pronostic et de sa position centrale dans cette boucle, AKR1C3 pourrait devenir à la fois un marqueur pour identifier les patients à haut risque et une cible pour de nouveaux médicaments. Bien que des applications cliniques requièrent des tests supplémentaires, perturber cette voie IL-6/STAT3/AKR1C3 offre une stratégie prometteuse pour affaiblir les cancers des voies biliaires en attaquant la communication entre les cellules tumorales et leur voisinage nourricier.
Citation: Huang, Tc., Feng, Wd., Fang, Gx. et al. Cancer-Associated fibroblasts regulate the development of cholangiocarcinoma through IL-6/STAT3/AKR1C3 signaling axis. Sci Rep 16, 10467 (2026). https://doi.org/10.1038/s41598-026-37583-y
Mots-clés: cholangiocarcinome, fibroblastes associés au cancer, AKR1C3, signalisation IL-6 STAT3, métabolisme tumoral