Clear Sky Science · ru
Фибробласты, связанные с раком, регулируют развитие холангиокарциномы через сигнальную ось IL-6/STAT3/AKR1C3
Почему окружение опухоли имеет значение
Холангиокарцинома — рак желчных протоков в печени и вокруг неё — известна тем, что её трудно выявить на ранних стадиях и сложно лечить после обнаружения. В этом исследовании задан на первый взгляд простой, но важный вопрос: как ткань вокруг этих опухолей помогает им расти, сопротивляться химиотерапии и перенастраивать энергетический обмен? Выявляя ключевой путь коммуникации между поддерживающими клетками и раковыми клетками, авторы работы указывают на новую уязвимость, на которую могли бы быть нацелены будущие терапевтические подходы.
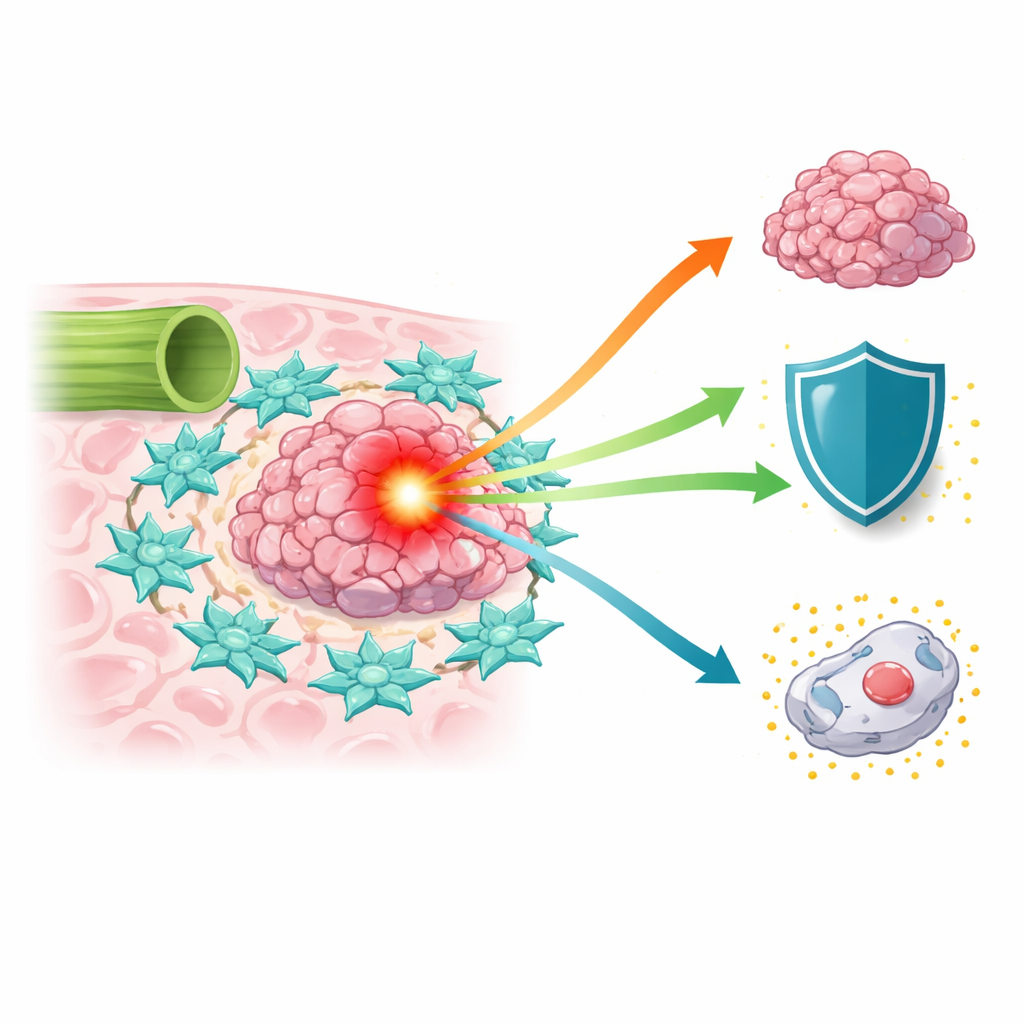
Трудноизлечимая опухоль, частота которой растёт
За последние два десятилетия заболеваемость раком желчных протоков увеличивается во всём мире, однако прогноз у пациентов часто остаётся неблагоприятным, поскольку опухоли обнаруживаются поздно и их сложно полностью удалить хирургически. Стандартные препараты химиотерапии, такие как 5‑фторурацил и препараты на платиновой основе, дают ограниченную пользу. Ученые приходят к выводу, что опухоль — это не просто скопление злокачественных клеток, а сложная «микросреда» сосудов, иммунных клеток и клеток соединительной ткани, которые могут либо сдерживать, либо поддерживать рак. Среди этих помощников фибробласты, связанные с раком — клетки, которые обычно строят и перестраивают ткани — проявляют себя как мощные соучастники, способные подпитывать опухоли и ослаблять эффект лечения.
Проблемный фермент внутри раковых клеток
Группа сосредоточилась на метаболическом ферменте AKR1C3, ранее связанном с несколькими другими видами рака, но плохо изученном при опухолях желчных протоков. Анализ образцов пациентов показал, что уровни AKR1C3 значительно выше в ткани холангиокарциномы, чем в прилегающих нормальных желчных протоках. У пациентов с высокой экспрессией этого белка опухоли были крупнее, чаще отмечалось поражение лимфоузлов, более поздняя стадия заболевания и более короткая общая выживаемость. В культурах раковых клеток повышение уровня AKR1C3 ускоряло деление, увеличивало образование колоний и усиливало устойчивость к химиотерапии, тогда как снижение его уровня замедляло рост и делало препараты более эффективными. Эти результаты указывают на то, что AKR1C3 — не случайный попутчик, а активный фактор агрессивного поведения.
Подпитывая тягу рака к сахару
Раковые клетки часто предпочитают стратегию, называемую аэробным гликолизом: интенсивно сжигают глюкозу даже при наличии кислорода. Этот метаболический путь поддерживает быстрый рост и перестраивает окружающую ткань. Когда исследователи уменьшали AKR1C3 в клетках холангиокарциномы, клетки меньше поглощали глюкозу, выделяли меньше лактата (побочного продукта гликолиза) и демонстрировали пониженные показатели кислотности и генерации энергии. Иными словами, AKR1C3 помогает перенастроить метаболизм опухоли в сторону этого быстрого, энергозатратного режима. Без него раковые клетки становились метаболически менее агрессивными, что даёт основание полагать, что блокирование AKR1C3 могло бы не только замедлить рост опухоли, но и «голодать» её.
Сигнальная передача от поддерживающих клеток к раковым
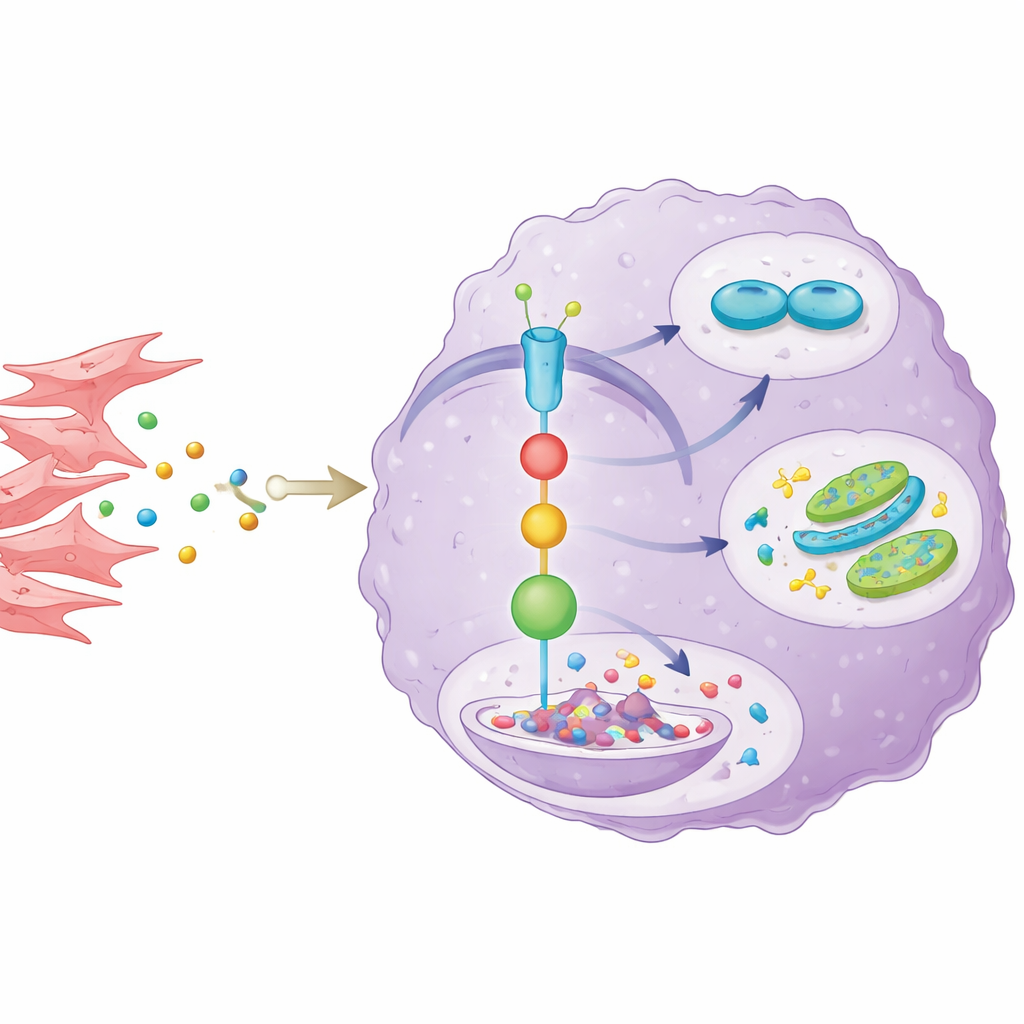
Чтобы понять, как клетки окружения опухоли регулируют AKR1C3, учёные выделили фибробласты, связанные с раком, из тканей пациентов и выращивали их вместе с клетками холангиокарциномы. Фибробласты секретировали воспалительный мессенджер IL‑6, который активировал известный внутриклеточный путь передачи сигналов STAT3 в раковых клетках. Это, в свою очередь, повышало уровни AKR1C3. Когда команда блокировала IL‑6 или ключевой этап в сигналинге STAT3, уровни AKR1C3 снижались, и раковые клетки теряли часть своих преимуществ в росте, лекарственной устойчивости и сахарном обмене. Авторы также обнаружили дополнительную деталь: AKR1C3 мешал SOCS1, природному тормозу STAT3, способствуя его разрушению. Так образовывался самоподдерживающийся цикл: IL‑6, поступающий от фибробластов, включает STAT3, STAT3 повышает AKR1C3, а AKR1C3 поддерживает активность STAT3, ослабляя его ингибитор.
От мышиных моделей к возможным терапиям
Наблюдения подтвердились в животной модели. Когда в мышей имплантировали человеческие клетки холангиокарциномы с пониженной экспрессией AKR1C3, опухоли росли медленнее. Смешивание этих раковых клеток с фибробластами обычно ускоряло рост опухолей и делало их менее чувствительными к химиотерапии. Однако при подавлении AKR1C3 в раковых клетках даже наличие фибробластов не могло полностью восстановить их агрессивность, и опухоли оставались более чувствительными к 5‑фторурацилу. Образцы опухолей этих мышей подтверждали пониженные уровни AKR1C3, ослабленную активность STAT3, меньше признаков деления клеток и сниженные метаболические маркеры, что укрепляет ключевую роль этой сигнальной оси в живой ткани.
Что это значит для пациентов
Проще говоря, это исследование показывает, что определённые поддерживающие клетки в опухолях желчных протоков посылают химический сигнал, который включает белок внутри раковых клеток, заставляя их расти быстрее, сопротивляться химиотерапии и активнее «сжигать» сахар. Этот белок, AKR1C3, также помогает поддерживать сигнал, отключая встроенный предохранитель. Благодаря сильной связи с плохим исходом и центральной роли в этом цикле, AKR1C3 может стать как маркером для выявления пациентов с высоким риском, так и мишенью для новых препаратов. Хотя клиническое применение потребует дальнейшей валидации, вмешательство в путь IL‑6/STAT3/AKR1C3 представляет собой перспективную стратегию ослабления рака желчных протоков за счёт нарушения диалога между опухолевыми клетками и их «кормящим» окружением.
Цитирование: Huang, Tc., Feng, Wd., Fang, Gx. et al. Cancer-Associated fibroblasts regulate the development of cholangiocarcinoma through IL-6/STAT3/AKR1C3 signaling axis. Sci Rep 16, 10467 (2026). https://doi.org/10.1038/s41598-026-37583-y
Ключевые слова: холангиокарцинома, фибробласты, связанные с раком, AKR1C3, сигналинг IL-6 STAT3, метаболизм опухоли