Clear Sky Science · sv
$${\bf{Micro}}{{\mathbb{S}}}{\bf{plit}}$$ : semantisk uppdelning av fluorescerande mikroskopidata
Se mer med mindre ljus
Moderna mikroskop låter forskare följa levande celler i arbete, men varje bild har sin kostnad. Varje ljusblixt kan skada känsliga celler, och att använda många olika glödande markörer når snabbt fysiska begränsningar. Denna artikel presenterar MicroSplit, ett beräkningsmässigt knep som låter forskare fånga flera cellstrukturer i en enda, enklare bild och sedan separera dem i efterhand i datorn, vilket minskar belastningen både på mikroskopet och på cellerna.
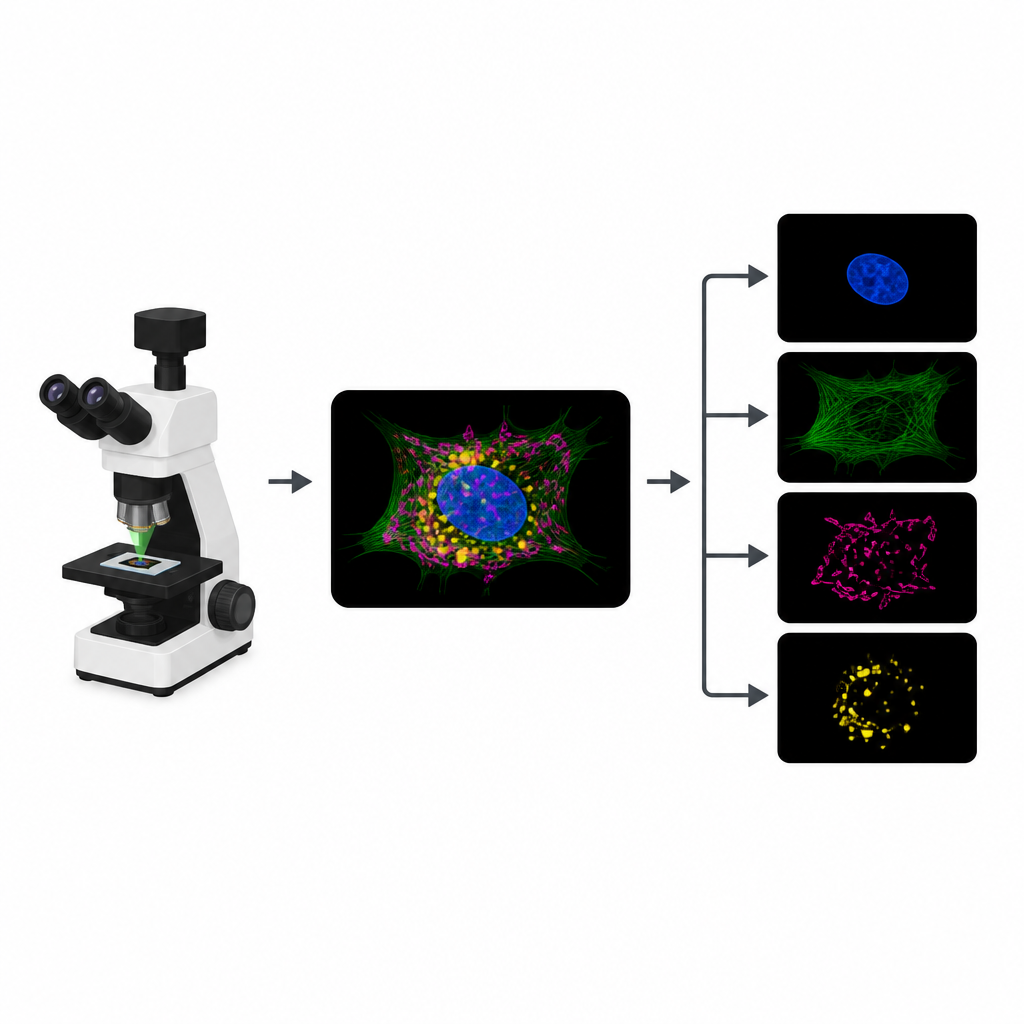
Varför glödande celler stöter på en gräns
För att följa olika delar av en cell fäster biologer distinkta fluorescerande färgämnen vid strukturer som kärnan, cytoskelettet eller cellernas energiverk. I ett typiskt experiment registrerar mikroskopet en separat bildkanal för varje färgämne. Färgämnena reagerar dock ofta på liknande våglängder, så deras signaler överlappar. Denna överlapp begränsar hur många strukturer som kan följas samtidigt. Dessutom innebär varje extra kanal en ny omgång belysning, vilket förbrukar en begränsad “fotonbudget” och kan göra filmer långsammare, sudda ut detaljer eller skada levande prover.
Förvandla en trång bild till många tydliga
MicroSplit angriper denna kompromiss genom att ändra hur information samlas in och bearbetas. Istället för att ta flera separata bilder kan forskare märka flera strukturer som vanligt men registrera dem tillsammans i en enda fluorescerande kanal. Denna enda, trängda bild matas sedan in i en djupinlärningsmodell som tränats för att ”avblanda” de mönster den ser. Nätverket ger ut flera rengjorda bilder, där varje bild framhäver en annan struktur som om den hade avbildats i sin egen kanal från början.
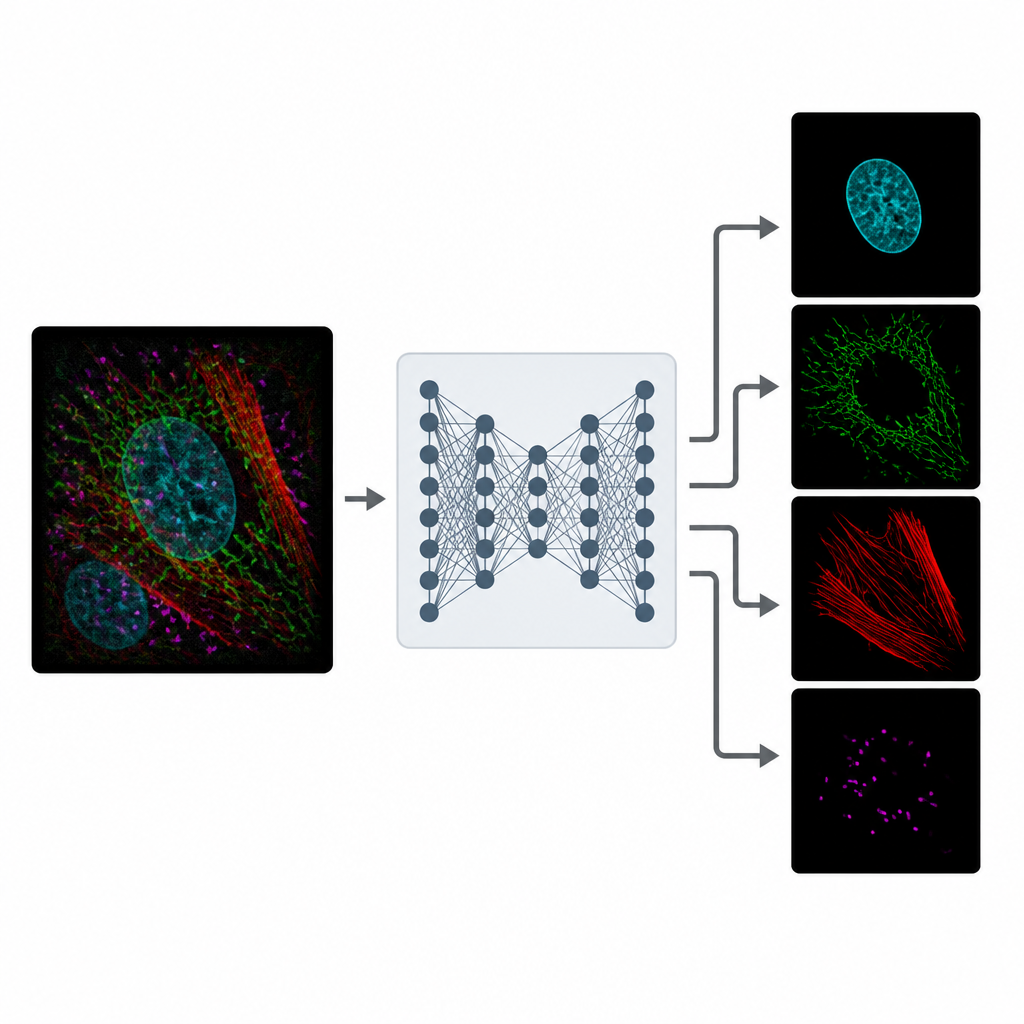
Lärande från brusig verklighet
Att träna MicroSplit kräver inte fläckfria referensbilder. Författarna visar att modellen kan lära sig från vanliga, brusiga mikroskopdata, som är mycket enklare att få fram. Under träningen får systemet exempel där separata kanaler och deras summerade kombination finns tillgängliga. Det lär sig två saker samtidigt: hur man separerar överlappande strukturer och hur man tar bort brus. Med en speciell typ av neuralt nätverk som provar många plausibla lösningar kan MicroSplit också uppskatta var sina egna prediktioner är osäkra, och flagga regioner som bör behandlas försiktigt eller kontrolleras av en expert.
Fungerar över dataset och användningar
Forskarna testade MicroSplit på tio olika mikroskopdataset, i både två och tre dimensioner och med upp till fyra överlappande cellstrukturer. I 30 huvuduppgifter var de separerade bilderna tillräckligt precisa för att stödja vanliga efterföljande analyser som segmentering av celldelar. I noggranna tester producerade mänskliga analytiker lika konsekventa segmenteringar på MicroSplit‑resultat som på konventionella multikanalsbilder. Metoden kan också vändas för att ta bort oönskade inslag: genom att lära MicroSplit att skilja verklig signal från återkommande prickar eller fläckar kan modellen subtrahera dessa bildartefakter samtidigt som verkliga strukturer bevaras.
Känna till begränsningarna
MicroSplit är ingen magi, och författarna utforskar öppet när det får problem. Prestandan sjunker om de ursprungliga bilderna är extremt brusiga, om en struktur är mycket svagare än en annan, eller om två strukturer ser nästan identiska ut. I sådana fall tenderar modellen att jämna ut mycket fina detaljer snarare än att hitta falsk skärpa. Ändå levererar MicroSplit ofta separerade bilder som är tillräckliga för kvantitativt arbete även vid korta exponeringstider, samtidigt som betydligt färre fotoner används än i traditionella metoder.
Vad detta betyder för framtidens avbildning
För icke‑specialister är huvudbudskapet att MicroSplit låter mikroskop ”se” fler strukturer på kortare tid och med mindre ljus genom att flytta en del av arbetet från hårdvara till mjukvara. Istället för att begränsas av hur många färger ett mikroskop kan separera optiskt kan forskare kombinera signaler i en kanal och låta MicroSplit göra sorteringen. Detta frigör ljus för att göra filmer snabbare, fånga svaga strukturer skonsammare eller lägga till extra markörer som tidigare var opraktiska. Genom att publicera kod, data och tränade modeller öppet strävar författarna efter att göra denna typ av beräkningsmässig multiplexering till en rutin inom biologisk avbildning.
Citering: Ashesh, A., Carrara, F., Zubarev, I. et al. \({\bf{Micro}}{{\mathbb{S}}}{\bf{plit}}\): semantic unmixing of fluorescent microscopy data. Nat Methods 23, 1047–1057 (2026). https://doi.org/10.1038/s41592-026-03082-1
Nyckelord: fluorescensmikroskopi, djupinlärning, bildavblandning, beräkningsmässig multiplexering, bioimage-analys