Clear Sky Science · de
$${\bf{Micro}}{{\mathbb{S}}}{\bf{plit}}$$ : semantisches Entmischen von fluoreszenzmikroskopischen Daten
Mehr sehen mit weniger Licht
Moderne Mikroskope erlauben es Forschern, lebende Zellen in Aktion zu beobachten, aber jedes Bild hat seinen Preis. Jeder Lichtblitz kann empfindliche Zellen schädigen, und viele verschiedene leuchtende Marker stoßen schnell an physikalische Grenzen. Dieses Paper stellt MicroSplit vor, einen rechnerischen Trick, mit dem Forschende mehrere Zellstrukturen in einem einzigen, einfacheren Bild erfassen und diese später am Computer trennen können, wodurch sowohl das Mikroskop als auch die Zellen entlastet werden.
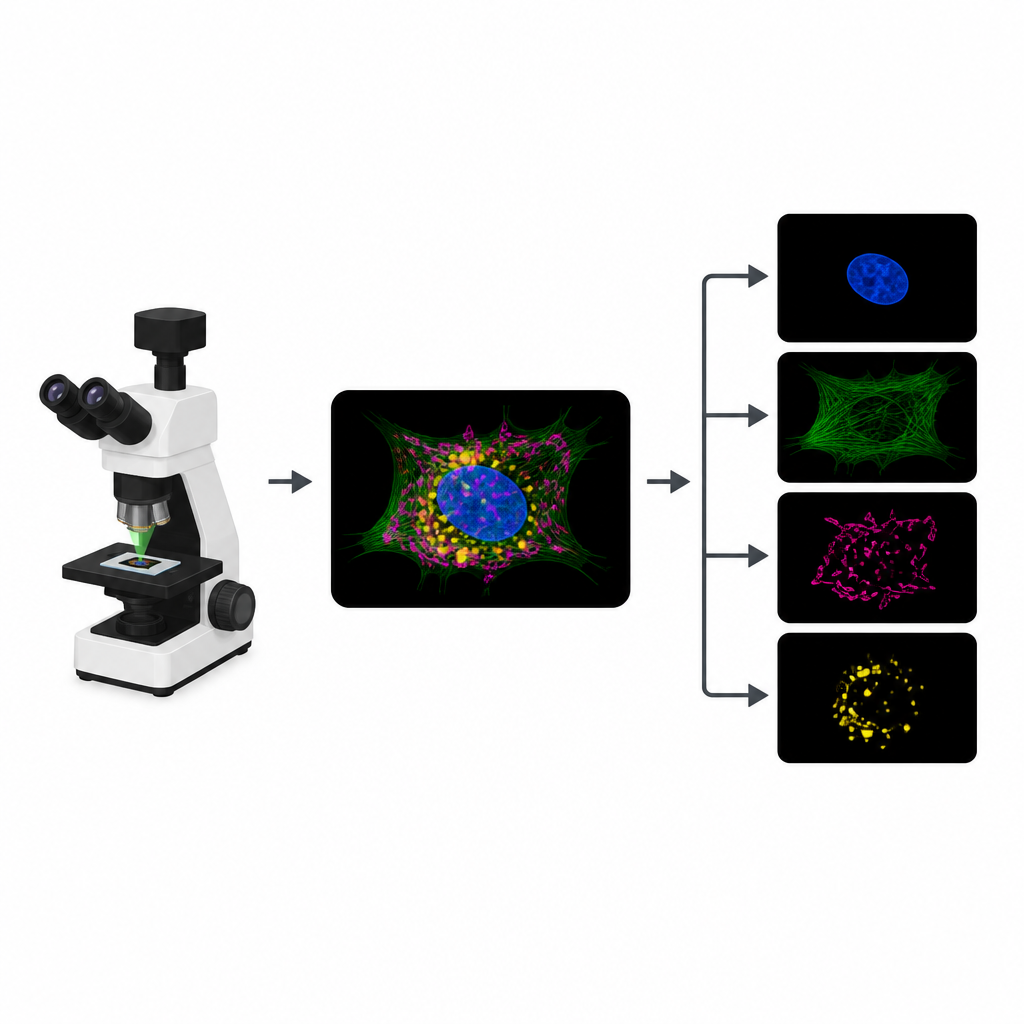
Warum leuchtende Zellen an Grenzen stoßen
Um verschiedene Teile einer Zelle zu verfolgen, bringen Biologen unterschiedliche fluoreszierende Farbstoffe an Strukturen wie Zellkern, Zytoskelett oder Energiezentralen an. In einem typischen Experiment zeichnet das Mikroskop für jeden Farbstoff einen eigenen Bildkanal auf. Die Farbstoffe sprechen jedoch oft auf ähnliche Lichtfarben an, sodass sich ihre Signale überlappen. Diese Überlappung begrenzt, wie viele Strukturen gleichzeitig verfolgt werden können. Zusätzlich bedeutet jeder zusätzliche Kanal eine weitere Belichtung, was das knappe „Photonenbudget“ aufzehrt und Filme verlangsamen, Details verwischen oder lebende Proben schädigen kann.
Aus einem überfüllten Bild viele klare machen
MicroSplit begegnet diesem Kompromiss, indem es die Art der Informationsgewinnung und -verarbeitung verändert. Statt mehrere separate Aufnahmen zu machen, können Forschende mehrere Strukturen wie gewohnt markieren, sie aber gemeinsam in einem einzigen Fluoreszenzkanal aufzeichnen. Dieses einzelne, überfüllte Bild wird dann in ein Deep-Learning-Modell eingespeist, das darauf trainiert wurde, die darin enthaltenen Muster zu „entmischen“. Das Netzwerk liefert mehrere bereinigte Bilder aus, von denen jedes eine andere Struktur hervorhebt — so, als wäre sie von Anfang an in einem eigenen Kanal aufgenommen worden.
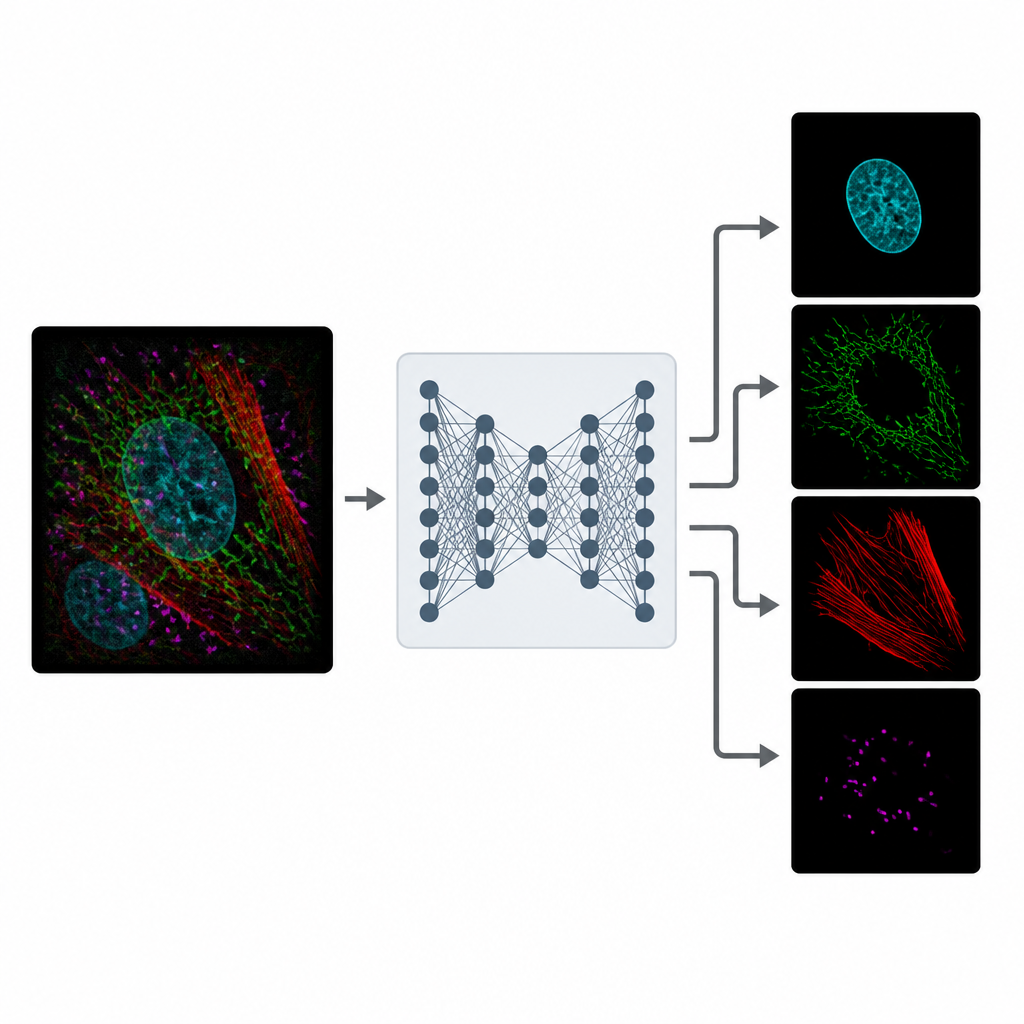
Vom verrauschten Realbild lernen
Das Training von MicroSplit erfordert keine makellosen Referenzbilder. Die Autoren zeigen, dass das Modell aus gewöhnlichen, verrauschten Mikroskopiedaten lernen kann, die deutlich leichter zu beschaffen sind. Während des Trainings werden Beispiele bereitgestellt, bei denen separate Kanäle und deren Summenkombination verfügbar sind. Es lernt zwei Dinge gleichzeitig: wie überlappende Strukturen zu trennen sind und wie Rauschen entfernt werden kann. Mithilfe einer speziellen Art von neuronalen Netzwerk, das viele plausible Lösungen sampelt, kann MicroSplit außerdem abschätzen, wo seine Vorhersagen unsicher sind, und Bereiche markieren, die mit Vorsicht zu behandeln oder von einer Expertin beziehungsweise einem Experten zu prüfen sind.
Über verschiedene Datensätze und Anwendungen hinweg
Die Forschenden testeten MicroSplit an zehn verschiedenen Mikroskopiedatensätzen, in zwei und drei Dimensionen und mit bis zu vier überlappenden Zellstrukturen. In 30 Hauptaufgaben waren die getrennten Bilder genau genug, um gängige Folgeanalysen wie die Segmentierung von Zellteilen zu unterstützen. In sorgfältigen Tests erzeugten menschliche Analysten gleichermaßen konsistente Segmentierungen auf MicroSplit-Ergebnissen und auf herkömmlichen Multikanal-Bildern. Die Methode lässt sich auch umkehren, um unerwünschte Merkmale zu entfernen: Indem MicroSplit beigebracht wird, echtes Signal von wiederkehrenden Flecken oder Verunreinigungen zu unterscheiden, kann das Modell diese Bildartefakte subtrahieren und gleichzeitig reale Strukturen bewahren.
Die Grenzen kennen
MicroSplit ist keine Magie, und die Autorinnen und Autoren untersuchen offen, wann das Verfahren an seine Grenzen stößt. Die Leistung sinkt, wenn die Ausgangsbilder extrem verrauscht sind, wenn eine Struktur deutlich schwächer ist als eine andere oder wenn zwei Strukturen sich fast identisch zeigen. In solchen Fällen neigt das Modell dazu, sehr feine Details zu glätten, statt falsche Schärfe zu erzeugen. Dennoch liefert MicroSplit selbst bei kurzen Belichtungszeiten häufig getrennte Bilder, die für quantitative Auswertungen ausreichend sind, während deutlich weniger Photonen als bei traditionellen Ansätzen verwendet werden.
Was das für die zukünftige Bildgebung bedeutet
Für Nicht‑Spezialisten ist die Kernbotschaft, dass MicroSplit Mikroskopen ermöglicht, mehr Strukturen in weniger Zeit und mit weniger Licht zu „sehen“, indem ein Teil der Arbeit von der Hardware auf Software verlagert wird. Anstatt durch die optische Fähigkeit eines Mikroskops eingeschränkt zu sein, wie viele Farben es trennen kann, können Forschende Signale in einem Kanal kombinieren und MicroSplit die Sortierung überlassen. Dies schafft Freiraum für Licht, um Filme schneller aufzunehmen, schwache Strukturen schonender zu erfassen oder zusätzliche Marker zu verwenden, die zuvor unpraktisch waren. Indem die Autorinnen und Autoren Code, Daten und trainierte Modelle offen zugänglich machen, wollen sie diese Form der computationalen Multiplexierung zu einem routinemäßigen Bestandteil biologischer Bildgebung machen.
Zitation: Ashesh, A., Carrara, F., Zubarev, I. et al. \({\bf{Micro}}{{\mathbb{S}}}{\bf{plit}}\): semantic unmixing of fluorescent microscopy data. Nat Methods 23, 1047–1057 (2026). https://doi.org/10.1038/s41592-026-03082-1
Schlüsselwörter: Fluoreszenzmikroskopie, Deep Learning, Bildentmischung, computationale Multiplexierung, Bioimage-Analyse