Clear Sky Science · sv
En profagkodad abortiv infektionsprotein bevarar värd och profagsspridning
Hur bakterier använder dolda passagerare för att bekämpa virus
Bakterier utsätts ständigt för angrepp från virus kallade fag, men många överlever tack vare små genetiska fripassagerare som kallas profager—vilande virus inbyggda i deras DNA. Denna studie visar hur en sådan profag utrustar Salmonella med en kraftfull självdödsknapp som stoppar invaderande virus, samtidigt som profagen själv kan fortsätta spridas. Att förstå detta molekylära dragkamp förklarar hur farliga patogener ligger steget före sina egna rovdjur.
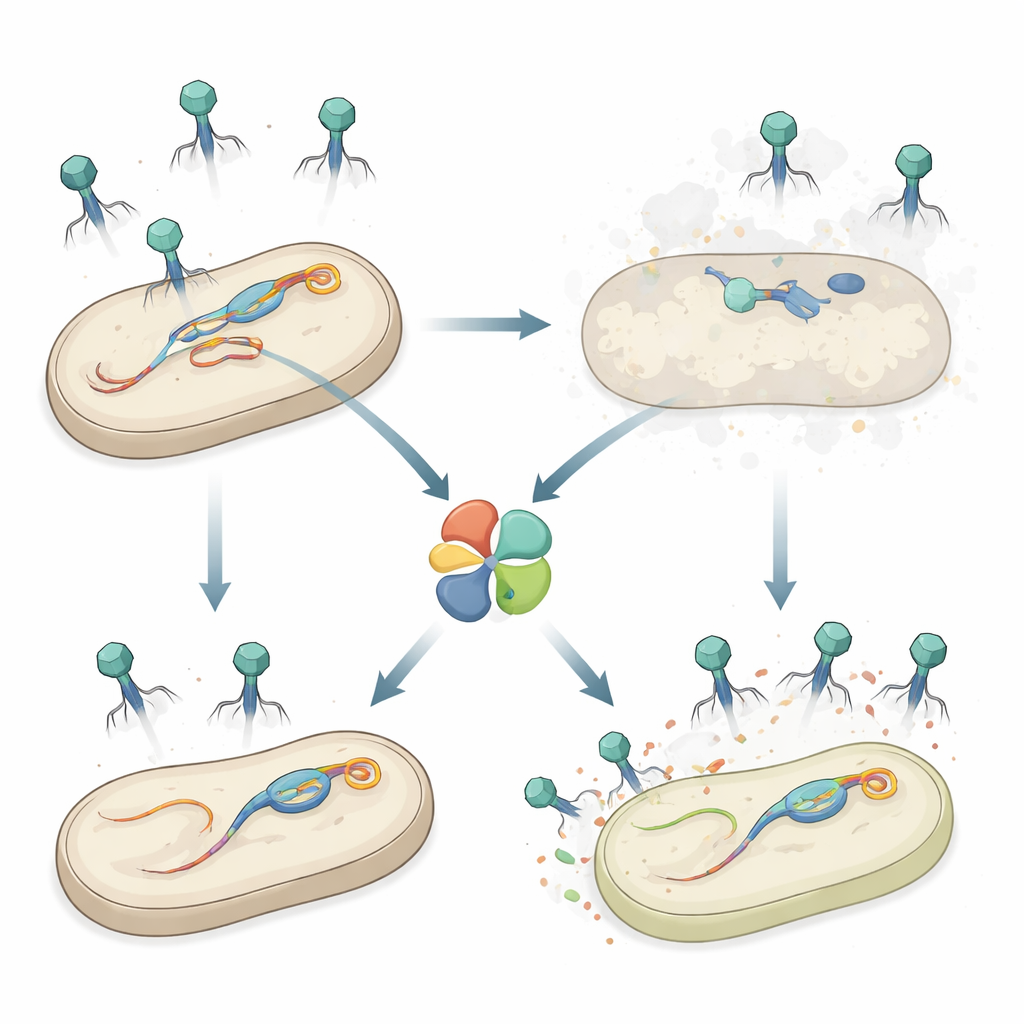
Ett hemligt vapen inuti Salmonella
Forskarna studerade Salmonella enterica serovar Typhimurium, en matburen patogen som, liksom många bakterier, bär flera profager i sitt kromosom. Tidigare arbete visade att en profag, kallad Gifsy‑1, hjälper Salmonella att motstå angrepp från vissa fag. Här upptäckte teamet en ytterligare försvarsgene på Gifsy‑1, namngiven hepS, som gör bakterierna betydligt mindre sårbara för en grupp långtstjärtade fag som kallas Siphoviridae. När hepS togs bort bildade invaderande fag många fler plack—klara fläckar av döda celler—vilket visar att HepS kraftigt minskar lyckade infektioner och att det verkar oberoende av andra kända försvar i samma profag.
Ett självuppoffrande system som bara vaknar vid angrepp
HepS tillhör en familj proteiner som ofta fungerar som molekylära "sista stånd": när de känner av en infektion stänger de ner viktiga cellulära processer så att både cellen och viruset dör. Forskarna visade att HepS beter sig på detta sätt—ett abortivt infektionssystem—som skyddar den övergripande bakteriepopulationen genom att offra enskilda infekterade celler. Strukturella studier visade att HepS naturligt monteras ihop till en fyra‑delad komplex (en tetramer) där de aktiva centra är begravda och dåligt inriktade, vilket tyder på ett "av"‑läge som är säkert för värden. Överuttryck av HepS i bakterier hämmande inte tillväxten, vilket stöder idén att proteinet förblir ofarligt tills det triggas precis.
Hur fagstjärtspetsar växlar molekylströmbrytaren
För att ta reda på vad som aktiverar HepS utsatte teamet bakterier med hepS för många olika fag och fann att de flesta känsliga virus delade liknande stjärtspetsproteiner, delarna som känner igen och genomborrar bakterieytan. Genom att välja sällsynta "flykt"‑fag som kunde växa trots HepS spårade de resistens till enstaka aminosyreförändringar i ett kort segment av stjärtspetsproteinet, kallat J. Att uttrycka detta J‑fragment inne i celler gjorde plötsligt HepS toxiskt, men flyktvarianten gjorde det inte längre. Biokemiska experiment bekräftade att HepS binder detta lilla J‑peptid direkt. Högupplösta kristallstrukturer visade att när peptiden dockar på varje subenhet i HepS‑tetrameren omarrangeras hela komplexet: de aktiva sätena svänger upp och inriktas, vilket omvandlar HepS till ett potent RNA‑skärande enzym.
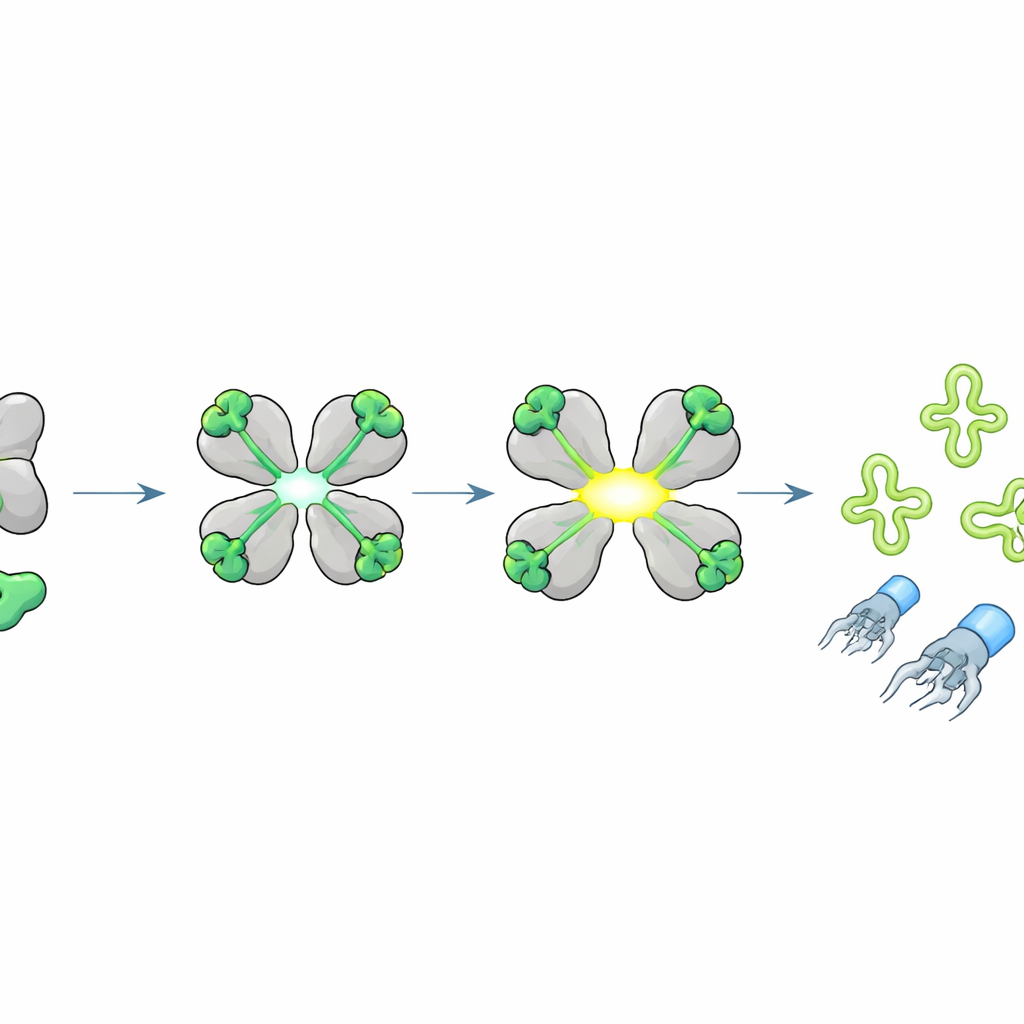
Skär ut nyckel‑tRNA för att stoppa virusproduktion
Vad skär det aktiverade HepS upp? Forskarna observerade att när J‑peptiden slog på HepS bröts cellens RNA i karakteristiska fragment. Genom specialiserad sekvensering fokuserad på transfer‑RNA (tRNA)—adaptrarna som läser den genetiska koden under proteinsyntes—fann de att HepS skär specifika tRNA exakt i deras antikodonloopar, särskilt de för aminosyrorna treonin, isoleucin och serin. Strukturell modellering föreslog hur en öppnad HepS‑tetramer kan omsluta ett måltaveltRNA och placera sina katalytiska rester precis vid antikodonet. Att förstöra dessa tRNA berövar cellen viktiga byggstenar för proteinsyntes, vilket abrupt stoppar produktionen av virusproteiner och blockerar monteringen av kompletta faggänget, trots att virusets DNA‑replikation fortfarande kan ske.
Hur den boende profagen undviker vänskapseld
En central gåta är varför Gifsy‑1, som kodar för HepS, inte dödas av sitt eget försvar. Svaret ligger återigen i stjärtspetsproteinet. De tre bofasta Gifsy‑profagerna i Salmonella har alla J‑proteiner som är nära besläktade med de HepS‑utlösande varianterna, men vid den kritiska position där aktiverande fag bär en stor fenylalanin, har Gifsy J‑proteiner en mildare isoleucin. Experiment visade att vildtypens Gifsy J inte aktiverar HepS, medan konstruerade versioner som byter in fenylalanin plötsligt gör det, vilket leder till nästan fullständig förlust av Gifsy‑1‑partiklar—men endast när hepS är närvarande. Vid blandade infektioner, när Gifsy‑1 samexisterar med en aktiverande profag som ES18, försvagar HepS framför allt ES18 medan Gifsy‑1 endast påverkas måttligt, vilket ger den HepS‑kodande profagen en konkurrensfördel i att producera nya partiklar och sprida sig till nya värdar.
Vad detta betyder för bakterier, virus och oss
Sammantaget avslöjar detta arbete en finslipad överlevnadsstrategi: en profag beväpnar sin Salmonella‑värd med ett fällprote som känner igen ett kännetecken hos närbesläktade invaderande virus, och därefter förstör cellens egna proteinproducerande maskineri genom att skära ut utvalda tRNA. Detta uppoffrande drag stoppar angriparens livscykel och skyddar den bredare bakteriesamhället, medan subtila förändringar i profagens eget stjärtspetsprotein låter den smita förbi sin egen fälla och fortsätta replikera. Studien belyser hur virus inbäddade i bakteriegenom gör mer än att ligga vilande—de formar aktivt strider mot andra virus och påverkar vilka stammar av både bakterier och fag som frodas i mikrobiella ekosystem.
Citering: Sargen, M.R., Antine, S.P., Grabe, G.J. et al. A prophage-encoded abortive infection protein preserves host and prophage spread. Nature 652, 201–208 (2026). https://doi.org/10.1038/s41586-025-10070-6
Nyckelord: bakteriofagförsvar, profag, abortiv infektion, tRNA‑nukleas, Salmonella‑faginteraktioner