Clear Sky Science · fr
Une protéine d’infection avortée codée par un prophage préserve l’hôte et la propagation du prophage
Comment les bactéries utilisent des passagers cachés pour lutter contre les virus
Les bactéries subissent en permanence des attaques de virus appelés phages, et pourtant de nombreuses s’en sortent grâce à de petits passagers génétiques appelés prophages — des virus dormants intégrés à leur ADN. Cette étude révèle comment un prophage de ce type équipe Salmonella d’un puissant interrupteur d’autodestruction qui stoppe les virus envahisseurs, tout en permettant au prophage lui‑même de continuer à se propager. Comprendre ce bras de fer moléculaire aide à expliquer comment des agents pathogènes dangereux restent en avance sur leurs propres prédateurs.
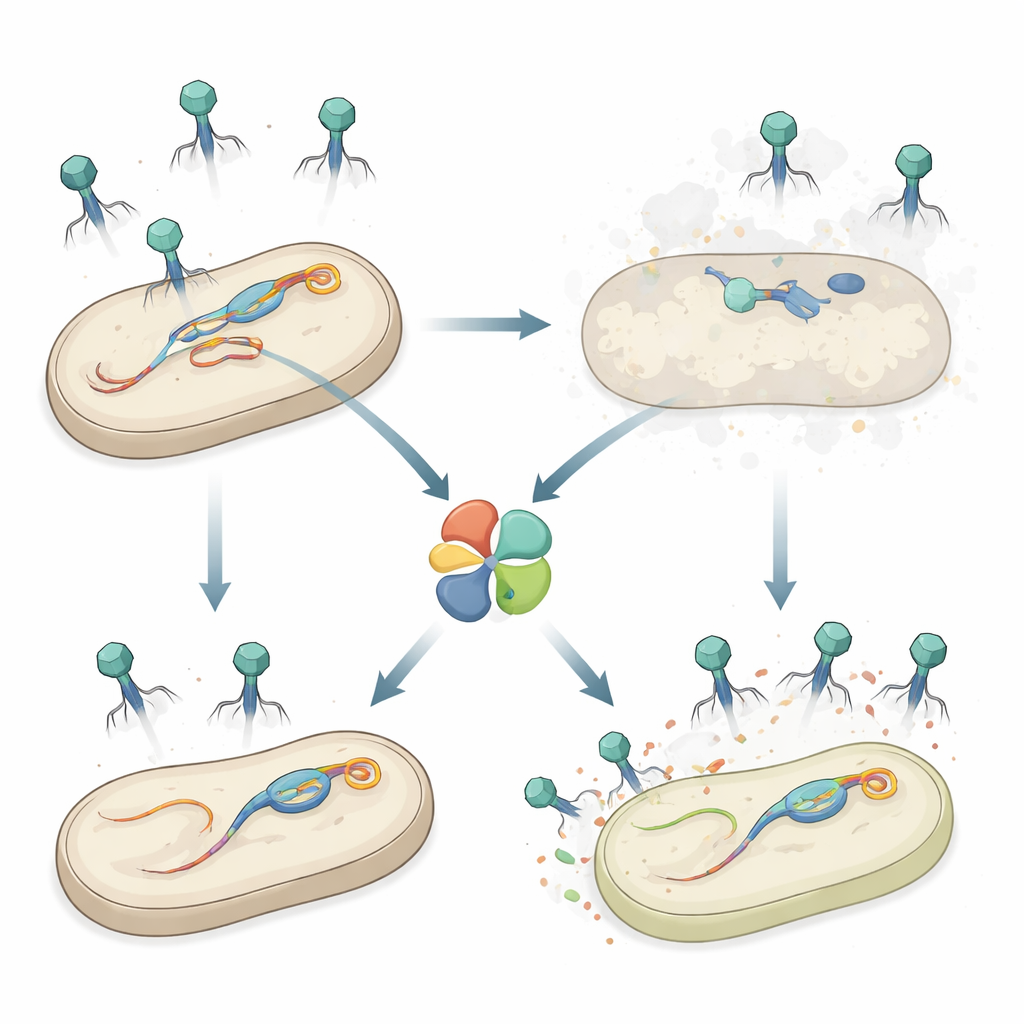
Une arme secrète à l’intérieur de Salmonella
Les auteurs ont étudié Salmonella enterica sérovar Typhimurium, un pathogène d’origine alimentaire qui, comme beaucoup de bactéries, porte plusieurs prophages dans son chromosome. Des travaux antérieurs avaient montré qu’un prophage nommé Gifsy‑1 aide Salmonella à résister à certains phages. Ici, l’équipe a découvert un gène de défense supplémentaire sur Gifsy‑1, appelé hepS, qui rend les bactéries beaucoup moins vulnérables à un groupe de phages à longue queue connus sous le nom de Siphoviridae. Lorsque hepS était supprimé, les phages envahisseurs formaient beaucoup plus de plaques — zones claires de cellules mortes — révélant que HepS réduit fortement les infections réussies et qu’il agit indépendamment d’autres défenses connues sur le même prophage.
Un système d’autosacrifice qui ne s’active qu’en cas d’attaque
HepS appartient à une famille de protéines qui servent souvent de « dernier rempart » moléculaire : lorsqu’elles détectent une infection, elles arrêtent des processus cellulaires essentiels de sorte que la cellule et le virus périssent. Les chercheurs ont montré que HepS se comporte ainsi — un système d’infection avortée — protégeant la population bactérienne globale en sacrifiant les cellules individuelles infectées. Des études structurales ont révélé que HepS s’assemble naturellement en un complexe à quatre parties (un tétramère) dont les centres actifs sont enfouis et mal alignés, suggérant un état « éteint » sûr pour l’hôte. La surproduction de HepS dans les bactéries n’entravait pas la croissance, ce qui soutient l’idée que la protéine reste inoffensive jusqu’à ce qu’elle soit déclenchée précisément.
Comment les pointes de queue des phages déclenchent l’interrupteur moléculaire
Pour savoir ce qui active HepS, l’équipe a mis au défi des bactéries portant hepS avec de nombreux phages différents et a constaté que la plupart des virus sensibles partageaient des protéines de pointe de queue similaires, les parties qui reconnaissent et percent la surface bactérienne. En sélectionnant des phages rares « échappés » capables de croître malgré HepS, ils ont relié la résistance à des changements d’un seul acide aminé dans un court segment de la protéine de pointe de queue, appelée J. L’expression de ce fragment J à l’intérieur des cellules rendait soudain HepS toxique, mais la variante échappée ne le faisait plus. Des expériences biochimiques ont confirmé que HepS se lie directement à ce petit peptide J. Des structures cristallographiques à haute résolution ont montré que, une fois le peptide arrimé sur chaque sous‑unité du tétramère HepS, l’ensemble du complexe se réarrange : les sites actifs s’ouvrent et s’alignent, convertissant HepS en une enzyme puissante de clivage de l’ARN.
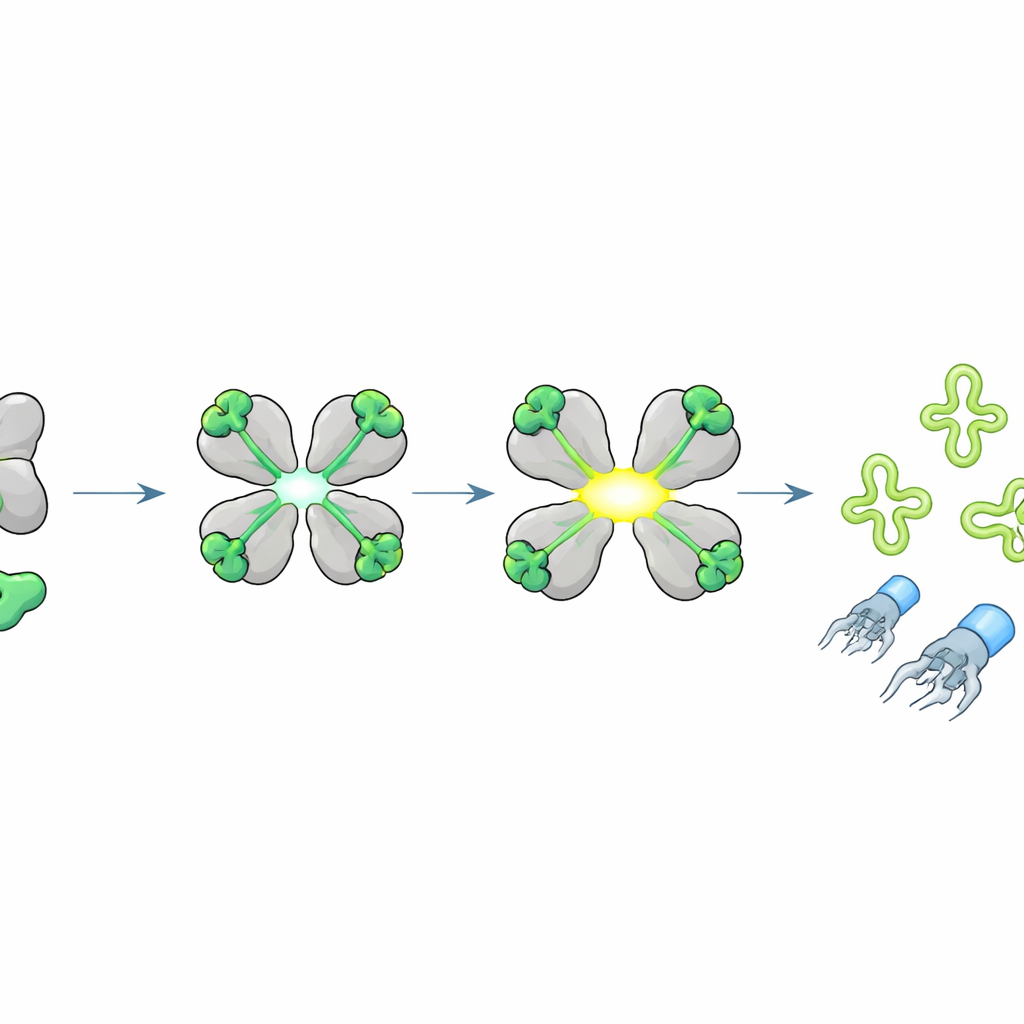
Couper des ARNt clés pour ralentir la production virale
Que coupe HepS activé ? Les chercheurs ont observé que, lorsque le peptide J activait HepS, l’ARN cellulaire se fragmentait en morceaux caractéristiques. En utilisant un séquençage spécialisé ciblant les ARN de transfert (ARNt) — les adaptateurs qui lisent le code génétique lors de la synthèse protéique — ils ont trouvé que HepS tranche des ARNt spécifiques exactement au niveau de leur boucle anticodon, en particulier ceux pour les acides aminés thréonine, isoleucine et sérine. La modélisation structurale a suggéré comment un tétramère HepS ouvert peut accueillir un ARNt cible et positionner ses résidus catalytiques précisément au niveau de l’anticodon. La destruction de ces ARNt prive la cellule de blocs constitutifs essentiels à la synthèse protéique, interrompant brusquement la production des protéines virales et bloquant l’assemblage de particules phagiques complètes, même si la réplication de l’ADN viral peut encore se produire.
Comment le prophage résident évite les tirs amis
Une énigme centrale est de savoir pourquoi Gifsy‑1, qui code pour HepS, n’est pas tué par sa propre défense. La réponse tient encore à la protéine de pointe de queue. Les trois prophages Gifsy résidents chez Salmonella possèdent tous des protéines J étroitement apparentées aux versions déclencheuses de HepS, mais à la position critique où les phages activants portent une phénylalanine volumineuse, les protéines J de Gifsy portent une isoleucine plus douce. Les expériences ont montré que la J sauvage de Gifsy n’active pas HepS, tandis que des versions modifiées qui remplacent cette position par une phénylalanine l’activent soudainement, entraînant une perte quasi totale des particules de Gifsy‑1 — mais seulement lorsque hepS est présent. Lors d’infections mixtes, lorsque Gifsy‑1 coexiste avec un prophage activant comme ES18, HepS handicape préférentiellement ES18 tout en affectant seulement modestement Gifsy‑1, donnant ainsi un avantage compétitif au prophage codant HepS pour produire de nouvelles particules et se propager vers de nouveaux hôtes.
Ce que cela signifie pour les bactéries, les virus et nous
Dans l’ensemble, ce travail dévoile une stratégie de survie finement réglée : un prophage arme son hôte Salmonella d’une protéine piégée qui détecte une marque caractéristique de virus envahisseurs apparentés, puis détruit la machinerie de production protéique de la cellule en découpant des ARNt sélectionnés. Ce geste sacrificiel arrête le cycle de vie de l’envahisseur et protège la communauté bactérienne élargie, tandis que des changements subtils dans la propre protéine de pointe du prophage lui permettent d’éviter son propre piège et de continuer à se répliquer. L’étude met en lumière le fait que les virus intégrés aux génomes bactériens ne se contentent pas de rester dormants — ils façonnent activement les batailles contre d’autres virus, influençant quelles souches de bactéries et de phages prospèrent dans les écosystèmes microbien.
Citation: Sargen, M.R., Antine, S.P., Grabe, G.J. et al. A prophage-encoded abortive infection protein preserves host and prophage spread. Nature 652, 201–208 (2026). https://doi.org/10.1038/s41586-025-10070-6
Mots-clés: défense contre les bactériophages, prophage, infection avortée, nucléase d’ARNt, interactions phage–Salmonella