Clear Sky Science · es
Una proteína de abortivo de infección codificada por un profago preserva al hospedador y la propagación del profago
Cómo las bacterias usan pasajeros ocultos para combatir virus
Las bacterias están constantemente bajo ataque por virus llamados fagos, y sin embargo muchas sobreviven gracias a pequeños polizones genéticos conocidos como profagos: virus latentes integrados en su ADN. Este estudio revela cómo uno de esos profagos equipa a la Salmonella con un potente interruptor de autodestrucción que detiene a los virus invasores, mientras permite que el propio profago siga propagándose. Comprender este tira y afloja molecular ayuda a explicar cómo patógenos peligrosos se mantienen un paso por delante de sus propios depredadores.
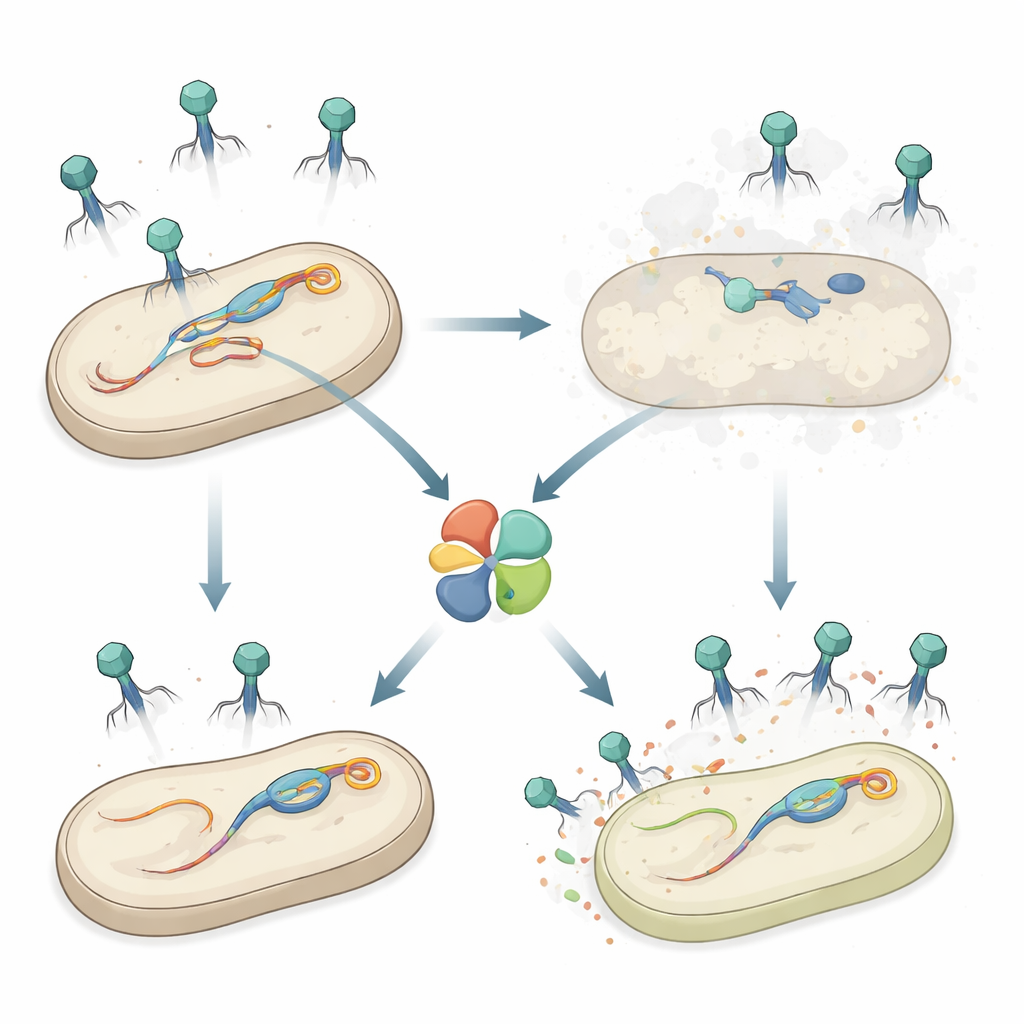
Un arma secreta dentro de Salmonella
Los autores estudiaron Salmonella enterica serovar Typhimurium, un patógeno transmitido por alimentos que, como muchas bacterias, porta varios profagos en su cromosoma. Trabajos previos mostraron que un profago llamado Gifsy‑1 ayuda a Salmonella a resistir el ataque de ciertos fagos. Aquí, el equipo descubrió un gen de defensa adicional en Gifsy‑1, llamado hepS, que hace a las bacterias mucho menos vulnerables a un grupo de fagos de cola larga conocidos como Siphoviridae. Cuando se eliminó hepS, los fagos invasores formaron muchas más placas —zonas claras de células muertas—, lo que reveló que HepS reduce fuertemente las infecciones exitosas y que actúa de forma independiente a otras defensas conocidas en el mismo profago.
Un sistema de autolesión que solo despierta durante el ataque
HepS pertenece a una familia de proteínas que a menudo funcionan como “últimos recursos”: cuando detectan infección, cierran procesos celulares esenciales de modo que tanto la célula como el virus mueren. Los investigadores demostraron que HepS se comporta de esta manera —un sistema de infección abortiva—, protegiendo a la población bacteriana en conjunto mediante el sacrificio de células individuales infectadas. Estudios estructurales revelaron que HepS se ensambla de forma natural en un complejo de cuatro partes (un tetrámero) cuyos centros activos están enterrados y mal alineados, lo que sugiere un estado “apagado” seguro para el hospedador. La sobreproducción de HepS en bacterias no obstaculizó el crecimiento, apoyando la idea de que la proteína permanece inofensiva hasta que se desencadena con precisión.
Cómo las puntas de la cola del fago giran el interruptor molecular
Para saber qué activa a HepS, el equipo desafió bacterias portadoras de hepS con muchos fagos diferentes y encontró que la mayoría de los virus susceptibles compartían proteínas similares en la punta de la cola, las partes que reconocen y perforan la superficie bacteriana. Al seleccionar fagos raros “escapistas” que podían crecer a pesar de HepS, trazaron la resistencia a cambios de un solo aminoácido en un segmento corto de la proteína de la punta de la cola, llamada J. Expresar este fragmento J dentro de las células volvió a HepS tóxico, pero la variante escapista ya no lo hizo. Experimentos bioquímicos confirmaron que HepS une directamente a este pequeño péptido J. Estructuras cristalinas de alta resolución mostraron que, una vez que el péptido se acopla a cada subunidad del tetrámero de HepS, todo el complejo se reordena: los sitios activos se abren y se alinean, convirtiendo a HepS en una potente enzima cortadora de ARN.
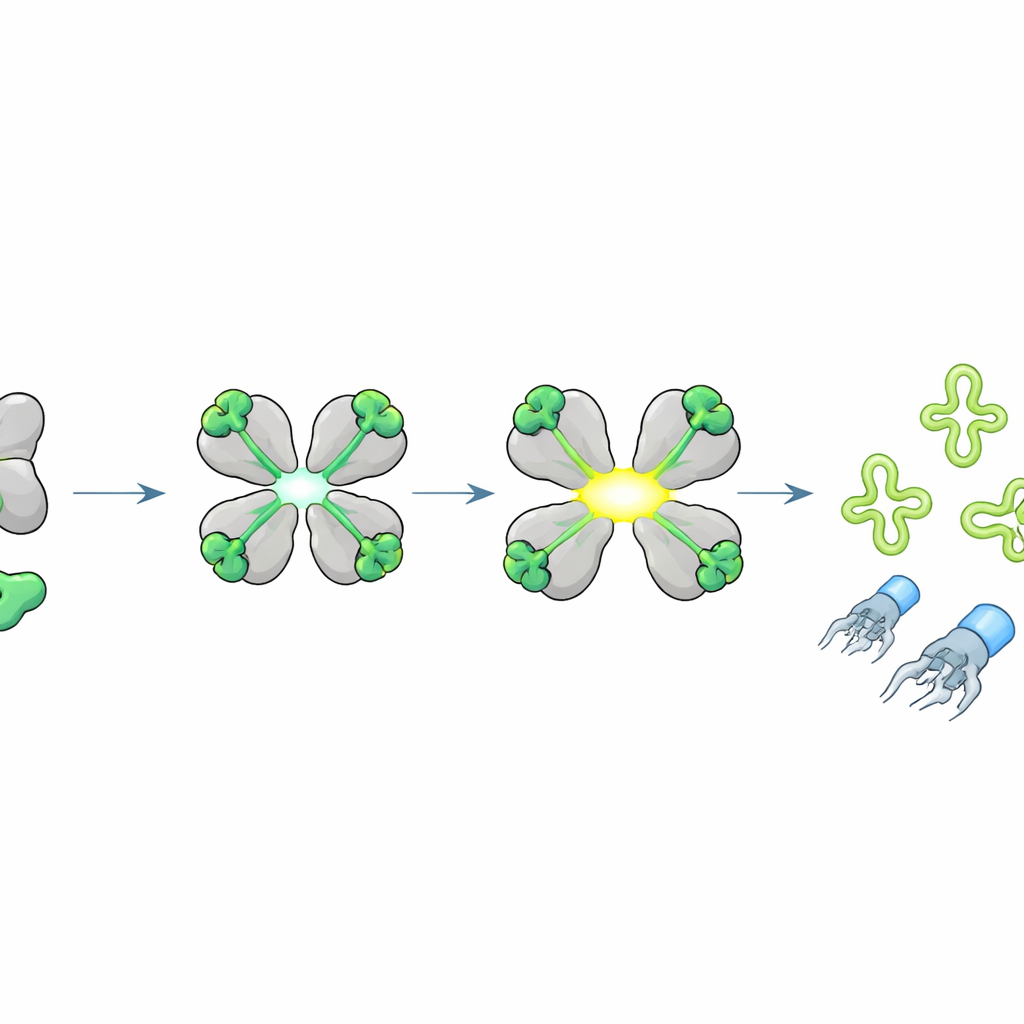
Cortando ARNt clave para frenar la producción viral
¿Qué corta HepS activado? Los investigadores observaron que, cuando el péptido J activó a HepS, el ARN celular se fragmentó en patrones característicos. Usando secuenciación especializada centrada en los ARN de transferencia (ARNt) —los adaptadores que leen el código genético durante la síntesis proteica— encontraron que HepS corta ARNt específicos exactamente en sus lazos anticodón, especialmente los correspondientes a los aminoácidos treonina, isoleucina y serina. Modelos estructurales sugirieron cómo un tetrámero de HepS abierto puede acunar un ARNt objetivo y posicionar sus residuos catalíticos justo en el anticodón. Destruir estos ARNt priva a la célula de bloques de construcción clave para la síntesis proteica, deteniendo abruptamente la producción de proteínas virales y bloqueando el ensamblaje de partículas completas de fago, aunque la replicación del ADN viral aún pueda ocurrir.
Cómo el profago residente evita el fuego amigo
Un enigma central es por qué Gifsy‑1, que codifica HepS, no es eliminado por su propia defensa. La respuesta recae de nuevo en la proteína de la punta de la cola. Los tres profagos residentes Gifsy en Salmonella tienen proteínas J estrechamente relacionadas con las versiones que activan HepS, pero en la posición crítica donde los fagos activadores llevan una fenilalanina voluminosa, las proteínas J de Gifsy llevan una isoleucina más moderada. Los experimentos mostraron que la J de Gifsy de tipo silvestre no activa HepS, mientras que versiones diseñadas que incorporan fenilalanina sí lo hacen, llevando a una pérdida casi total de partículas de Gifsy‑1 —pero solo cuando hepS está presente. En infecciones mixtas, cuando Gifsy‑1 coexiste con un profago activador como ES18, HepS paraliza preferentemente a ES18 mientras afecta solo modestamente a Gifsy‑1, otorgando al profago que codifica HepS una ventaja competitiva en la producción de nuevas partículas y su propagación a hospedadores nuevos.
Qué significa esto para bacterias, virus y para nosotros
En conjunto, este trabajo descubre una estrategia de supervivencia finamente sintonizada: un profago arma a su hospedador Salmonella con una proteína trampa que detecta una señal característica de virus invasores relacionados y luego destruye la propia maquinaria de producción de proteínas de la célula cortando ARNt selectos. Este movimiento sacrificial detiene el ciclo vital del invasor y protege a la comunidad bacteriana en general, mientras que cambios sutiles en la propia proteína de la punta de la cola del profago le permiten eludir su propia trampa y continuar replicándose. El estudio destaca cómo los virus incrustados en genomas bacterianos hacen más que permanecer latentes: moldean activamente las batallas contra otros virus, influyendo en qué cepas de bacterias y fagos prosperan en los ecosistemas microbianos.
Cita: Sargen, M.R., Antine, S.P., Grabe, G.J. et al. A prophage-encoded abortive infection protein preserves host and prophage spread. Nature 652, 201–208 (2026). https://doi.org/10.1038/s41586-025-10070-6
Palabras clave: defensa frente a bacteriófagos, profago, abortive infection, nucleasa de ARNt, interacciones de fagos con Salmonella