Clear Sky Science · pl
Białko przeciwko zakażeniom zakodowane przez profag chroni gospodarza i rozprzestrzenianie się profaga
Jak bakterie wykorzystują ukrytych pasażerów do walki z wirusami
Bakterie są ciągle atakowane przez wirusy zwane fagami, a mimo to wiele z nich przetrwa dzięki drobnym genetycznym pasażerom — profagom, czyli uśpionym wirusom wbudowanym w ich DNA. W tym badaniu pokazano, jak jeden z profagów wyposaża Salmonella w potężny „przycisk samowyzwalający”, który powstrzymuje atakujące wirusy, a jednocześnie pozwala samemu profagowi dalej się rozprzestrzeniać. Zrozumienie tej molekularnej rozgrywki pomaga wyjaśnić, jak groźne patogeny utrzymują przewagę nad własnymi drapieżnikami.
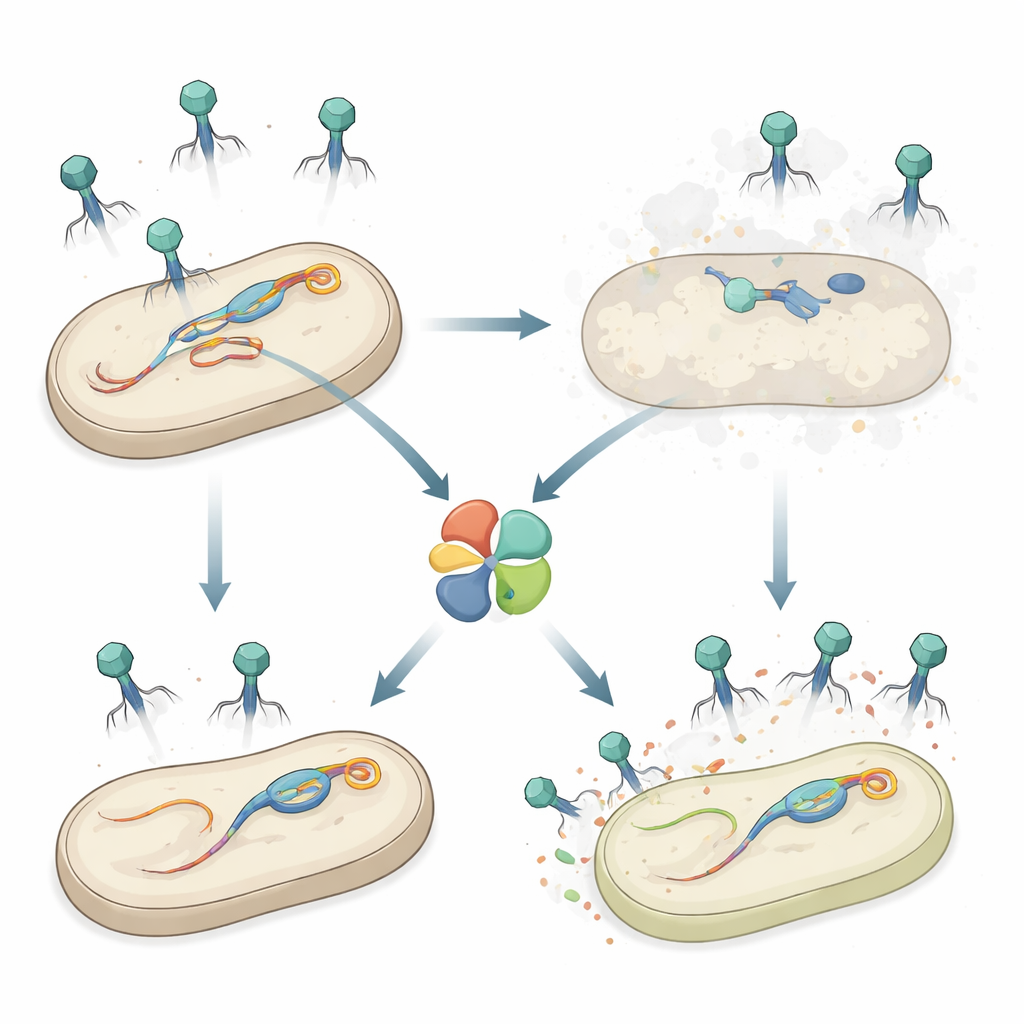
Tajemnicza broń w Salmonella
Autorzy badali Salmonella enterica serovar Typhimurium, patogen przenoszony przez żywność, który, jak wiele bakterii, nosi w chromosomie kilka profagów. Wcześniejsze prace wykazały, że jeden z profagów, nazwany Gifsy‑1, pomaga Salmonella przeciwstawiać się atakom niektórych fagów. Tutaj zespół odkrył dodatkowy gen obronny na Gifsy‑1, nazwany hepS, który znacząco zmniejsza podatność bakterii na grupę długosterowych fagów znanych jako Siphoviridae. Po usunięciu hepS atakujące fagi tworzyły znacznie więcej plamek (tzw. płytek) — przejrzystych ognisk martwych komórek — co pokazuje, że HepS silnie ogranicza udane zakażenia i działa niezależnie od innych znanych mechanizmów obronnych tego profaga.
System samopoświęcenia, który budzi się tylko przy ataku
HepS należy do rodziny białek, które często pełnią rolę molekularnych „ostatnich bastionów”: gdy wykrywają zakażenie, wyłączają niezbędne procesy komórkowe tak, że zarówno komórka, jak i wirus giną. Badacze wykazali, że HepS zachowuje się w ten sposób — jako system abortywnego zakażenia — chroniąc całą populację bakteryjną przez poświęcenie poszczególnych zainfekowanych komórek. Badania strukturalne ujawniły, że HepS naturalnie łączy się w czteroczęściowy kompleks (tetramer), którego centra aktywne są schowane i źle ustawione, co sugeruje stan „wyłączony” bezpieczny dla gospodarza. Nadmierna ekspresja HepS w komórkach nie hamowała wzrostu, co potwierdza, że białko pozostaje nieszkodliwe aż do precyzyjnego uruchomienia.
Jak końcówki ogonka faga przełączają molekularny łącznik
Aby ustalić, co aktywuje HepS, zespół wystawił bakterie niosące hepS na działanie wielu różnych fagów i odkrył, że większość wirusów wrażliwych miała podobne białka końcówek ogonka — części, które rozpoznają i przebijają powierzchnię bakterii. Selekcjonując rzadkie „uciekające” fagi, które potrafiły rosnąć mimo HepS, przypisano odporność pojedynczym zmianom aminokwasowym w krótkim fragmencie białka końcówki, zwanego J. Ekspresja tego fragmentu J wewnątrz komórek nagle uczyniła HepS toksycznym, podczas gdy wariant „uciekający” już nie. Eksperymenty biochemiczne potwierdziły bezpośrednie wiązanie HepS z tym małym peptydem J. Struktury krystaliczne o wysokiej rozdzielczości wykazały, że po zadokowaniu peptydu do każdej podjednostki tetrameru HepS cały kompleks reorganizuje się: centra aktywne otwierają się i ustawiają, przekształcając HepS w potężną enzymatyczną nukleazę RNA.
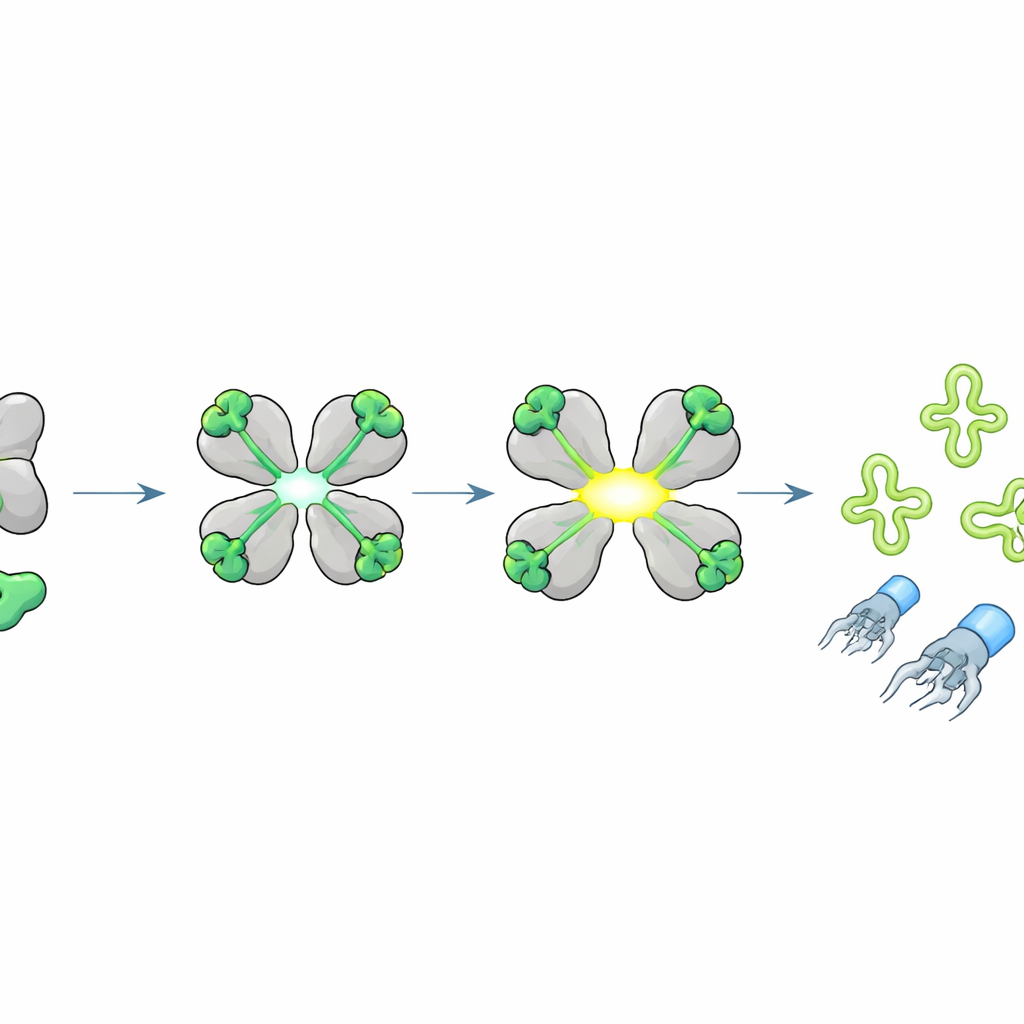
Cięcie kluczowych tRNA zatrzymuje produkcję wirusa
Czego tnie aktywowany HepS? Badacze zaobserwowali, że gdy peptyd J aktywował HepS, RNA komórki rozpadało się na charakterystyczne fragmenty. Przy użyciu specjalistycznego sekwencjonowania skoncentrowanego na transferowych RNA (tRNA) — adapterach odczytujących kod genetyczny podczas syntezy białek — odkryli, że HepS tnie specyficzne tRNA dokładnie w pętlach antykodonowych, szczególnie te dla aminokwasów treoniny, izoleucyny i seryny. Modelowanie strukturalne sugerowało, jak otwarty tetramer HepS może ułożyć docelowe tRNA i umieścić reszty katalityczne dokładnie nad antykodonem. Zniszczenie tych tRNA pozbawia komórkę kluczowych elementów do syntezy białek, gwałtownie zatrzymując produkcję białek wirusowych i blokując składanie pełnych cząstek faga, nawet jeśli replikacja DNA wirusa nadal może zachodzić.
Jak rezydujący profag unika ognia przyjaznego
Centralną zagadką jest to, dlaczego Gifsy‑1, który koduje HepS, nie zostaje zabity przez swoją własną obronę. Odpowiedź znów leży w białku końcówki ogonka. Trzy rezydujące profagi Gifsy w Salmonella mają białka J blisko spokrewnione z wariantami wyzwalającymi HepS, ale w krytycznej pozycji, gdzie aktywujące fagi mają masywną fenyloalaninę, białka J Gifsy niosą łagodniejszą izoleucynę. Eksperymenty wykazały, że dziki typ białka J Gifsy nie aktywuje HepS, podczas gdy skonstruowane wersje z podstawioną fenyloalaniną nagle to robią, prowadząc do niemal całkowitej utraty cząstek Gifsy‑1 — ale tylko kiedy hepS jest obecny. W mieszanych zakażeniach, gdy Gifsy‑1 współistnieje z aktywującym profagiem takim jak ES18, HepS preferencyjnie paraliżuje ES18, podczas gdy wpływ na Gifsy‑1 jest umiarkowany, dając profagowi kodującemu HepS przewagę konkurencyjną w produkcji nowych cząstek i rozprzestrzenianiu się do nowych gospodarzy.
Co to znaczy dla bakterii, wirusów i nas
Podsumowując, praca ta ujawnia dopracowaną strategię przetrwania: profag uzbraja swojego gospodarza Salmonella w pułapkowe białko, które rozpoznaje cechę charakterystyczną pokrewnych napadających wirusów, po czym niszczy urządzenie robocze komórki do produkcji białek, przecinając wybrane tRNA. Ten ofiarny zabieg zatrzymuje cykl życiowy intruza i chroni szerszą społeczność bakteryjną, podczas gdy subtelne zmiany we własnym białku końcówki profaga pozwalają mu prześlizgnąć się poza własną pułapkę i dalej replikować się. Badanie podkreśla, że wirusy osadzone w genomach bakteryjnych robią więcej niż tylko pozostają uśpione — aktywnie kształtują walki z innymi wirusami, wpływając na to, które szczepy bakterii i fagów dominują w ekosystemach mikrobiologicznych.
Cytowanie: Sargen, M.R., Antine, S.P., Grabe, G.J. et al. A prophage-encoded abortive infection protein preserves host and prophage spread. Nature 652, 201–208 (2026). https://doi.org/10.1038/s41586-025-10070-6
Słowa kluczowe: obrona przed bakteriofagami, profag, abortywne zakażenie, nukleaza tRNA, interakcje fag–Salmonella