Clear Sky Science · he
חלבון הפסקת זיהום המקודד על ידי פרופאייג' שומר על המארח ובהתפשטות הפרופאייג'
איך חיידקים משתמשים בנוסעים נסתרים כדי להלחם בוירוסים
חיידקים נתונים תמיד למתקפות של וירוסים הנקראים פאג'ים, אך רבים שורדים הודות ליוצאי דופן גנטיים זעירים המכונים פרופאייג'ים — וירוסים רדומים המוטמעים בדנ"א שלהם. המחקר הזה חושף כיצד פרופאייג' אחד מצייד את סלמונלה במתג השמדה עצמי חזק שמעצור וירוסים פולשים, וכל זאת תוך כדי שהפרופאייג' עצמו ממשיך להתפשט. הבנת מאבק המולקולות הזה מסבירה כיצד פתוגנים מסוכנים נשארים צעד אחד לפני הטורפים שלהם.
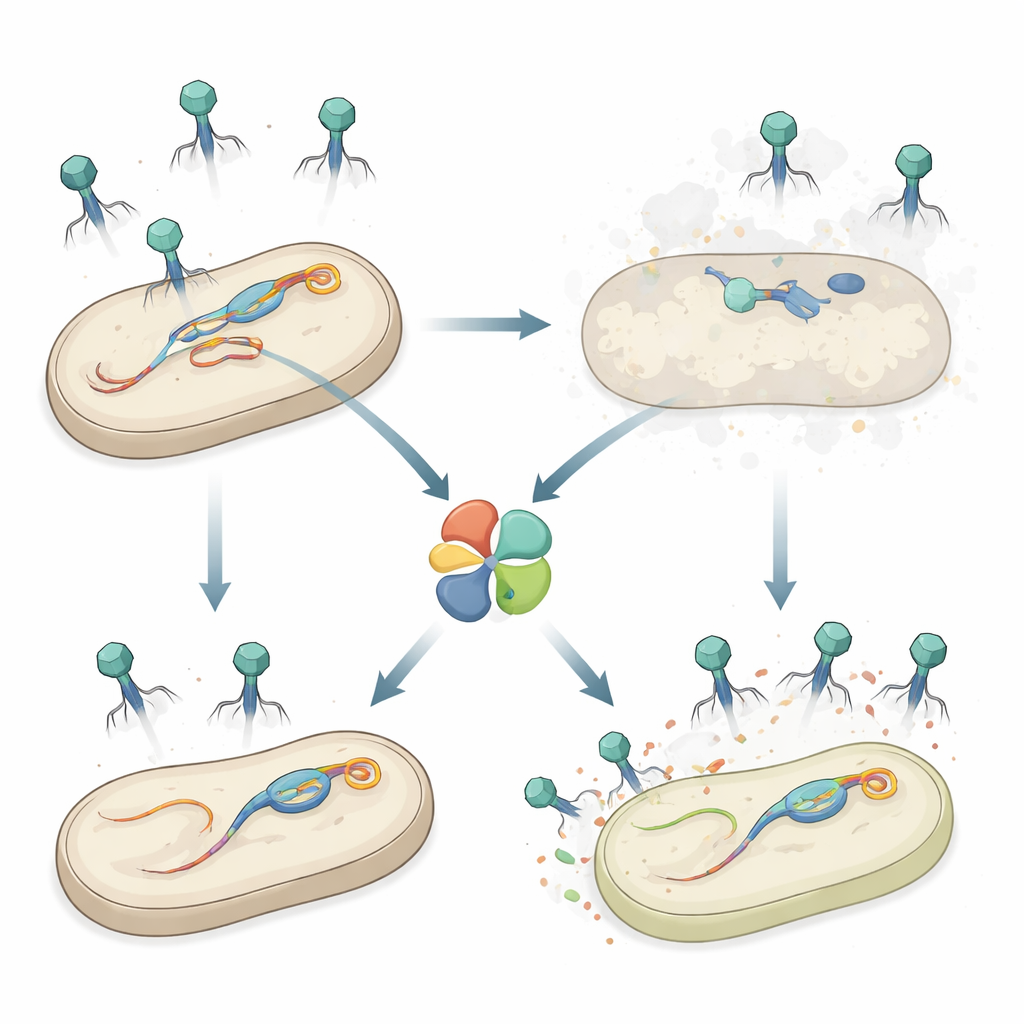
נשק סודי בתוך סלמונלה
המחברים חקרו Salmonella enterica סרובאר Typhimurium, פתוגן מועבר מזון שלחלק מהחיידקים יש מספר פרופאייג'ים בכרומוזום שלהם. עבודה קודמת הראתה שפרופאייג' אחד, שנקרא Gifsy‑1, מסייע לסלמונלה לעמוד בהתקפות מפאג'ים מסוימים. כאן גילו החוקרים גן הגנה נוסף על Gifsy‑1, בשם hepS, שהופך את החיידקים לפחות פגיעים לקבוצה של פאג'ים בעלי זנבות ארוכים הידועים כ‑Siphoviridae. כאשר hepS נמחק, הפאג'ים הפולשים יצרו הרבה יותר פלקות — נקודות נקיות של תאים מתים — מה שחשף כי HepS מקטין מאוד זיהומים מוצלחים, וכי הוא פועל באופן עצמאי מההגנות המוכרות האחרות באותו פרופאייג'.
מערכת הקרבה עצמית שמתעוררת רק בהתקפה
HepS שייך למשפחה של חלבונים שממלאים לעתים קרובות תפקיד של "עמידה אחרונה" מולקולרית: כאשר הם חשים זיהום, הם סוגרים תהליכים תאיים חיוניים כך שגם התא וגם הוירוס ימותו. החוקרים הראו ש‑HepS מתנהג באופן זה — מערכת הפסקת זיהום — המגינה על האוכלוסייה החיידקית על ידי הקרבת תאים מזוהמים בודדים. מחקרים מבניים גילו ש‑HepS מתאחד באופן טבעי למבנה בן ארבעה חלקים (טטראמר) שעמדות הפעילות שלו חבויות ומעט מיושרות, מה שמעיד על מצב "כבוי" בטוח למארח. ייצור כמות גבוהה של HepS בחיידקים לא פגע בצמיחה, מה שתומך ברעיון שהחלבון נשאר בלתי מזיק עד שמופעל בדיוק.
איך קצות זנב הפאג' גורמים להפעלת המתג המולקולרי
כדי לגלות מה מפעיל את HepS, הצוות אתגר חיידקים נשאים של hepS עם פאג'ים שונים וגילה שרוב הווירוסים הרגישים שיתפו חלבונים דמויי קצה זנב דומים, אותם חלקים שמזהים ודוקרים את פני השטח החיידקי. באמצעות בחירת פאג'ים נדירים "נמלטים" שיכלו לגדול למרות HepS, הם עקבו אחרי ההתנגדות לשינויים של חומצת אמינו בודדת בקטע קצר של חלבון קצה הזנב, הקרוי J. הבעת קטע J זה בתוך תאים הפכה לפתע את HepS לרעיל, אך הווריאנט הנמלט כבר לא עשה זאת. ניסויים ביוכימיים אישרו ש‑HepS נקשר ישירות לפפטיד J הקטן הזה. מבני גביש ברזולוציה גבוהה הראו שברגע שהפפטיד נתפס על כל תת‑יחידה של הטטראמר של HepS, כל המורכבות מתארגנת מחדש: אתרי הפעילות נפתחים ומיושרים, והופכים את HepS לאנזים חותך RNA עוצמתי.
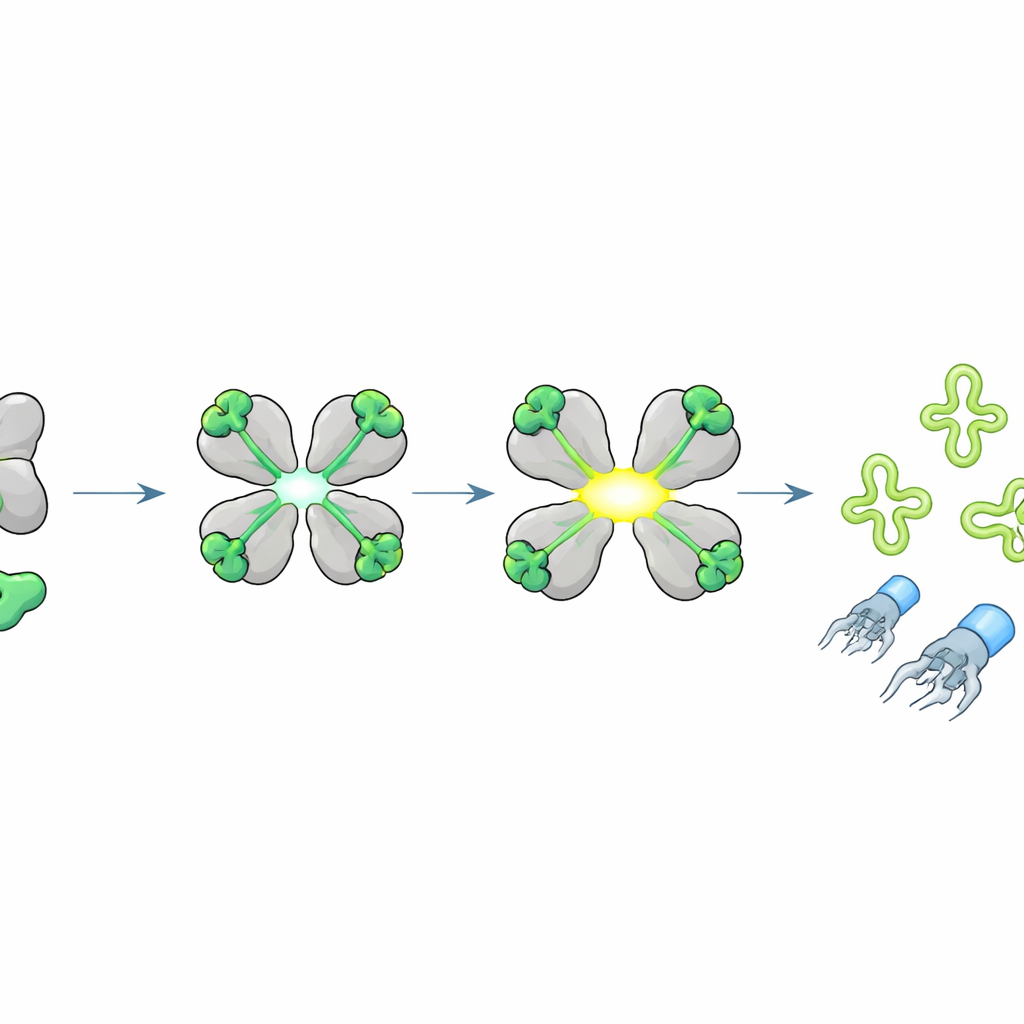
חיתוך tRNA מרכזיים כדי לעכב ייצור ויראלי
מה בדיוק HepS החתם חותך? החוקרים הבחינו שכאשר פפטיד J מפעיל את HepS, ה‑RNA התאי נשבר לחתיכות אופייניות. באמצעות ריצוף מיוחד המתמקד ב‑tRNA — המתאמים שקוראים את הקוד הגנטי בזמן הסינתזה החלבונית — הם מצאו ש‑HepS חותך tRNA ספציפיים בדיוק בלולאות האנטיקודון שלהם, במיוחד אלה של חומצות האמינו תראונין, איזולאוצין וסרין. דגמי מבנה הציעו איך טטראמר HepS הפתוח יכול לאחוז tRNA מטרה ולמקם את שאריות הקטליזה ממש בלולאת האנטיקודון. השמדת אותם tRNA מרעיבה את התא מבניינים חיוניים לתרגום חלבונים, ועוצרת באופן פתאומי ייצור חלבוני הוירוס ומנעת הרכבת חלקיקי פאג' שלמים, אף על פי ששכפול DNA הויראלי עשוי עדיין להתקיים.
איך הפרופאייג' החי בתוך התא נמנע מאש ידידותית
חידה מרכזית היא מדוע Gifsy‑1, שמקודד את HepS, אינו נהרג על ידי ההגנה שלו עצמו. התשובה שוב טמונה בחלבון קצה הזנב. שלושת פרופאייג'י Gifsy שגרתייים בסלמונלה כולם נושאים חלבוני J קרובים לאלו שמפעילים את HepS, אך במקום המיקום הקריטי שבו פאג'ים מפעילים נושאים פנילאלנין גדול, חלבוני J של Gifsy נושאים איזולאוצין עדין יותר. ניסויים הראו ש‑J הפראי של Gifsy אינו מפעיל את HepS, בעוד שווריאנטים מהונדסים שמחליפים פנילאלנין גורמים לפתאום להפעלה, מה שמוביל לאובדן כמעט מלא של חלקיקי Gifsy‑1 — אך רק כאשר hepS נוכח. בזיהומים מעורבים, כאשר Gifsy‑1 משתף מקום עם פרופאייג' מפעיל כמו ES18, HepS מפלה לטובת השבתת ES18 בעוד שהוא משפיע במידה מועטה יותר על Gifsy‑1, ומעניק לפרופאייג' המקודד HepS יתרון תחרותי בייצור חלקיקים חדשים ובהתפשטות למארחים טריים.
מסקנות לגבי חיידקים, וירוסים ואנחנו
ביחד, העבודה חושפת אסטרטגיית הישרדות מלוטשת: פרופאייג' מצייד את מארחו הסלמונלה בחלבון מלכודת שמזהה סימן היכר של וירוסים פולשים קרובים, ואז הורס את מכונת עשיית החלבונים של התא על‑ידי חיתוך tRNA נבחרים. המהלך ההקרבתי הזה עוצר את מחזור החיים של הפולש ומגן על הקהילה החיידקית הרחבה, בעוד ששינויים עדינים בחלבון קצה הזנב של הפרופאייג' עצמו מאפשרים לו לעבור את המלכודת ולהמשיך לשכפל. המחקר מדגיש שוירוסים הקבורים בגנומים חיידקיים עושים יותר משהם נמצאים במנוחה — הם מעצבים באופן פעיל קרבות נגד וירוסים אחרים ומשפיעים אילו זנים של חיידקים ופאג'ים שורדים ומצליחים במערכות המיקרוביאליות.
ציטוט: Sargen, M.R., Antine, S.P., Grabe, G.J. et al. A prophage-encoded abortive infection protein preserves host and prophage spread. Nature 652, 201–208 (2026). https://doi.org/10.1038/s41586-025-10070-6
מילות מפתח: הגנה מפאג'ים, פרופאייג', הפסקת זיהום (abortive infection), נוקלאז tRNA, אינטראקציות פאג'ים של סלמונלה