Clear Sky Science · it
Una proteina anti-infettiva codificata da un profago preserva l’ospite e la diffusione del profago
Come i batteri usano passeggeri nascosti per combattere i virus
I batteri sono costantemente sotto attacco da virus chiamati fagi, eppure molti sopravvivono grazie a piccoli occupanti genetici noti come profagi—virus dormienti integrati nel loro DNA. Questo studio rivela come uno di questi profagi fornisca a Salmonella un potente interruttore di autodistruzione che blocca i virus invasori, permettendo al contempo al profago stesso di continuare a diffondersi. Comprendere questa lotta molecolare aiuta a spiegare come agenti patogeni pericolosi rimangano un passo avanti rispetto ai loro predatori.
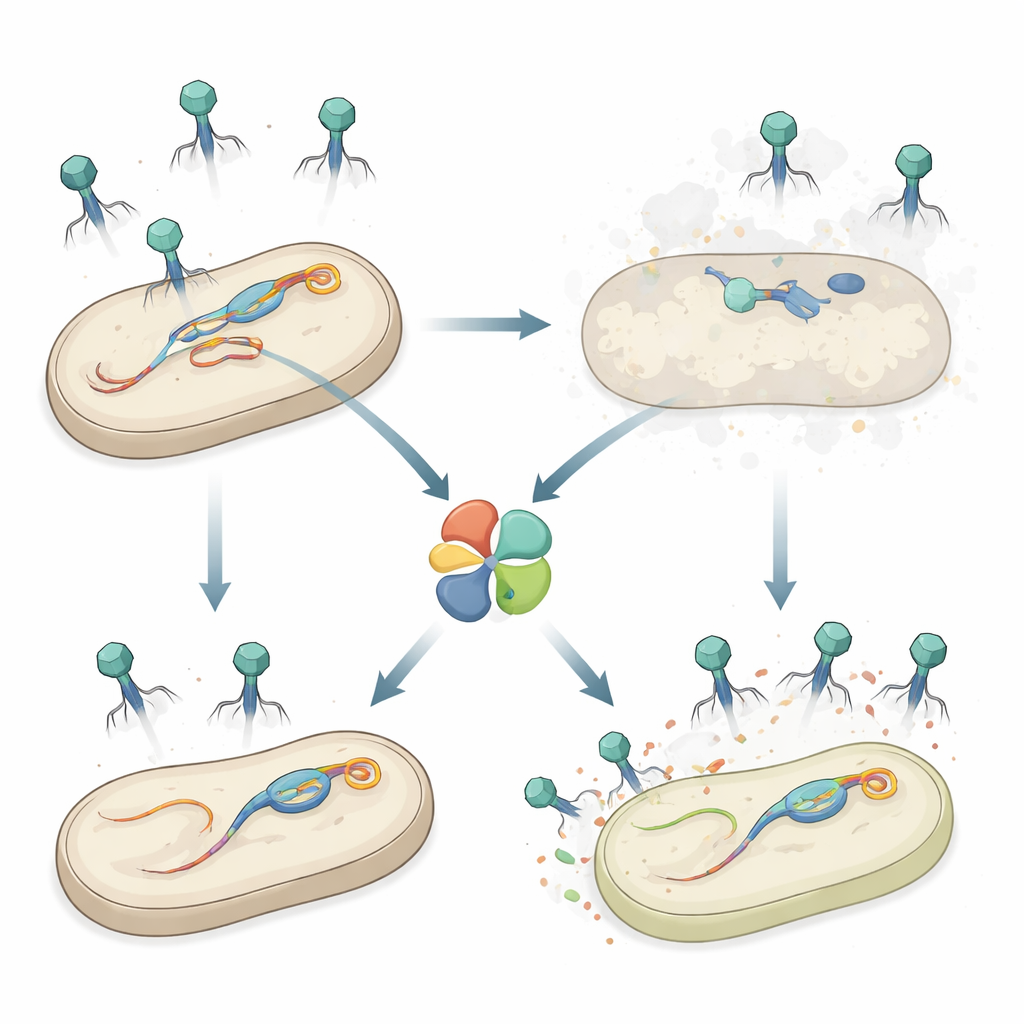
Un’arma segreta dentro Salmonella
Gli autori hanno studiato Salmonella enterica sierovar Typhimurium, un patogeno di origine alimentare che, come molti batteri, porta diversi profagi nel proprio cromosoma. Lavori precedenti avevano mostrato che un profago chiamato Gifsy‑1 aiuta Salmonella a resistere all’attacco di certi fagi. Qui, il gruppo ha scoperto un ulteriore gene di difesa su Gifsy‑1, denominato hepS, che rende i batteri molto meno vulnerabili a un gruppo di fagi a coda lunga noti come Siphoviridae. Quando hepS è stato eliminato, i fagi invasori hanno formato molte più placca—aree chiare di cellule morte—rivelando che HepS riduce fortemente le infezioni riuscite e che agisce in modo indipendente da altre difese note presenti nello stesso profago.
Un sistema di autosacrificio che si attiva solo durante l’attacco
HepS appartiene a una famiglia di proteine che spesso fungono da “ultima difesa” molecolare: quando rilevano l’infezione, spengono processi cellulari essenziali così che sia la cellula sia il virus muoiano. I ricercatori hanno dimostrato che HepS si comporta in questo modo—un sistema di abortive infection—proteggendo la popolazione batterica complessiva sacrificando le singole cellule infette. Studi strutturali hanno rivelato che HepS si assembla naturalmente in un complesso a quattro parti (tetramero) i cui centri attivi sono sepolti e poco allineati, suggerendo uno stato “spento” sicuro per l’ospite. La sovraespressione di HepS nei batteri non ha ostacolato la crescita, supportando l’idea che la proteina rimanga innocua fino a un preciso innesco.
Come le punte della coda del fago capovolgono l’interruttore molecolare
Per capire cosa attiva HepS, il team ha sfidato i batteri portatori di hepS con molti fagi diversi e ha scoperto che la maggior parte dei virus suscettibili condivideva proteine simili sulla punta della coda, le parti che riconoscono e perforano la superficie batterica. Selezionando rari fagi “evasori” in grado di crescere nonostante HepS, hanno ricondotto la resistenza a singole variazioni aminoacidiche in un breve segmento della proteina della punta della coda, chiamata J. L’espressione di questo frammento J all’interno delle cellule ha reso improvvisamente HepS tossico, mentre la variante evasiva non lo ha fatto. Esperimenti biochimici hanno confermato che HepS lega direttamente questo piccolo peptide J. Strutture cristallografiche ad alta risoluzione hanno mostrato che, una volta che il peptide si ancora su ciascun subunità del tetramero di HepS, l’intero complesso si riorganizza: i siti attivi si aprono e si allineano, convertendo HepS in un potente enzima che taglia RNA.
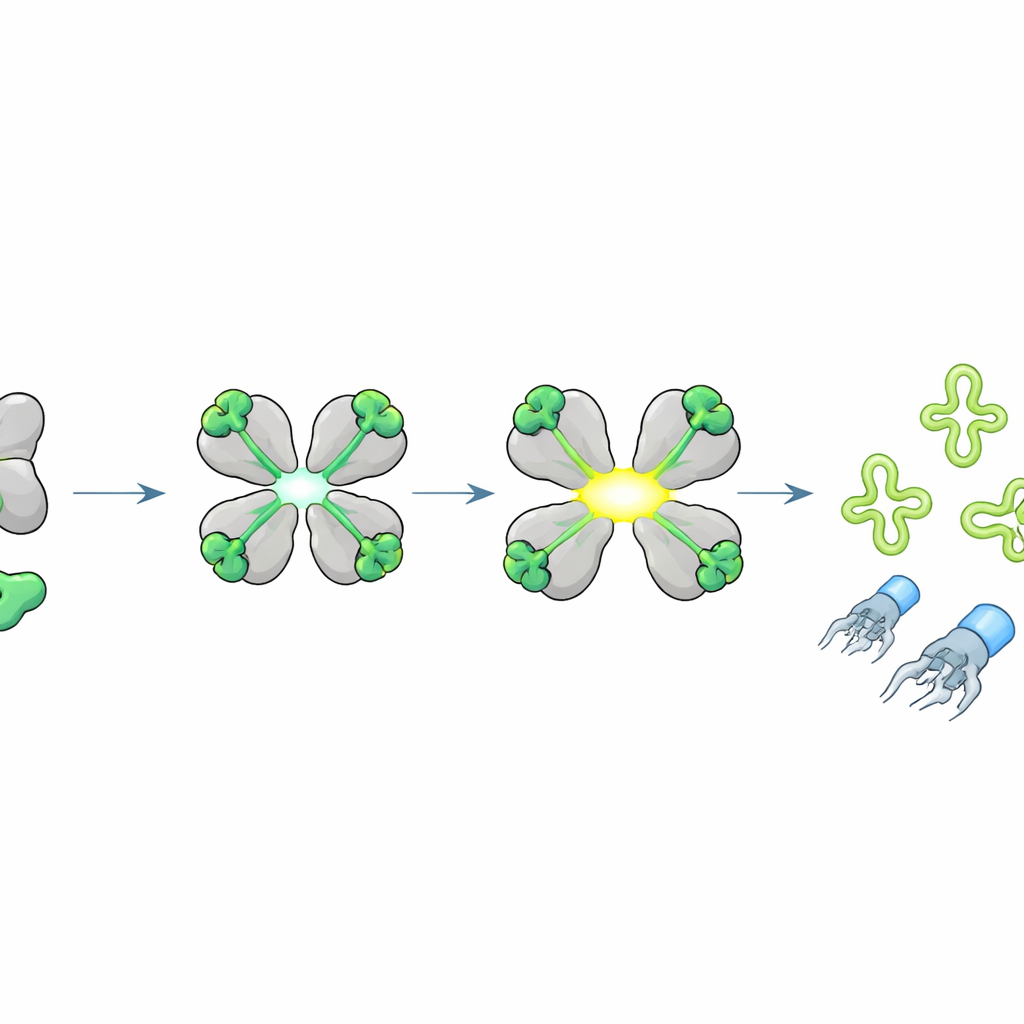
Tagliare tRNA chiave per arrestare la produzione virale
Cosa taglia HepS attivato? I ricercatori hanno osservato che, quando il peptide J attivava HepS, l’RNA cellulare si rompeva in frammenti caratteristici. Utilizzando un sequenziamento specializzato focalizzato sugli RNA di trasferimento (tRNA)—gli adattatori che leggono il codice genetico durante la sintesi proteica—hanno scoperto che HepS incide tRNA specifici esattamente nei loro anelli anticodone, in particolare quelli per gli amminoacidi treonina, isoleucina e serina. Modellizzazione strutturale ha suggerito come un tetramero di HepS aperto possa accogliere un tRNA bersaglio e posizionare i residui catalitici proprio sull’anticodone. La distruzione di questi tRNA priva la cellula di mattoni essenziali per la sintesi proteica, bloccando bruscamente la produzione di proteine virali e impedendo l’assemblaggio di particelle fagiche complete, anche se la replicazione del DNA virale può ancora avvenire.
Come il profago residente evita il fuoco amico
Un enigma centrale è perché Gifsy‑1, che codifica HepS, non venga eliminato dalla propria difesa. La risposta risiede nuovamente nella proteina della punta della coda. I tre profagi residenti Gifsy in Salmonella hanno tutti proteine J strettamente correlate a quelle che attivano HepS, ma nella posizione critica dove i fagi attivanti portano una fenilalanina ingombrante, le J di Gifsy portano una isoleucina più tenue. Gli esperimenti hanno mostrato che la J selvaggia di Gifsy non attiva HepS, mentre versioni ingegnerizzate che sostituiscono la fenilalanina lo fanno improvvisamente, portando a una quasi completa perdita delle particelle di Gifsy‑1—ma solo quando hepS è presente. In infezioni miste, quando Gifsy‑1 coesiste con un profago attivante come ES18, HepS danneggia preferenzialmente ES18 mentre influenza solo modestamente Gifsy‑1, conferendo al profago che codifica HepS un vantaggio competitivo nella produzione di nuove particelle e nella diffusione a nuovi ospiti.
Cosa significa per batteri, virus e per noi
Complessivamente, questo lavoro scopre una strategia di sopravvivenza finemente sintonizzata: un profago arma il suo ospite Salmonella con una proteina-trappola che riconosce un tratto caratteristico di virus invasori correlati, quindi distrugge la macchina cellulare per la produzione proteica tagliando tRNA selezionati. Questa mossa sacrifica la cellula per fermare il ciclo vitale dell’invasore e proteggere la comunità batterica più ampia, mentre sottili cambiamenti nella proteina della punta della coda del profago gli permettono di eludere la propria trappola e continuare a replicarsi. Lo studio mette in evidenza come i virus integrati nei genomi batterici facciano molto più che restare dormienti—plasmano attivamente le battaglie contro altri virus, influenzando quali ceppi di batteri e fagi prosperano negli ecosistemi microbici.
Citazione: Sargen, M.R., Antine, S.P., Grabe, G.J. et al. A prophage-encoded abortive infection protein preserves host and prophage spread. Nature 652, 201–208 (2026). https://doi.org/10.1038/s41586-025-10070-6
Parole chiave: difesa dai batteriofagi, profago, abortive infection, nucleasi tRNA, interazioni dei fagi con Salmonella