Clear Sky Science · de
Ein von einem Prophagen codiertes Abortive-Infection-Protein bewahrt Wirt und Prophagenverbreitung
Wie Bakterien versteckte Mitreisende zur Abwehr von Viren nutzen
Bakterien werden ständig von Viren, sogenannten Phagen, angegriffen, doch viele überleben dank winziger genetischer Mitbewohner, den Prophagen — ruhender Viren, die in ihr Erbgut eingebaut sind. Diese Studie zeigt, wie ein solcher Prophage Salmonella-Bakterien mit einem mächtigen Selbstzerstörungs‑Schalter ausstattet, der eindringende Viren stoppt, während sich der Prophage selbst weiterverbreiten kann. Das Verständnis dieses molekularen Tauziehens erklärt, wie gefährliche Krankheitserreger ihren eigenen Räubern einen Schritt voraus bleiben.
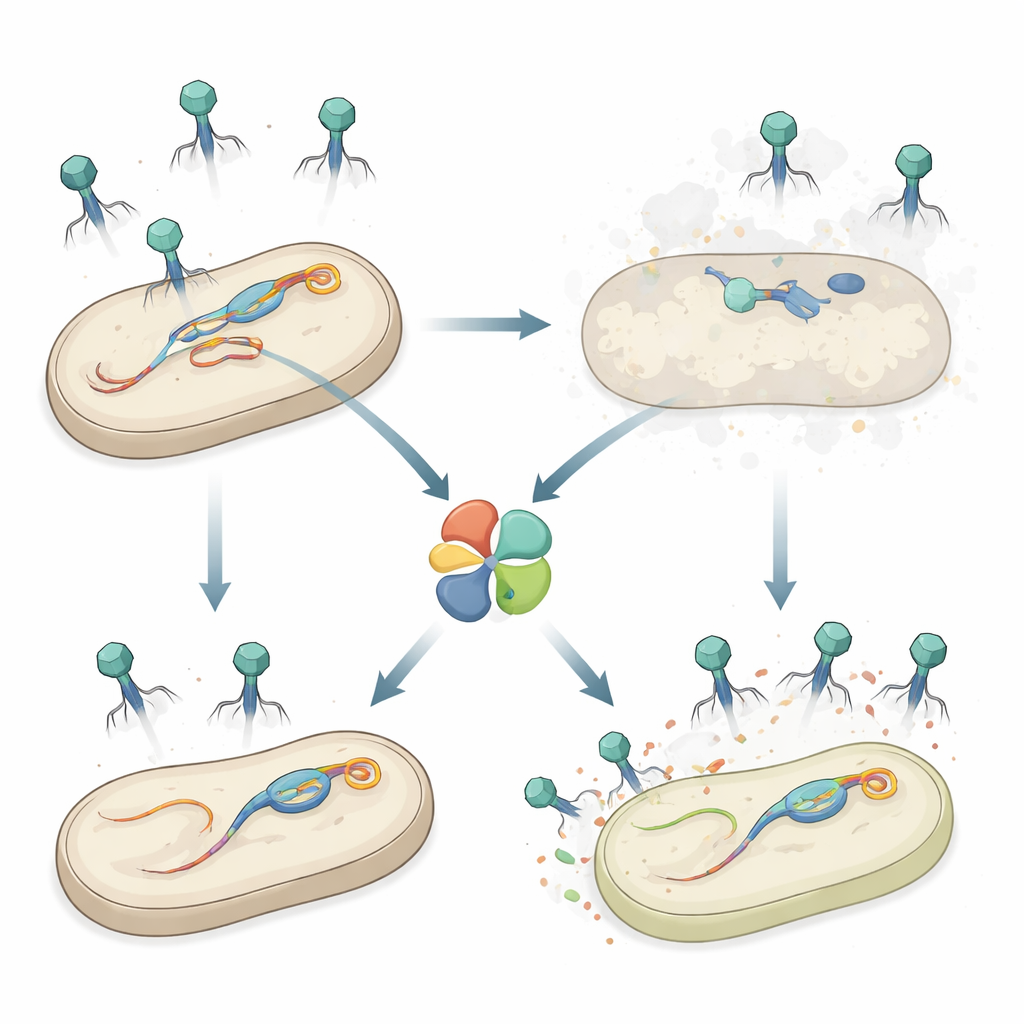
Eine Geheimwaffe in Salmonella
Die Autoren untersuchten Salmonella enterica Serovar Typhimurium, einen lebensmittelübertragenen Erreger, der wie viele Bakterien mehrere Prophagen im Chromosom trägt. Vorangehende Arbeiten zeigten, dass ein Prophage namens Gifsy‑1 Salmonella bei der Abwehr bestimmter Phagen unterstützt. Hier entdeckte das Team ein zusätzliches Abwehrgen auf Gifsy‑1, genannt hepS, das die Bakterien gegenüber einer Gruppe langschwänziger Phagen, den Siphoviridae, deutlich weniger anfällig macht. Wurde hepS entfernt, bildeten eindringende Phagen deutlich mehr Plaques — klare Flecken toter Zellen — was zeigt, dass HepS erfolgreiche Infektionen stark reduziert und unabhängig von anderen bekannten Abwehrsystemen desselben Prophagen wirkt.
Ein Selbstopfer-System, das nur bei Angriff aktiviert wird
HepS gehört zu einer Familie von Proteinen, die oft als molekulare „letzte Stände“ dienen: Sobald sie eine Infektion wahrnehmen, schalten sie essentielle Zellprozesse ab, sodass sowohl die Zelle als auch das Virus zugrunde gehen. Die Forschenden zeigten, dass HepS so funktioniert — als abortive-infection-System — und die Gesamtpopulation schützt, indem einzelne infizierte Zellen geopfert werden. Strukturelle Untersuchungen ergaben, dass HepS natürlicherweise zu einem vierteiligen Komplex (Tetramer) assembliert, dessen aktive Zentren vergraben und schlecht ausgerichtet sind, was einen sicheren „Aus“-Zustand für den Wirt nahelegt. Eine Überexpression von HepS hemmte das Wachstum der Bakterien nicht, was stützt, dass das Protein harmlos bleibt, bis es präzise ausgelöst wird.
Wie Phagen-Schwanzspitzen den molekularen Schalter umlegen
Um herauszufinden, was HepS aktiviert, konfrontierte das Team hepS-tragende Bakterien mit vielen verschiedenen Phagen und fand, dass die meisten empfindlichen Viren ähnliche Schwanzspitzenproteine teilen, jene Teile, die die bakterielle Oberfläche erkennen und durchstechen. Durch die Auswahl seltener „Entkommungs“-Phagen, die trotz HepS wachsen konnten, führten sie die Resistenz auf einzelne Aminosäureänderungen in einem kurzen Segment des Schwanzspitzenproteins namens J zurück. Die Expression dieses J‑Fragments in Zellen machte HepS plötzlich toxisch, die Entkommungsvariante jedoch nicht mehr. Biochemische Experimente bestätigten, dass HepS dieses kleine J‑Peptid direkt bindet. Hochauflösende Kristallstrukturen zeigten, dass nach Andocken des Peptids an jede Untereinheit des HepS‑Tetramers der gesamte Komplex umorganisiert: Die aktiven Stellen schlagen auf und richten sich aus, wodurch HepS in ein potentes RNA-schneidendes Enzym verwandelt wird.
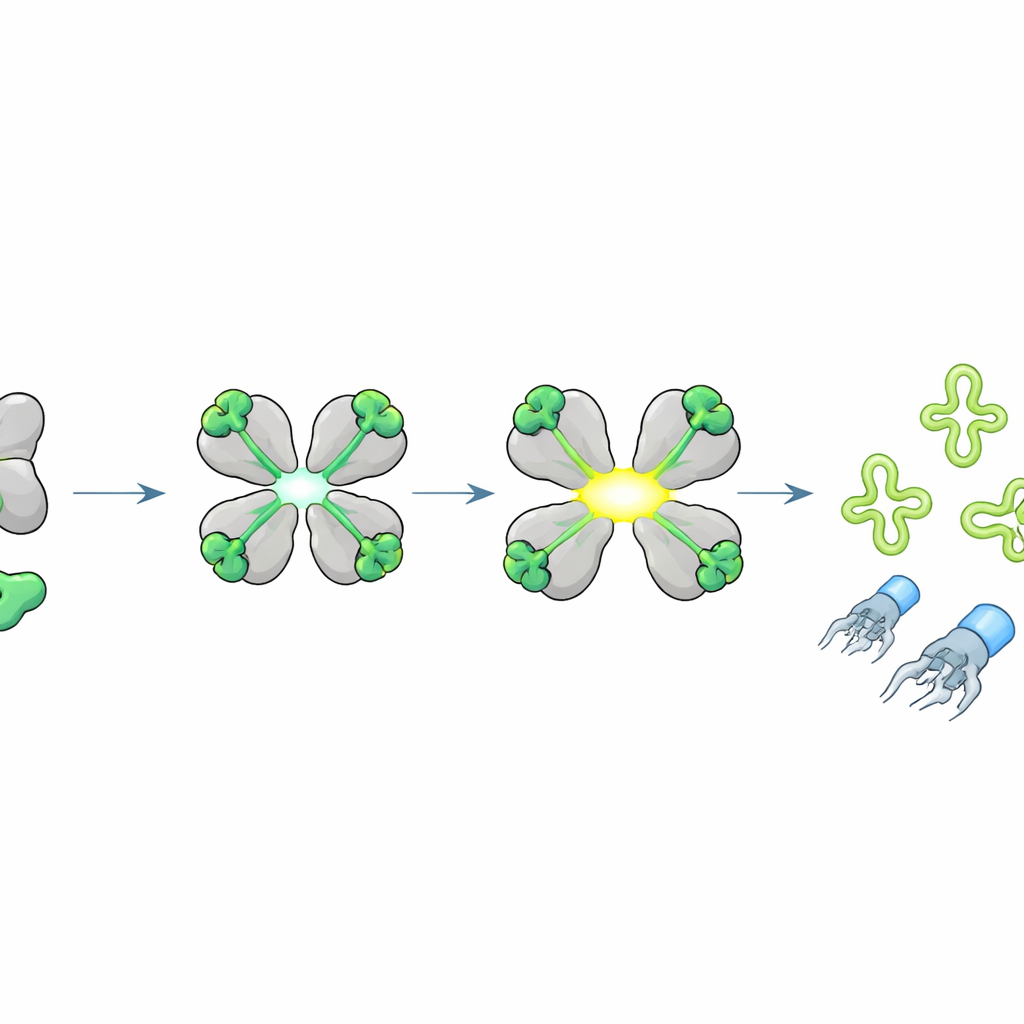
Wichtige tRNAs zerschneiden, um die Virenproduktion zu stoppen
Was schneidet aktiviertes HepS? Die Forschenden beobachteten, dass bei Aktivierung durch das J‑Peptid die zelluläre RNA in charakteristische Fragmente zerfiel. Mit spezieller Sequenzierung, die sich auf Transfer‑RNAs (tRNAs) konzentrierte — die Adapter, die beim Proteinaufbau den genetischen Code lesen — fanden sie, dass HepS bestimmte tRNAs genau in ihren Anticodon‑Schleifen schneidet, besonders jene für die Aminosäuren Threonin, Isoleucin und Serin. Strukturelle Modellierung legte nahe, wie ein geöffnetes HepS‑Tetramer eine Ziel‑tRNA umschließen und seine katalytischen Reste genau an das Anticodon positionieren kann. Die Zerstörung dieser tRNAs beraubt die Zelle wichtiger Bausteine der Proteinsynthese, stoppt abrupt die Produktion viraler Proteine und verhindert die Montage kompletter Phagenpartikel, obwohl die Replikation viraler DNA weiterhin stattfinden kann.
Wie der ansässige Prophage eigener Kollateralschäden entgeht
Ein zentrales Rätsel ist, warum Gifsy‑1, das HepS kodiert, nicht von seiner eigenen Abwehr getötet wird. Die Antwort liegt erneut im Schwanzspitzenprotein. Die drei in Salmonella residierenden Gifsy‑Prophagen besitzen alle J‑Proteine, die den HepS‑aktivierenden Versionen naheverwandt sind, aber an der kritischen Position, an der aktivierende Phagen eine sperrige Phenylalanin‑Restgruppe tragen, haben die Gifsy‑J‑Proteine ein milderes Isoleucin. Experimente zeigten, dass das Wildtyp‑Gifsy‑J HepS nicht aktiviert, während künstlich veränderte Versionen, in denen Phenylalanin eingesetzt wurde, dies plötzlich tun und nahezu zum Verlust von Gifsy‑1‑Partikeln führen — jedoch nur, wenn hepS vorhanden ist. Bei Mischinfektionen, in denen Gifsy‑1 mit einem aktivierenden Prophagen wie ES18 koexistiert, schwächt HepS bevorzugt ES18 stark und beeinträchtigt Gifsy‑1 nur mäßig, wodurch der HepS‑kodierende Prophage einen Wettbewerbsvorteil bei der Produktion neuer Partikel und der Ausbreitung auf neue Wirte erhält.
Was das für Bakterien, Viren und uns bedeutet
Insgesamt deckt diese Arbeit eine fein abgestimmte Überlebensstrategie auf: Ein Prophage rüstet seinen Salmonella‑Wirt mit einer Falle in Form eines Proteins aus, das ein Kennzeichen verwandter eindringender Viren erkennt und dann die eigene Proteinfabrik der Zelle durch gezieltes Zerschneiden ausgewählter tRNAs zerstört. Dieser opferbereite Zug stoppt den Lebenszyklus des Eindringlings und schützt die breitere bakterielle Gemeinschaft, während subtile Veränderungen im Schwanzspitzenprotein des Prophagen ihm erlauben, seiner eigenen Falle zu entkommen und weiter zu replizieren. Die Studie betont, dass in bakteriellen Genomen eingebettete Viren mehr tun als nur ruhen — sie prägen aktiv Kämpfe gegen andere Viren und beeinflussen, welche Stämme von Bakterien und Phagen in mikrobiellen Ökosystemen gedeihen.
Zitation: Sargen, M.R., Antine, S.P., Grabe, G.J. et al. A prophage-encoded abortive infection protein preserves host and prophage spread. Nature 652, 201–208 (2026). https://doi.org/10.1038/s41586-025-10070-6
Schlüsselwörter: Abwehr gegen Bakteriophagen, Prophage, abortive infection, tRNA-Nuklease, Interaktionen von Salmonella-Phagen