Clear Sky Science · nl
Een door een profaag gecodeerd abortief infectie-eiwit beschermt gastheer en de verspreiding van de profaag
Hoe bacteriën verborgen passagiers gebruiken om virussen te bestrijden
Bacteriën worden constant aangevallen door virussen die fagen worden genoemd, maar velen overleven dankzij kleine genetische aanhangsels die profagen heten—slapende virussen ingebed in hun DNA. Deze studie onthult hoe één dergelijke profaag Salmonella voorziet van een krachtig zelfvernietigingsmechanisme dat indringende virussen stopt, terwijl de profaag zelf toch kan blijven verspreiden. Het begrijpen van dit moleculaire touwtrekken helpt verklaren hoe gevaarlijke ziekteverwekkers hun eigen roofdieren vaak een stap voor blijven.
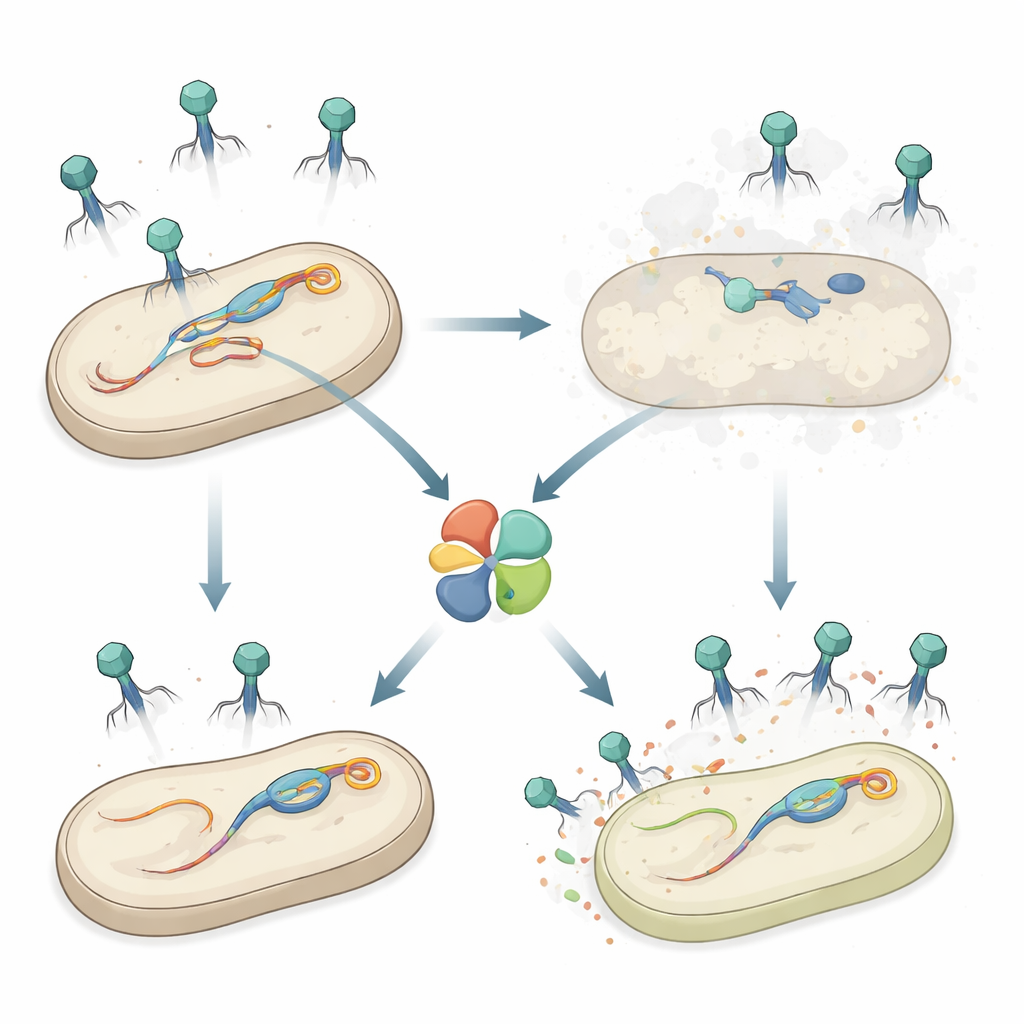
Een geheime wapen in Salmonella
De auteurs bestudeerden Salmonella enterica serovar Typhimurium, een voedselovergedragen pathogeen dat, net als veel bacteriën, meerdere profagen in zijn chromosoom draagt. Eerder werk toonde aan dat één profaag, Gifsy‑1 genoemd, Salmonella helpt bestand te zijn tegen bepaalde fagen. Hier ontdekte het team een extra verdedigingsgen op Gifsy‑1, hepS genoemd, dat de bacteriën veel minder kwetsbaar maakt voor een groep langstaartige fagen bekend als Siphoviridae. Wanneer hepS werd verwijderd, vormden indringende fagen veel meer plaques—heldere plekken van dode cellen—wat aantoont dat HepS succesvolle infecties sterk vermindert en dat het onafhankelijk werkt van andere bekende verdedigingsmechanismen in dezelfde profaag.
Een zelfopofferend systeem dat alleen bij aanval ontwaakt
HepS behoort tot een familie van eiwitten die vaak fungeren als moleculaire "laatste verdedigingslinie": wanneer ze een infectie waarnemen, schakelen ze essentiële celprocessen uit zodat zowel de cel als het virus sterven. De onderzoekers lieten zien dat HepS zich op deze manier gedraagt—een abortief infectiesysteem—en de algemene bacteriële populatie beschermt door individuele geïnfecteerde cellen op te offeren. Structurele studies toonden aan dat HepS van nature assembleert tot een viervoudig complex (een tetrameren) waarvan de actieve centra begraven en slecht uitgelijnd zijn, wat wijst op een veilige "uit"-toestand voor de gastheer. Overexpressie van HepS in bacteriën remde de groei niet, wat de gedachte ondersteunt dat het eiwit onschadelijk blijft totdat het precies wordt geactiveerd.
Hoe fagtipjes de moleculaire schakel omzetten
Om te achterhalen wat HepS activeert, daagde het team bacteriën met hepS uit met veel verschillende fagen en ontdekte dat de meeste gevoelige virussen vergelijkbare staarttip-eiwitten deelden, de onderdelen die het bacteriële oppervlak herkennen en doorboren. Door zeldzame "ontsnappings"-fagen te selecteren die konden groeien ondanks HepS, traceerden ze resistentie tot enkele aminozuurveranderingen in een kort segment van het staarttippoteïne, genoemd J. Expressie van dit J-fragment in cellen maakte HepS plotseling toxisch, terwijl de ontsnappingsvariant dat niet deed. Biochemische experimenten bevestigden dat HepS direct bindt aan dit kleine J-peptide. Röntgenkristalstructuren met hoge resolutie toonden dat, zodra het peptide op elk subunit van de HepS-tetramer dockt, het gehele complex zich herstructureert: de actieve plaatsen opengaan en uitlijnen, waarmee HepS wordt omgezet in een krachtige RNA-knippende enzym.
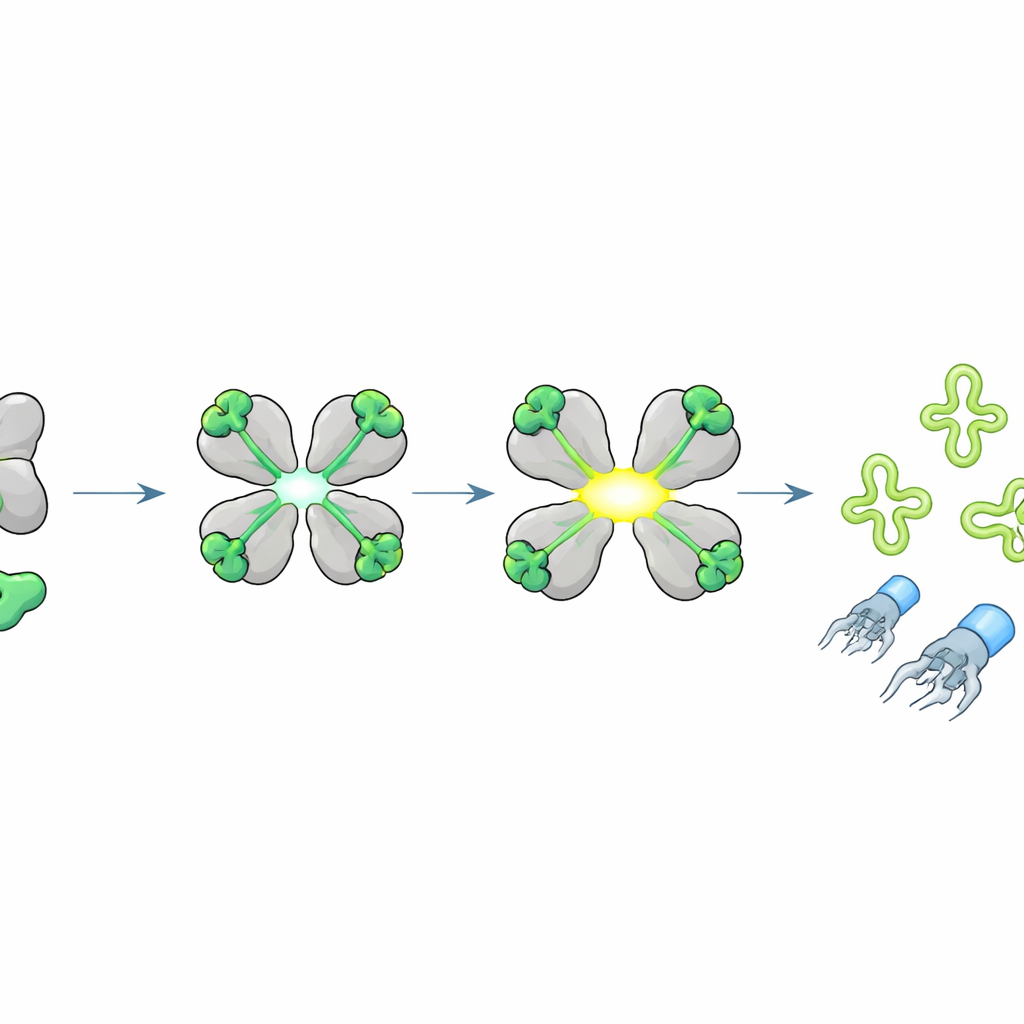
Belangrijke tRNA's doorknippen om virusproductie te stoppen
Wat knipt geactiveerde HepS? De onderzoekers zagen dat, wanneer het J-peptide HepS inschakelde, het RNA van de cel in karakteristieke fragmenten brak. Met gespecialiseerde sequencing gericht op transfer-RNA's (tRNA's)—de adapters die de genetische code lezen tijdens eiwitsynthese—vonden ze dat HepS specifieke tRNA's precies in hun anticodonlussen doorsnijdt, vooral die voor de aminozuren threonine, isoleucine en serine. Structurele modellering suggereerde hoe een geopende HepS-tetramer een doeltarget tRNA kan omvatten en zijn katalytische residuen precies bij het anticodon kan positioneren. Het vernietigen van deze tRNA's onthongert de cel van essentiële bouwstenen voor eiwitsynthese, wat abrupt de productie van virale eiwitten stillegt en de assemblage van complete fagedeeltjes blokkeert, ook al kan virale DNA-replicatie nog plaatsvinden.
Hoe de residentiële profaag vriendelijk vuur ontloopt
Een centraal raadsel is waarom Gifsy‑1, dat HepS codeert, niet wordt gedood door zijn eigen verdediging. Het antwoord ligt opnieuw in het staarttip-eiwit. De drie residentiële Gifsy-profagen in Salmonella hebben alle J-eiwitten die nauw verwant zijn aan de HepS-activerende versies, maar op de kritieke positie waar activerende fagen een omvangrijk fenylalanine dragen, bevatten de Gifsy J-eiwitten een mildere isoleucine. Experimenten toonden aan dat wildtype Gifsy J HepS niet activeert, terwijl geconstrueerde versies waarin fenylalanine werd ingebracht dat plotseling wel doen, wat leidt tot bijna volledig verlies van Gifsy‑1-deeltjes—maar alleen wanneer hepS aanwezig is. Bij gemengde infecties, wanneer Gifsy‑1 naast een activerende profaag zoals ES18 voorkomt, verlamt HepS ES18 bij voorkeur terwijl Gifsy‑1 slechts matig wordt getroffen, waardoor de HepS-coderende profaag een concurrentievoordeel krijgt bij het produceren van nieuwe deeltjes en het verspreiden naar nieuwe gastheren.
Wat dit betekent voor bacteriën, virussen en ons
Alles bij elkaar onthult dit werk een fijn afgestemde overlevingsstrategie: een profaag bewapent zijn Salmonella-gastheer met een hinderlaag-eiwit dat een kenmerk van verwante indringende virussen detecteert en vervolgens het eiwitmakerijmachinerie van de cel vernietigt door selecte tRNA's doormidden te snijden. Deze offeractie stopt de levenscyclus van de indringer en beschermt de bredere bacteriële gemeenschap, terwijl subtiele veranderingen in het eigen staarttip-eiwit van de profaag hem in staat stellen aan zijn eigen val te ontsnappen en te blijven repliceren. De studie benadrukt hoe in bacteriële genomen ingebedde virussen meer doen dan slapend liggen—ze vormen actief de strijd tegen andere virussen en beïnvloeden welke stammen van zowel bacteriën als fagen floreren in microbiële ecosystemen.
Bronvermelding: Sargen, M.R., Antine, S.P., Grabe, G.J. et al. A prophage-encoded abortive infection protein preserves host and prophage spread. Nature 652, 201–208 (2026). https://doi.org/10.1038/s41586-025-10070-6
Trefwoorden: verdediging tegen bacteriofagen, profaag, abortieve infectie, tRNA-nuclease, interacties tussen Salmonella en fagen