Clear Sky Science · ru
Белок, кодируемый профагом, прерывающий инфекцию, сохраняет хозяина и распространение профага
Как бактерии используют скрытых пассажиров против вирусов
Бактерии постоянно подвергаются атакам вирусов, называемых фагами, но многие выживают благодаря крошечным генетическим «попутчикам» — профагам, спящим вирусам, встроенным в их ДНК. В этом исследовании показано, как один такой профаг наделяет Salmonella мощным механизмом самоуничтожения, который останавливает вторгающиеся вирусы, одновременно позволяя самому профагу продолжать распространение. Понимание этой молекулярной борьбы помогает объяснить, как опасные патогены остаются на шаг впереди своих собственных хищников.
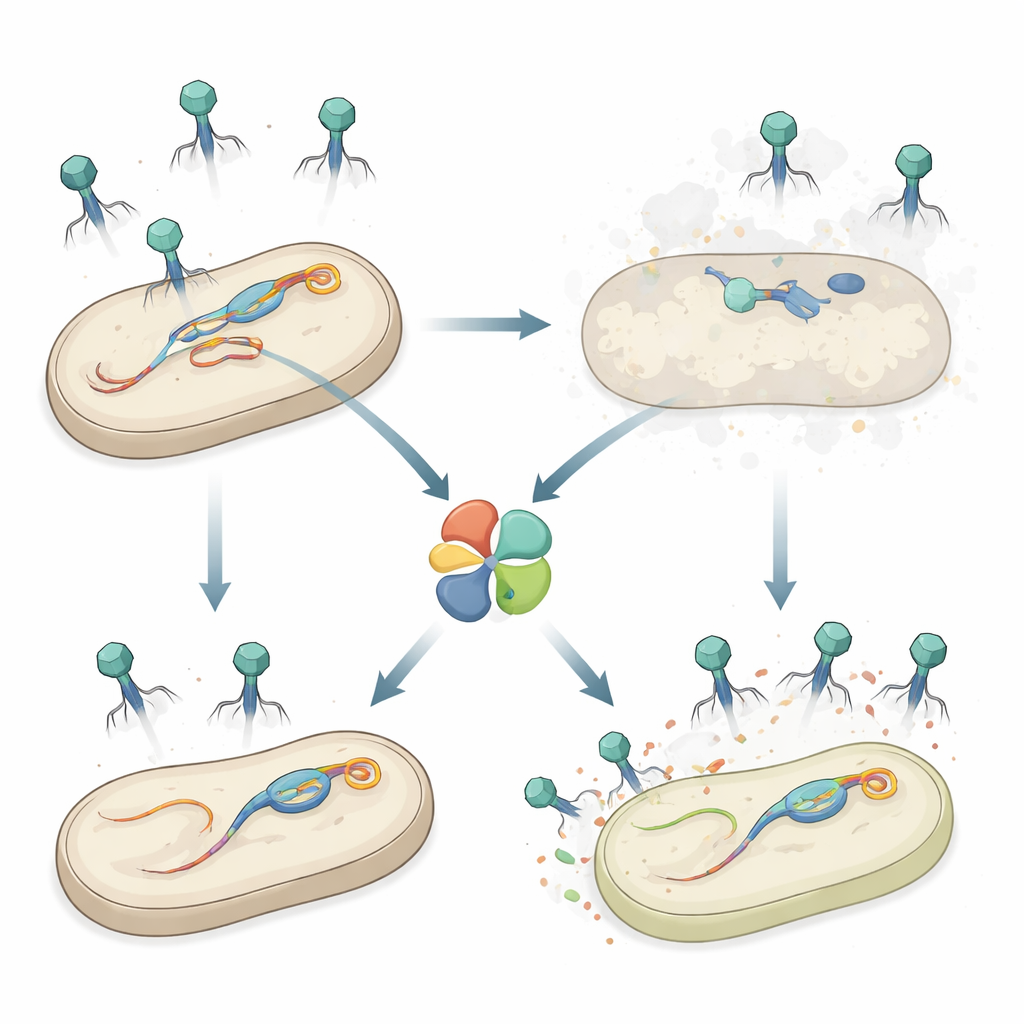
Секретное оружие внутри Salmonella
Авторы изучали Salmonella enterica серовар Typhimurium — пищевого происхождения патоген, который, как и многие бактерии, несет в хромосоме несколько профагов. Ранние работы показали, что один профаг, названный Gifsy‑1, помогает Salmonella сопротивляться атакам некоторых фагов. Здесь команда обнаружила дополнительный ген защиты на Gifsy‑1, названный hepS, который делает бактерии значительно менее уязвимыми к группе длиннохвостых фагов, известных как Siphoviridae. При удалении hepS вторгающиеся фаги образовывали намного больше бляшек — прозрачных зон мертвых клеток — что показало: HepS резко снижает успешность инфекций и действует независимо от других известных систем защиты на том же профаге.
Система самопожертвования, которая включается только при атаке
HepS принадлежит к семейству белков, часто выполняющих роль молекулярных «последних рубежей»: обнаружив инфекцию, они выключают жизненно важные клеточные процессы так, что погибают и клетка, и вирус. Исследователи показали, что HepS ведет себя именно так — как система прерывания инфекции — защищая популяцию бактерий путем жертвования отдельными зараженными клетками. Структурные исследования показали, что HepS естественным образом собирается в четырехмучный комплекс (тетрамер), чьи активные центры погружены и плохо сориентированы, что указывает на «выключенное» состояние, безопасное для хозяина. Переизбыточная экспрессия HepS в бактериях не мешала росту, что подтверждает идею о том, что белок остается безвредным до точного запуска.
Как наконечники хвостов фага переключают молекулярный механизм
Чтобы выяснить, что активирует HepS, команда испытывала бактерии с hepS против множества разных фагов и обнаружила, что большинство восприимчивых вирусов имеют сходные белки на концах хвостов — части, которые распознают и прокалывают поверхность бактерии. Отбирая редкие «сбегающие» фаги, которые могли расти несмотря на HepS, они проследили устойчивость до одиночных замен аминокислот в коротком сегменте белка наконечника хвоста, называемого J. Экспрессия этого фрагмента J внутри клеток внезапно делала HepS токсичным, тогда как вариант «сбегающего» фага этого не делал. Биохимические эксперименты подтвердили, что HepS непосредственно связывает этот маленький пептид J. Кристаллические структуры высокого разрешения показали, что как только пептид садится на каждый субъединицу тетрамера HepS, комплекс перестраивается: активные сайты раскрываются и выравниваются, превращая HepS в мощную энзимную RNase.
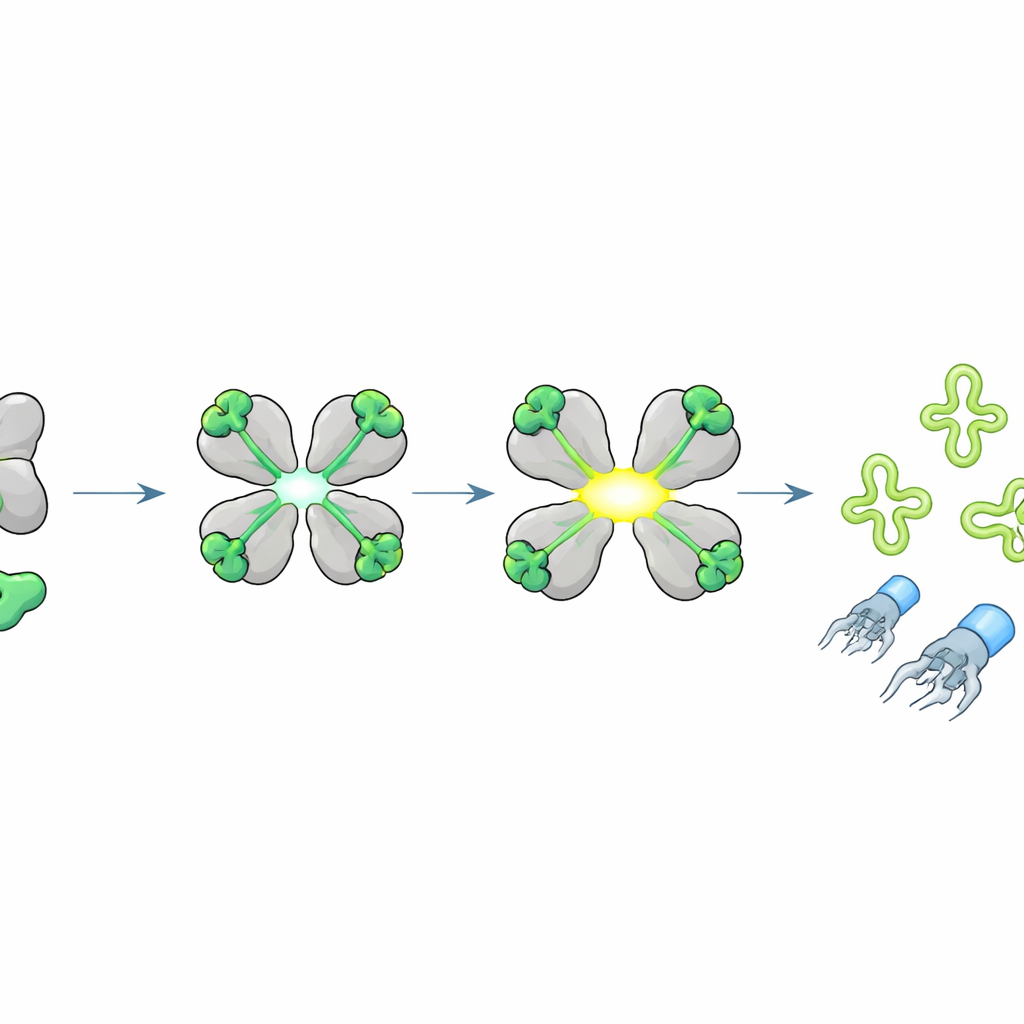
Резание ключевых tRNA, чтобы остановить производство вирусов
Что именно разрезает активированный HepS? Исследователи заметили, что при включении HepS пептидом J РНК клетки распадается на характерные фрагменты. Используя специализированное секвенирование, ориентированное на транспортные РНК (tRNA) — адаптеры, читающие генетический код при синтезе белка — они обнаружили, что HepS разрезает специфические tRNA точно в их антикодонных петлях, особенно для аминокислот треонина, изолейцина и серина. Структурное моделирование показало, как раскрытый тетрамер HepS может обхватывать целевую tRNA и располагать каталитические остатки прямо напротив антикодона. Разрушение этих tRNA лишает клетку ключевых компонентов для синтеза белка, внезапно останавливая производство вирусных белков и блокируя сборку завершенных фаговых частиц, хотя репликация вирусной ДНК при этом все еще может происходить.
Как резидентный профаг избегает «своего» огня
Ключевая загадка — почему Gifsy‑1, кодирующий HepS, сам не уничтожается собственным механизмом защиты. Ответ снова кроется в белке наконечника хвоста. Три резидентных профага Gifsy в Salmonella имеют белки J, близкие к версиям, активирующим HepS, но в критической позиции, где у активирующих фагов находится громоздкая фенилаланин, у Gifsy J стоит более мягкий изолейцин. Эксперименты показали, что дикий тип Gifsy J не активирует HepS, тогда как сконструированные версии с заменой на фенилаланин внезапно активируют его, что приводит к почти полному исчезновению частиц Gifsy‑1 — но лишь при наличии hepS. В смешанных инфекциях, когда Gifsy‑1 соседствует с активирующим профагом вроде ES18, HepS преимущественно калечит ES18, едва затрагивая Gifsy‑1, давая профагу, кодирующему HepS, конкурентное преимущество в продуцировании новых частиц и распространении на новых хозяев.
Что это означает для бактерий, вирусов и нас
В целом эта работа раскрывает тонко настроенную стратегию выживания: профаг вооружает своего хозяина Salmonella ловушечным белком, который распознает характерный элемент родственных вторгающихся вирусов и затем разрушает собственный механизм синтеза белка клетки, разрезая выборочные tRNA. Этот жертвенный ход останавливает жизненный цикл захватчика и защищает более широкое бактериальное сообщество, в то время как тонкие изменения в собственном белке наконечника профага позволяют ему проскакивать мимо собственной ловушки и продолжать репликацию. Исследование подчеркивает, что вирусы, встроенные в бактериальные геномы, делают больше, чем просто находятся в состоянии покоя — они активно формируют битвы с другими вирусами, влияя на то, какие штаммы бактерий и фагов процветают в микробных экосистемах.
Цитирование: Sargen, M.R., Antine, S.P., Grabe, G.J. et al. A prophage-encoded abortive infection protein preserves host and prophage spread. Nature 652, 201–208 (2026). https://doi.org/10.1038/s41586-025-10070-6
Ключевые слова: защита от бактериофагов, профаг, прерывание инфекции, нуклеаза tRNA, взаимодействия фага и Salmonella