Clear Sky Science · sv
Patogena varianter i cohesin-laddarens subenhet MAU2 ligger bakom en särskild undergrupp av Cornelia de Lange-syndromet
När en liten genförändring formar tillväxt och utveckling
Cornelia de Lange-syndrom är ett sällsynt tillstånd som påverkar tillväxt, ansiktsdrag och inlärning. För många familjer kvarstår orsaken som ett mysterium även efter genetisk testning. Denna studie fokuserar på en mindre känd gen kallad MAU2 och visar att förändringar i denna gen kan orsaka en distinkt form av Cornelia de Lange-syndrom, ofta med kortväxthet och liten huvudstorlek men generellt mildare inlärningssvårigheter än i de klassiska fallen.
En sällsynt åkomma med många ansikten
Cornelia de Lange-syndrom är mest känt för sitt karakteristiska ansiktsuttryck, tillväxtbegränsning och utvecklingsutmaningar, men det kan se väldigt olika ut från person till person. De flesta diagnostiserade har förändringar i en nyckelgen kallad NIPBL, som hjälper till att organisera hur DNA paketeras och läses i cellerna. Ändå saknar en betydande andel patienter alterationer i de vanliga generna, vilket lämnar familjer utan klara svar. Eftersom MAU2 normalt samarbetar nära med NIPBL i samma cellulära maskineri misstänkte forskarna att subtila fel i MAU2 kan förklara några av dessa oförklarade fall.
Kopplingen mellan MAU2-varianter och mänskliga symtom
Forskarna samlade en grupp på 18 individer som alla bar sällsynta förändringar i en kopia av MAU2-genen. Dessa förändringar sträckte sig från små utbyten av en byggsten i proteinet till prematura stoppkoder som förkortade det. Kliniskt delade de flesta av dessa individer två framträdande drag: kortväxthet och mikrocefali, vilket betyder en huvudstorlek mindre än väntat för åldern. Många hade lindriga till måttliga inlärningssvårigheter och vissa ansiktsdrag som överlappade med Cornelia de Lange-syndrom, om än generellt mindre uttalade än i typiska NIPBL-relaterade fall. Med ett etablerat kliniskt poängsystem för syndromet uppfyllde tre personer kriterierna för ”klassiskt” Cornelia de Lange, flera hamnade i ett ”icke-klassiskt” spann och ett par var så milda att de troligen inte skulle ha uppmärksammats utan genetisk testning.
Hur felaktig MAU2 stör genomets organisation
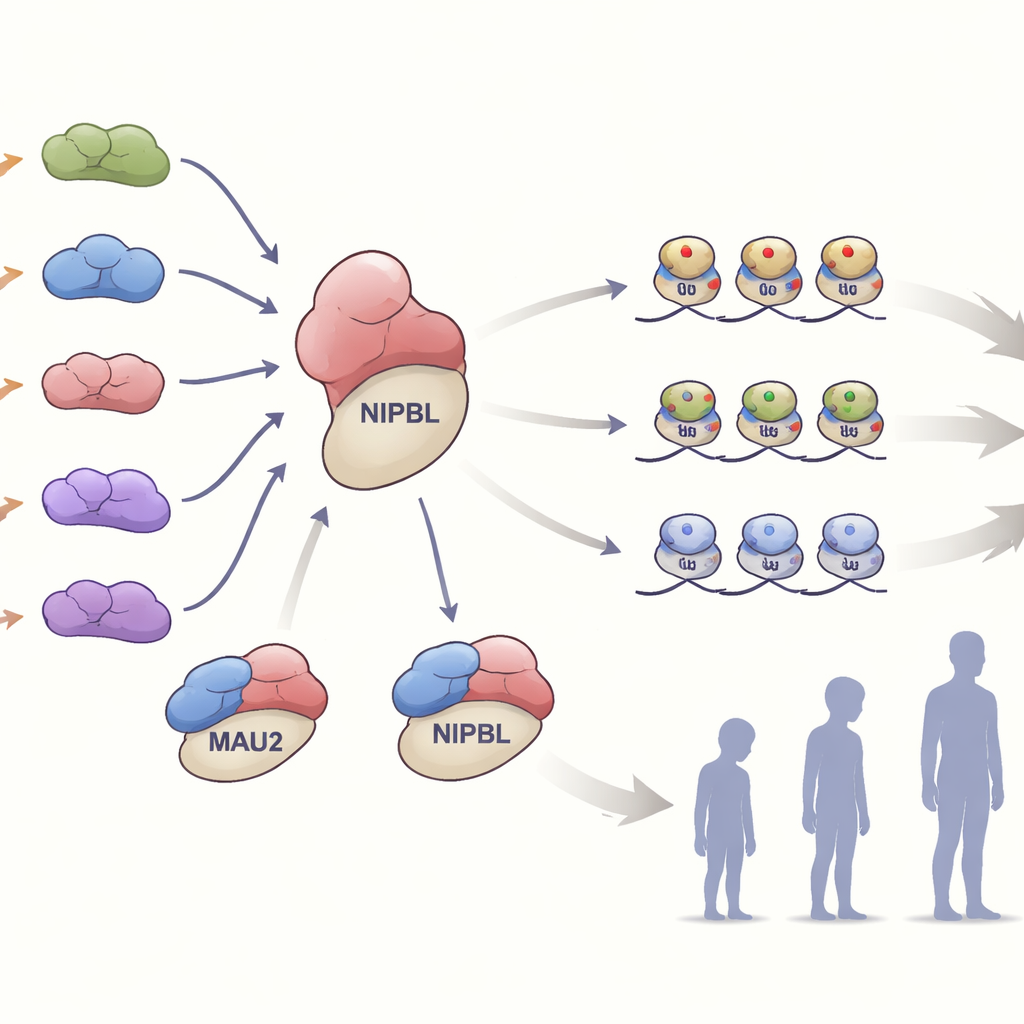
I cellerna bildar MAU2 ett tätt partnerskap med NIPBL för att lasta på en ringformad proteinkomplex kallad cohesin på DNA. Detta komplex hjälper till att vika genomet och finjustera vilka gener som är aktiva eller inaktiva. Teamet testade hur de olika MAU2-förändringarna påverkade detta samspel. Många av varianterna som helt enkelt tog bort eller ändrade ett litet segment av proteinet försvagade dess bindning till NIPBL utan att förstöra något av proteinerna helt. Andra varianter, som introducerade frameshift-mutationer eller tidiga stoppkoder, minskade MAU2-nivåerna med ungefär hälften, en situation som kallas haploinsufficiens. I celler från en familj med en sådan trunkerande variant minskade också nivåerna av NIPBL, vilket understryker hur hårt de två partnerna är beroende av varandra för stabilitet.
Läsa de epigenetiska fingeravtrycken
Studien gick längre än DNA-sekvensen och granskade de ”epigenetiska” markörer som sitter ovanpå genomet. I blodceller från drabbade individer mätte forskarna DNA-metylering, en kemisk markör som ofta speglar hur gener regleras. De flesta MAU2-variantbärare visade ett metyleringsmönster som nära matchade den kända signaturen för Cornelia de Lange-syndrom, vilket gav stark molekylär evidens för att MAU2-störning konvergerar mot samma sjukdomsväg som NIPBL. Intressant nog upptäckte teamet också två MAU2-specifika metyleringssignaturer som inte helt överlappade med det klassiska mönstret. Vissa individer som saknade den vanliga Cornelia de Lange-signaturen bar ändå en av dessa MAU2-specifika profiler och hade mildare symtom, vilket tyder på att partiell störning av MAU2 kan lämna ett eget igenkännligt epigenetiskt avtryck.
En musmodell speglar mänskliga tillväxt- och hjärnförändringar
För att se hur MAU2-förlust påverkar en hel organism studerade forskarna möss som konstruerats för att bara bära en fungerande kopia av Mau2-genen, vilket speglar situationen hos människor. Möss som helt saknade Mau2 överlevde inte, vilket visar hur väsentlig genen är. De överlevande halvdos-mössene var något kortare än sina normala kullsyskon och hade mindre hjärnor med specifika regioner reducerade i storlek, tillsammans med förstorade vätskefyllda utrymmen. Dessa fynd speglar kortväxthet, mikrocefali och subtila hjärnavvikelser som ses hos människor med MAU2-varianter och stärker kopplingen mellan genen, hjärnans utveckling och yttre drag.
Vad detta betyder för familjer och diagnostik
Tillsammans etablerar de mänskliga och musdata tydligt MAU2 som en gen som kan orsaka Cornelia de Lange-syndrom och närliggande tillstånd. Förändringar som kraftigt rubbar MAU2–NIPBL-partnerskapet tenderar att ge den fulla Cornelia de Lange-epigenetiska signaturen och mer igenkännliga ansiktsdrag, medan varianter med mildare effekter kan leda till lindrigare kortväxthet och liten huvudstorlek med endast MAU2-specifika molekylära fingeravtryck. För familjer innebär detta att lägga till MAU2 i diagnostiska paneler och att överväga epigenetisk profilering kan hjälpa till att förklara tidigare olösta fall, och det tydliggör hur även små störningar i genomets organiserande maskineri kan få vida följder för tillväxt och utveckling.
Citering: Parenti, I., Hesters, A., Gil-Salvador, M. et al. Pathogenic variants in the cohesin loader subunit MAU2 underlie a distinct Cornelia de Lange Syndrome subtype. Nat Commun 17, 3036 (2026). https://doi.org/10.1038/s41467-026-71177-6
Nyckelord: Cornelia de Lange-syndrom, MAU2-genen, cohesin-laddare, DNA-metylering, neuroutvecklingsstörningar