Clear Sky Science · ar
الطفرات الممرِضة في وحدة تحميل الكوهيسين MAU2 تُسفِر عن نوع مميز من متلازمة كورنليا دي لانج
عندما يشكّل تغيير جيني طفيف النمو والتطور
متلازمة كورنليا دي لانج هي حالة نادرة تؤثر على النمو والملامح الوجهية والتعلّم. بالنسبة للعديد من العائلات، وحتى بعد الفحوصات الجينية، يبقى السبب مجهولاً. تركز هذه الدراسة على جين أقل شهرة يُدعى MAU2 وتُبيّن أن تغيّرات في هذا الجين يمكن أن تُسَبِّب شكلاً مميزاً من متلازمة كورنليا دي لانج، غالباً مع قصر القامة وصغر حجم الرأس، لكن باضطرابات تعلّم أخف عمومًا مقارنةً بالحالات الكلاسيكية.
حالة نادرة ذات مظاهر متعددة
تُعرَف متلازمة كورنليا دي لانج بمظهرها الوجهي المميز، وتقييد النمو، والتحديات التطورية، لكنها قد تظهر بطرق مختلفة من شخص لآخر. يحمل معظم الأفراد المشخَّصين تغيّرات في جين محوري يُدعى NIPBL، الذي يساعد في تنظيم كيفية تغليف وقراءة الحمض النووي داخل الخلايا. ومع ذلك، يفتقر عدد لا بأس به من المرضى إلى تغيّرات في أي من الجينات المعهودة، مما يترك العائلات دون إجابات واضحة. وبما أن MAU2 يعمل عادةً جنباً إلى جنب مع NIPBL في نفس الآلية الخلوية، راح الباحثون يشتبهون بأن أعطاباً طفيفة في MAU2 قد تفسر بعض هذه الحالات غير المبرّرة.
ربط طفرات MAU2 بالأعراض لدى البشر
جمع الباحثون مجموعة مكوّنة من 18 فرداً كلٌّ منهم يحمل تغيّرات نادرة في نسخة واحدة من جين MAU2. تراوحت هذه التغيّرات بين استبدالات صغيرة لحمض أميني واحد إلى إشارات إيقاف مبكرة تقصّر البروتين. سريريًا، شارك معظم هؤلاء الأفراد علامة بارزة هي قصر القامة وصغر الرأس (صغر محيط الرأس مقارنة بالمفترض لعمر الشخص). عانى العديد منهم من صعوبات تعلم خفيفة إلى متوسطة، وامتلك بعضهم ملامح وجهية متداخلة مع متلازمة كورنليا دي لانج، رغم أنها كانت عامةً أقل وضوحاً من حالات NIPBL النمطية. باستخدام نظام تسجيل سريري معتمد للمتلازمة، وُجد أنّ ثلاثة أشخاص يطابقون معايير «الكلاسيكية» لمتلازمة كورنليا دي لانج، وسقط عدد آخر ضمن نطاق «غير كلاسيكي»، وكان بعضهم خفيف الأعراض لدرجة أنه لما كان لوجود الفحص الجيني لَمَرضهم أن يُكتشَف.
كيف يعطّل MAU2 المعيب تنظيم الجينوم
داخل الخلايا، يشكل MAU2 شراكة وثيقة مع NIPBL لتحميل معقّد بروتيني حلقي الشكل يُسمى الكوهيسين على الحمض النووي. يساعد هذا المعقّد في طي الجينوم وضبط أي الجينات تكون مُفعّلة أو مُطفأة. اختبر الفريق كيف أثّرت تغيّرات MAU2 المختلفة على هذه الشراكة. أضعفت العديد من المتغيرات التي أزالت أو غيرت قطعة صغيرة من البروتين قبضته على NIPBL دون أن تدمر أيًا من البروتينين تمامًا. في حين أن متغيرات أخرى، مثل تلك التي تُحدث إزاحة إطار القراءة أو إشارات إيقاف مبكرة، خفضت مستويات MAU2 بنحو النصف، وهي حالة تُعرف بنقص النسخة (haploinsufficiency). في خلايا من أسرة تحمل مثل هذا المتغير المقطوع، أدى انخفاض بروتين MAU2 أيضًا إلى تقليل مستويات NIPBL، مما يبرز مدى اعتماد الشريكين على بعضهما البعض من حيث الثبات البروتيني.
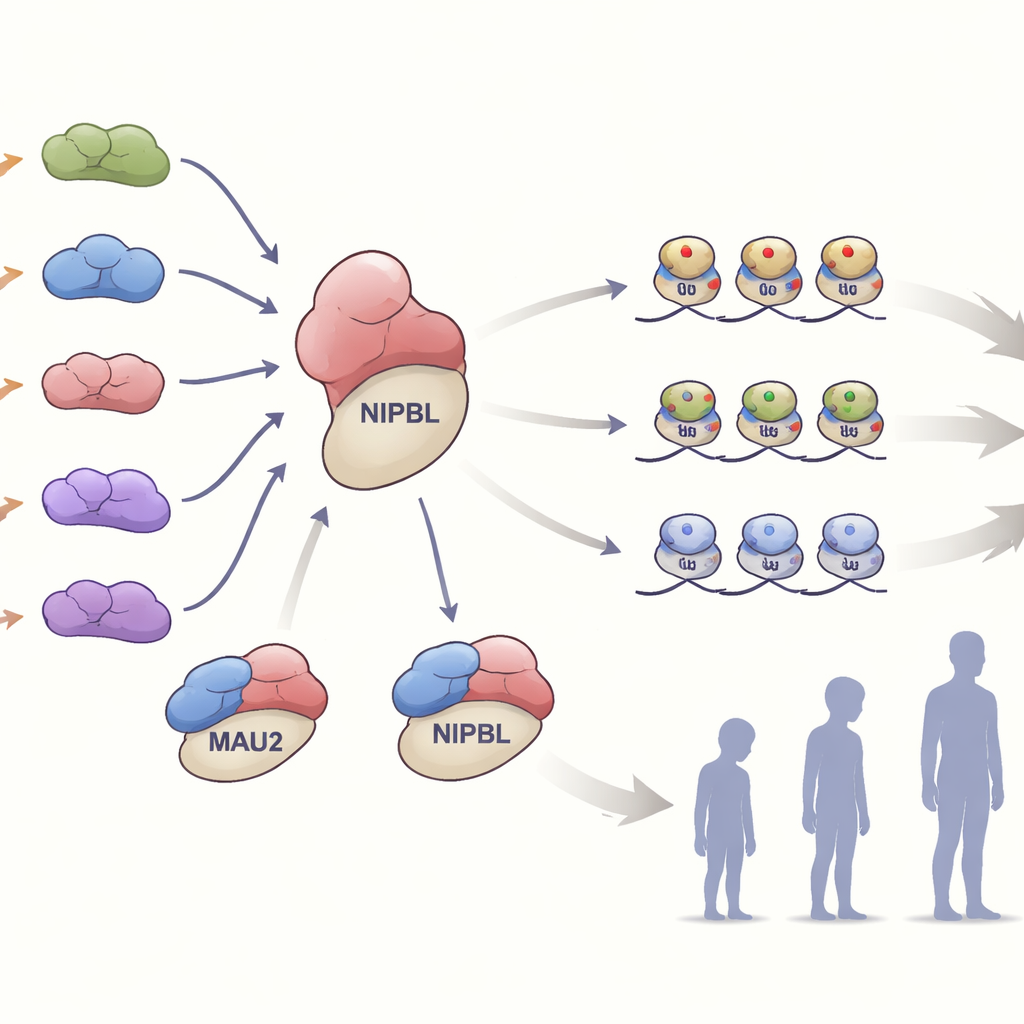
قراءة البصمات فوق الجينية
تجاوزت الدراسة تسلسل الحمض النووي لتفحص العلامات «فوق الجينية» التي تجلس فوق الجينوم. في خلايا الدم من الأفراد المتأثرين، قاس الباحثون مثيلة الحمض النووي، وهي علامة كيميائية تعكس غالبًا كيفية تنظيم الجينات. أظهر معظم حاملي متغيرات MAU2 نمطَ مثيلة يطابق عن كثب البصمة المعروفة لمتلازمة كورنليا دي لانج، مما قدّم دليلاً جزيئيًا قويًا أن تعطُّل MAU2 يتقاطع مع نفس مسار المرض المتصل بـ NIPBL. ومن المثير للاهتمام، أن الفريق اكتشف أيضًا بصمتين مثيليتين خاصتين بـ MAU2 لا تتطابقان تمامًا مع النمط الكلاسيكي. بعض الأفراد الذين افتقروا إلى البصمة الكلاسيكية لحالة كورنليا دي لانج حملوا أحد هذه الأنماط الخاصة بـ MAU2 وكان لديهم أعراض أهبَط، مما يوحي أن التعطيل الجزئي لـ MAU2 يمكن أن يترك أثرًا فوق جينيًا مميّزًا يمكن التعرف عليه.
نموذج فأر يعكس تغيّرات النمو والدماغ عند البشر
لمعرفة كيف يؤثر فقدان MAU2 على كائن حي كامِل، درس الباحثون فئرانًا مهندَسة لتحمل نسخةٍ عملٍ واحدة فقط من جين Mau2، مقلدين الحالة البشرية. لم تُبقَ الفئران الخالية تمامًا من Mau2 على قيد الحياة، مما يؤكد أن الجين أساسي. كانت الفئران التي تملك نصف الجرعة أقصر قليلًا من إخوتها الطبيعيين، وامتلكت أدمغة أصغر مع تقلص مناطق محددة وزيادة في المساحات المملوءة بالسوائل. تعكس هذه النتائج قصر القامة وصغر محيط الرأس والتشوهات الدماغية الطفيفة المرصودة لدى الأشخاص ذوي متغيرات MAU2، مما يعزّز الصلة بين الجين وتطور الدماغ والصفات الظاهرية.
ماذا يعني هذا للعائلات والتشخيص
معًا، تؤسس بيانات البشر والفئران بشكل راسخ لـ MAU2 كجين قادر على التسبّب في متلازمة كورنليا دي لانج والحالات القريبة منها. تميل التغيّرات التي تعطل بقوة شراكة MAU2–NIPBL إلى إنتاج البصمة فوق الجينية الكاملة لكورنليا دي لانج وملامح وجهية أكثر قابلية للتعرف، بينما قد تؤدي المتغيرات ذات التأثير الأخف إلى قصر قامة وصغر رأس أخف مع بصمات جزيئية خاصة بـ MAU2 فقط. بالنسبة للعائلات، يعني هذا أن إضافة MAU2 إلى لوحات الفحوصات التشخيصية والنظر في التحليل الفوق جيني يمكن أن يساعد في تفسير حالات كانت سابقًا دون حل، كما يبرز كيف أن حتى الخلل الطفيف في آلية تنظيم الجينوم يمكن أن يتسلسل تأثيره ليشكّل النمو والتطور.
الاستشهاد: Parenti, I., Hesters, A., Gil-Salvador, M. et al. Pathogenic variants in the cohesin loader subunit MAU2 underlie a distinct Cornelia de Lange Syndrome subtype. Nat Commun 17, 3036 (2026). https://doi.org/10.1038/s41467-026-71177-6
الكلمات المفتاحية: متلازمة كورنليا دي لانج, جين MAU2, محمل الكوهيسين, مثيلة الحمض النووي, اضطرابات النمو العصبي