Clear Sky Science · sv
En högaffinitets split-HaloTag för märkning av proteiner i levande celler
Att se den dolda maskineriet inne i levande celler
Modern biologi är beroende av möjligheten att iaktta enskilda proteiner i arbete inne i levande celler, men att fästa starka molekylära ”ficklampor” på dessa proteiner utan att störa dem är förvånansvärt svårt. Denna studie presenterar ett nytt märkningssystem som stoppar in en liten tagg i ett protein och sedan belyser den med kraftfulla kemiska färgämnen, vilket gör det möjligt för forskare att följa även sällsynta, känsliga mål i realtid med toppmoderna mikroskop.
En liten tagg möter ett kraftfullt ljus
Arbetet bygger på HaloTag, en mycket använd proteinmärkare som bildar en permanent bindning till särskilda fluorescerande färgämnen. HaloTag är ljusstark och mångsidig men också skrymmande, vilket kan påverka det normala beteendet hos det protein den är fuserad med. Författarna löser detta genom att dela HaloTag i två delar: en mycket liten peptid kallad Hpep, bara 14 aminosyror lång, och en större partnerprotein kallad cpHaloΔ3. Den lilla Hpep kan byggas in direkt i proteinet av intresse, medan cpHaloΔ3 tillförs separat. När de träffas inne i en cell hakar de i varandra med mycket hög affinitet och återskapar en aktiv HaloTag som kan fånga ljusstarka färgämnen.
Designa en ihopknäppbar ljusbrytare
För att göra detta split-system praktiskt var teamet tvunget att balansera flera egenskaper samtidigt. Hpep och cpHaloΔ3 behövde känna igen varandra extremt effektivt så att även en enda kopia på ett lågt uttryckt protein skulle märkas, samtidigt som cpHaloΔ3 ensam skulle förbli i princip inaktiv för att undvika oönskat bakgrundsljus. Med hjälp av jästdisplay och höggenomströmmande cellsortering skannade de bibliotek av lätt förändrade cpHalo-fragment för varianter som var tysta när de var ensamma men snabba och effektiva när de bundit Hpep. Slutversionen, cpHaloΔ3, kombinerade nanomolär bindningsstyrka, låga oönskade märkningar och snabb reaktion med färgämnen när de två delarna återförenades. Varianter av Hpep justerades också så att de, när de var bundna, subtilt påverkade hur de fästa färgämnena betedde sig och ändrade både ljusstyrka och fluorescenslivslängd.
Att belysa verkliga cellulära strukturer
Forskarna visade sedan att deras split-HaloTag fungerar i en rad olika cellulära sammanhang. De fäste Hpep till proteiner som markerar kärnan, mitokondriens yta och nukleära omslaget, och samexprimerade cpHaloΔ3 i humana celler. Efter tillsats av cellpermeabla HaloTag-färgämnen gav den återskapade taggen skarpa bilder av de förväntade strukturerna med mycket lite bakgrund från obundna cpHaloΔ3. Viktigt är att eftersom Hpep är så liten kunde den infogas direkt i cellens egna gener med CRISPR utan behov av att klona in stora DNA‑konstrukter. Teamet demonstrerade sömlösa "knock‑ins" för många olika endogena proteiner, från strukturella komponenter som vimentin till membrankanaler och klatrin, och visade att dessa kunde berikas och analyseras med flödescytometri och mikroskopi.
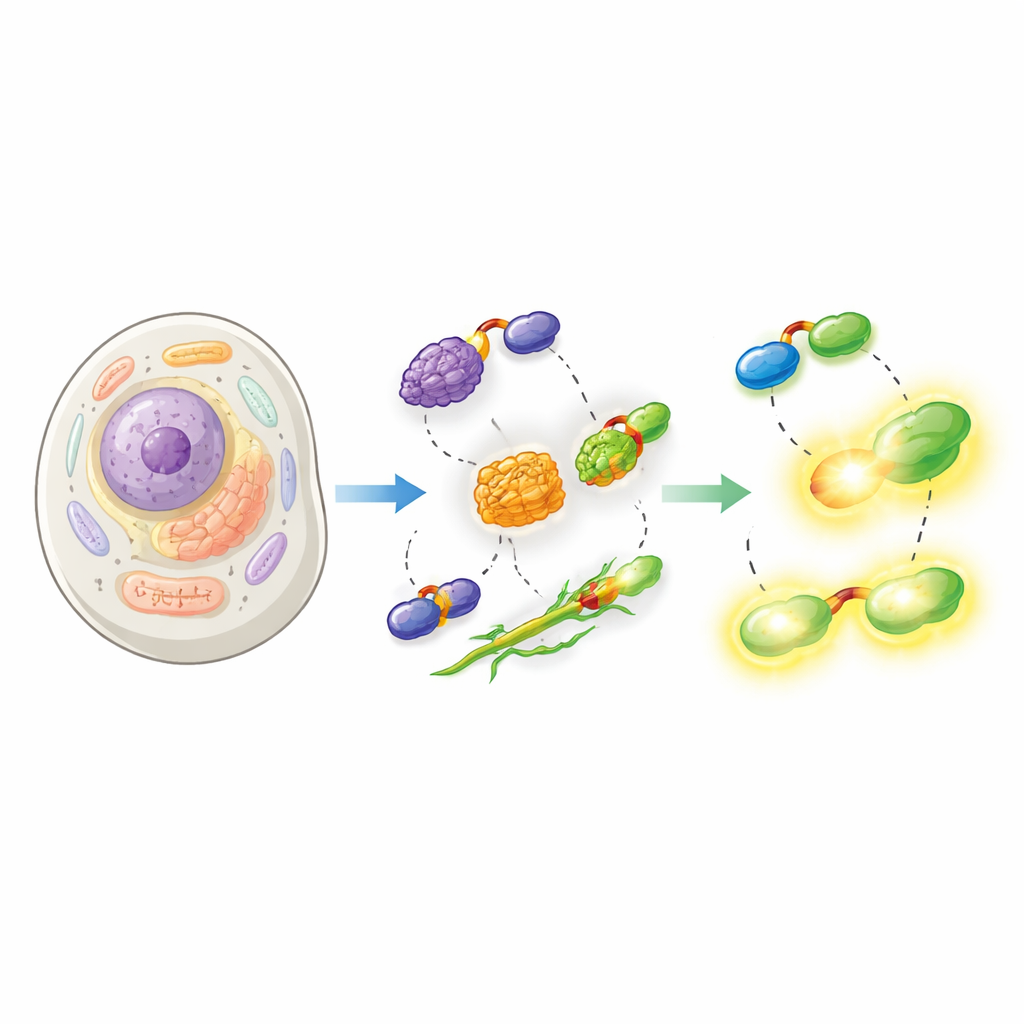
Pressa gränserna för modern mikroskopi
Förutom standard fluorescensavbildning testades den nya taggen med några av de mest krävande optiska teknikerna. Med specialfärger kompatibla med superupplösning och utplåningsmikroskopi kunde författarna upplösa mitokondriemembran och mikrotubuli med detaljer långt under den konventionella diffraktionsgränsen, i vissa fall i levande celler. De kombinerade också systemet med expansionsmikroskopi, där bevarade celler fysiskt sväller för att avslöja fin struktur, och med fluorescenslivslängdsavbildning. Olika Hpep‑varianter ändrade hur länge färgen stannade i sitt exciterade tillstånd, vilket gjorde det möjligt att särskilja två proteiner märkta med samma färg enbart genom deras livslängder och möjliggjorde multiplexad avbildning med en enda cpHaloΔ3‑partner.
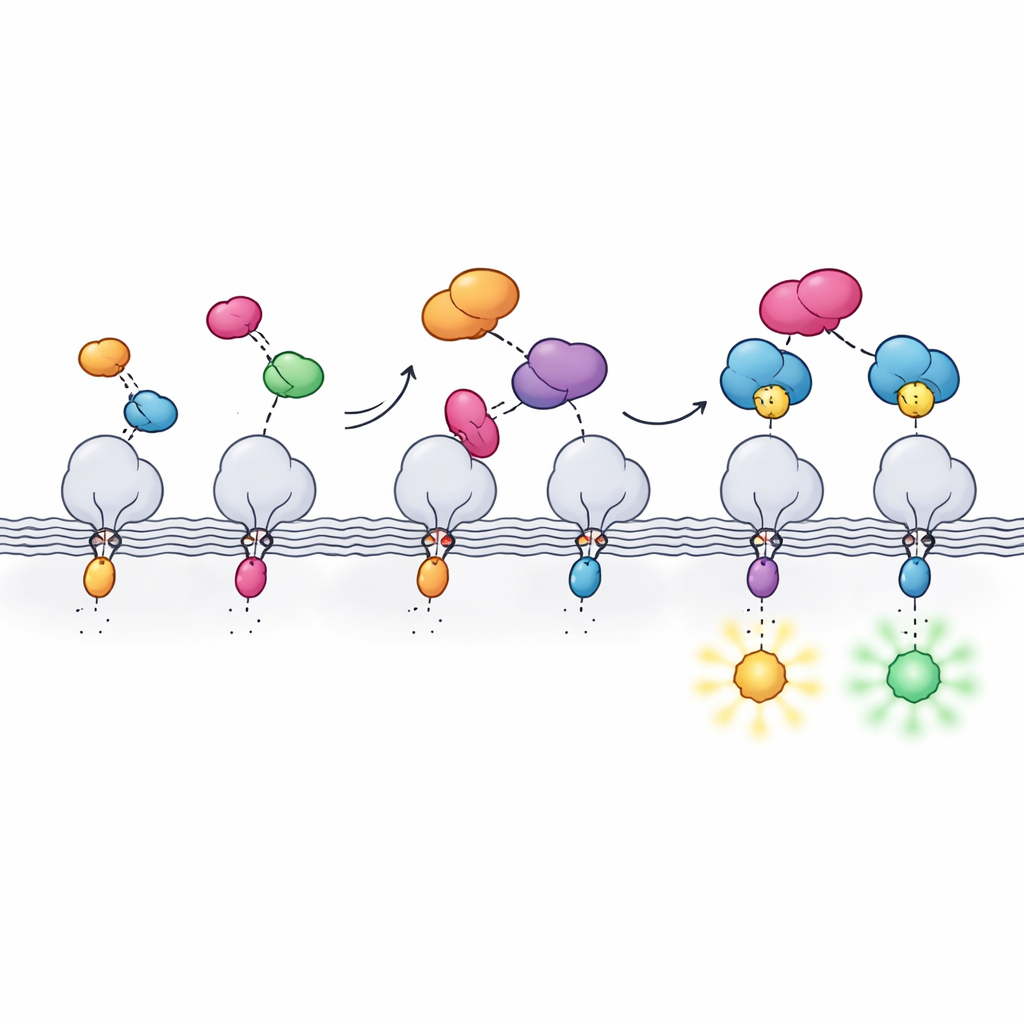
Varför denna nya tagg är betydelsefull
Tillsammans skapar dessa framsteg ett kompakt, flexibelt märkningssystem som förenar den genetiska bekvämligheten hos små peptidtaggar med den optiska kraften hos syntetiska färgämnen. Hpeps lilla storlek gör den lätt att infoga i endogena gener och mindre benägen att störa proteinets funktion, medan cpHaloΔ3 ger starka, stabila färger när och där de behövs. Resultatet är ett högkontrast-, låg‑bakgrundssätt att observera proteiner inne i levande celler, kompatibelt med avancerade mikroskop och experiment med flera mål. Detta split‑HaloTag‑verktygslåda bör hjälpa forskare att kartlägga hur cellulära komponenter är organiserade och hur de förändras över tid i hälsa och sjukdom.
Citering: Lin, YH., Kompa, J., Sun, De. et al. A high-affinity split-HaloTag for live-cell protein labeling. Nat Commun 17, 2865 (2026). https://doi.org/10.1038/s41467-026-71032-8
Nyckelord: proteinmärkning, avbildning av levande celler, HaloTag, CRISPR‑taggning, superupplösningsmikroskopi