Clear Sky Science · he
תגובת HaloTag מפוצלת עם הזיקה גבוהה לסימון חלבונים בתאים חיים
להתבונן במנגנון הנסתר בתוך תאים חיים
הביולוגיה המודרנית תלויה ביכולת לצפות בחלבונים בודדים פועלים בתוך תאים חיים, אך חיבור "פנסונים" מולקולריים בוהקים לאותם חלבונים בלי להפריע להם הוא אתגר לא טריוויאלי. מחקר זה מציג מערכת סימון חדשה שמטמיעה תווית זעירה בתוך חלבון ואז מאירה אותה עם צבעים כימיים עוצמתיים, מה שמאפשר לחוקרים לעקוב בזמן אמת אחרי מטרות נדירות ורגישות באמצעות מיקרוסקופים מתקדמים.
תווית זעירה פוגשת אור עוצמתי
העבודה מבוססת על HaloTag, תווית חלבון נפוצה שיוצרת קשר קבוע עם צבעים פלואורסצנטיים מיוחדים. HaloTag בהירה ורב-שימושית אך גם יחסית גדולה, מה שעלול לשבש את ההתנהגות הטבעית של החלבון אליה היא מחוברת. המחברים פתרו זאת על ידי פיצול ה-HaloTag לשני חלקים: פפטיד זעיר בשם Hpep, שכולל רק 14 חומצות אמינו, ובן זוג חלבוני גדול יותר שנקרא cpHaloΔ3. ה-Hpep הקטן ניתן לשזור ישירות לתוך החלבון הרצוי, בעוד ש-cpHaloΔ3 מסופק בנפרד. כשהשניים נפגשים בתוך התא, הם מתחברים בזיקה גבוהה ושחזורים HaloTag פעיל שיכול לקשור צבעים בוהקים.
עיצוב מתג אור שמתאים לשרטוט
כדי להפוך את המערכת המפוצלת למעשית, הצוות נדרש לאזן מספר תכונות בבת אחת. ה-Hpep וה-cpHaloΔ3 צריכים להכיר זה את זה בחוזקה רבה כדי שגם עותק בודד על חלבון בדל-שפע יסומן, אך cpHaloΔ3 לבדו צריך להישאר כמעט בלתי פעיל כדי למנוע זוהר רקע לא רצוי. באמצעות תצוגת שמרים ומיון תאי בריבוי גבוה הם סרקו ספריות של שברי cpHalo משוננים למציאת וריאנטים שקטים כשהם לבד אך מהירים ויעילים לאחר קשירה ל-Hpep. הגרסה הסופית, cpHaloΔ3, שילבה קשירה בננומולר, סימון מקרי נמוך ותגובה מהירה לצבעים לאחר איחוד שני החלקים. גם וריאנטים של Hpep כוונו כך שכאשר הם קשורים הם ישפיעו בעדינות על התנהגות הצבעים המחוברים, ישנו הן את הבהירות והן את משך החיים הפלואורסצנטי.
מאירים מבנים תאיים במציאות
החוקרים הראו גם שה-split-HaloTag שלהם פועל במגוון חומרים תאיים. הם שזרו Hpep לחלבונים שמסמנים את הגרעין, פני שטח המיטוכונדריה ומעטפת הגרעין, ובאותו זמן הביעו cpHaloΔ3 בתאים אנושיים. לאחר הוספת צבעי HaloTag חדירי תא, התווית המשוקמת הפיקה תמונות חדות של המבנים הצפויים עם מעט מאוד רקע מ-cpHaloΔ3 בלתי קשור. חשוב מכך, מאחר ש-Hpep קטן כל כך, ניתן להחדירו ישירות לגנים אנדוגניים באמצעות CRISPR ללא צורך בשיבוט קונסטרוקטים DNA גדולים. הצוות הדגים "נוק-אין" רציפים עבור חלבונים אנדוגניים רבים, מרכיבים מבניים כגון וימנטין ועד תעלות ממברנה וקלאטרין, והראה שניתן להעשירם ולנתחם בעזרת ציטומטריית זרימה ומיקרוסקופיה.
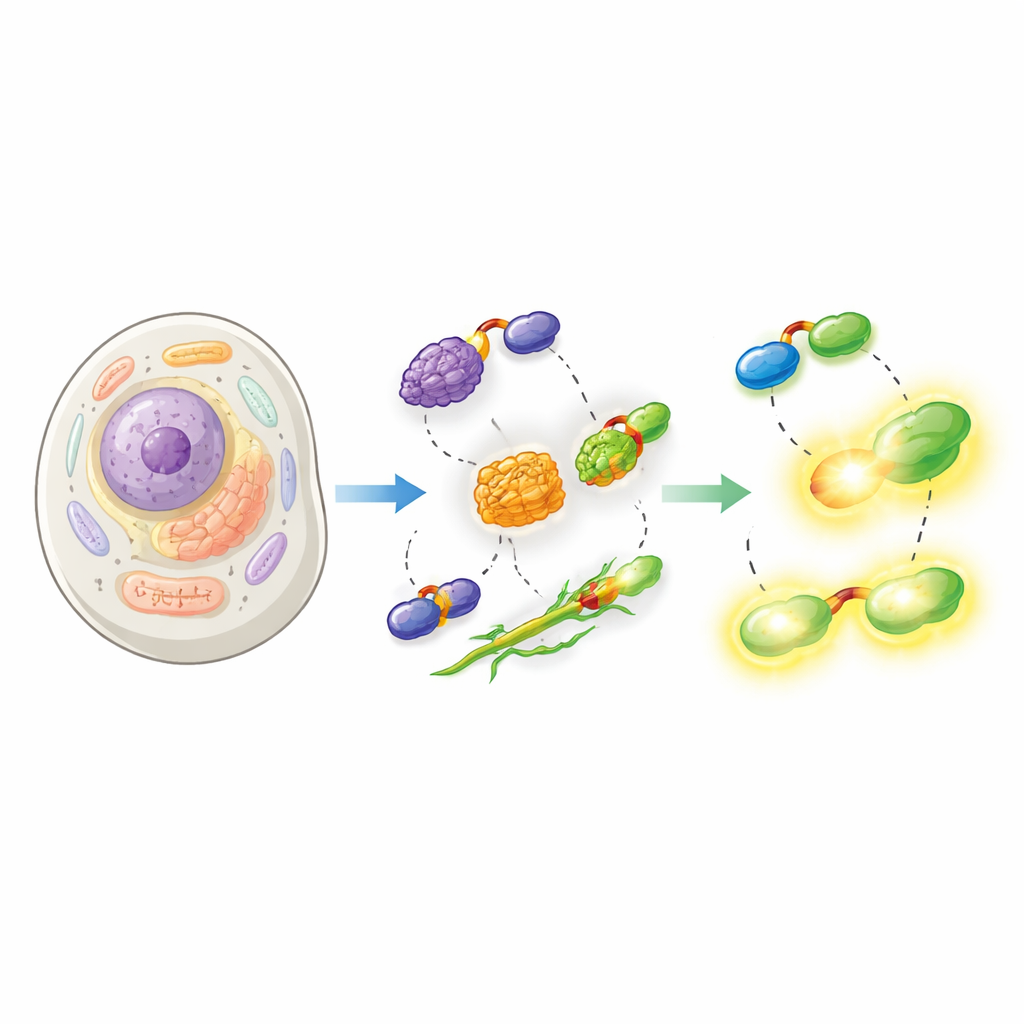
לדחוף את גבולות המיקרוסקופיה המודרנית
מעבר לדימות פלואורסצנטי סטנדרטי, התווית החדשה נבדקה בטכניקות האופטיות התובעניות ביותר. באמצעות צבעים מיוחדים התואמים למיקרוסקופיה ברזולוציה-על ולמיקרוסקופיית דילול הם פתרו ממברנות מיטוכונדריאליות ומיקרוטובולים בפרטים מתחת למגבלת הדיפרקציה הקונבנציונלית, ולעיתים בתאים חיים. הם גם שילבו את המערכת עם מיקרוסקופיה בהרחבה, שנועלת תאים ששמרו על מבנה והנפיחה פיזית כדי לחשוף פרטים עדינים, וכן עם הדמיית משך חיים פלואורסצנטי. וריאנטים שונים של Hpep שינו את משך הזמן שבו הצבע נשאר במצב מעורר, מה שאפשר להבדיל בין שני חלבונים המסומנים באותו צבע על בסיס משך החיים בלבד ולהנגיש דימות מרובה-מטרות עם אותו שותף cpHaloΔ3.
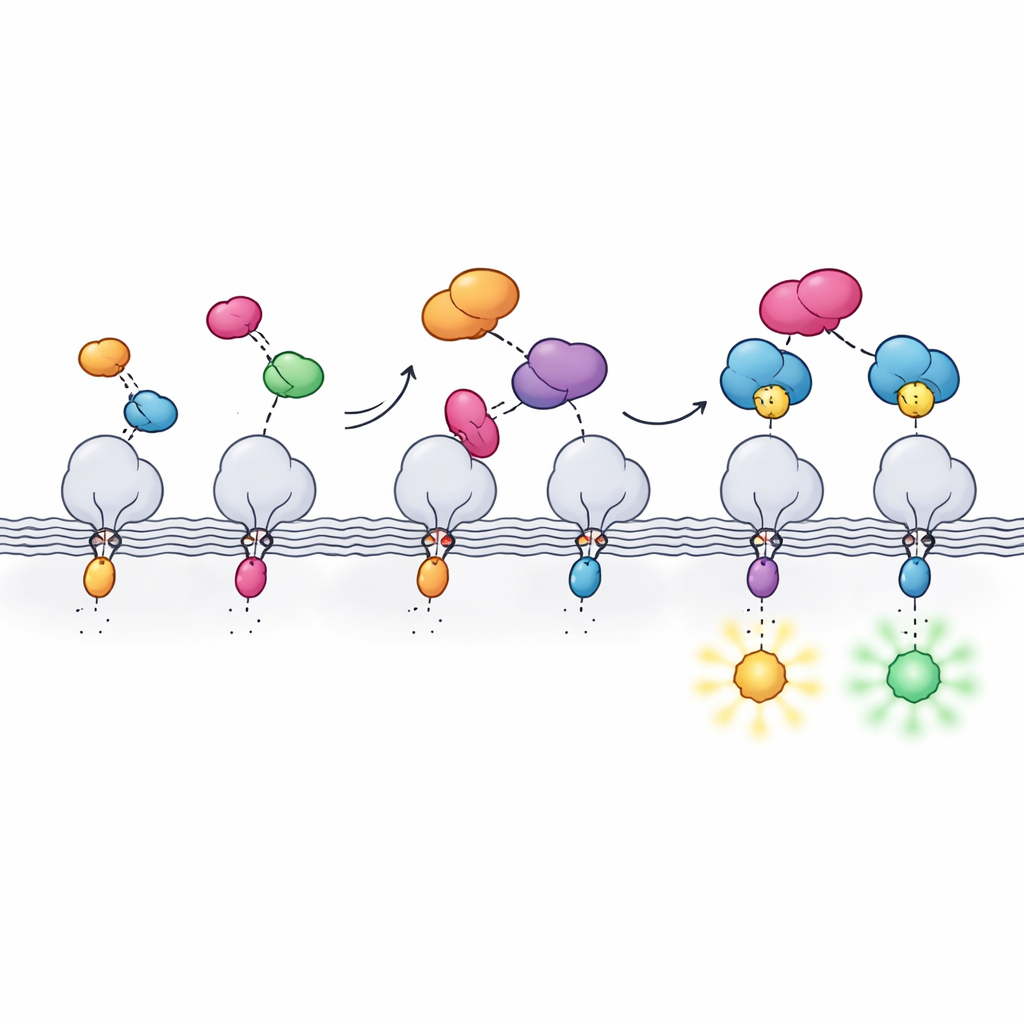
מדוע התווית החדשה חשובה
ביחד, החידושים הללו יוצרים מערכת סימון קומפקטית וגמישה שמשלבת את הנוחות הגנטית של תוויות פפטיד זעירות עם הכוח האופטי של צבעים סינתטיים. הגודל הקטן של Hpep מקל על ההכנסה לגנים טבעיים ופחות צפוי לשבש את תפקוד החלבון, בעוד cpHaloΔ3 מספק צבעים בהירים ויציבים כשנדרש. התוצאה היא שיטה בקונטרסט גבוה וברקע נמוך לצפייה בחלבונים בתוך תאים חיים, תואמת למיקרוסקופים מתקדמים ולניסויים מרובי-מטרות. ערכת הכלים של split-HaloTag הזו אמורה לסייע לחוקרים למפות כיצד מרכיבי התא מאורגנים וכיצד הם משתנים לאורך זמן במצב בריאותי ומחלה.
ציטוט: Lin, YH., Kompa, J., Sun, De. et al. A high-affinity split-HaloTag for live-cell protein labeling. Nat Commun 17, 2865 (2026). https://doi.org/10.1038/s41467-026-71032-8
מילות מפתח: סימון חלבונים, דימות תאים חיים, HaloTag, תיוג CRISPR, מיקרוסקופיה ברזולוציה-על